Желтуха после операции на желчном
Содержание статьи
Лечение механической желтухи
Механическая желтуха развивается при нарушении оттока желчи из желчного пузыря в двенадцатиперстную кишку. Данное состояние не является самостоятельным заболеванием. Механическая желтуха — это симптом, который характерен для многих болезней органов брюшной полости. Ввиду достаточно большой распространенности, врачам разных специальностей часто приходится сталкиваться с данной проблемой и назначать пациентам различные виды лечения.
Варианты развития механической желтухи
В зависимости от причин появления, симптом может быть опухолевого и неопухолевого генеза. Примерно в половине всех случаев механическая желтуха связана со злокачественными новообразованиями поджелудочной железы, печени, кишечника. Данные органы могут поражаться первичным опухолевым процессом или метастазами из отдаленных очагов.
У второй половины пациентов развитие механической желтухи обусловлено доброкачественными процессами, среди которых наиболее часто отмечаются:
- Воспалительные процессы желчного пузыря и желчевыводящих путей — холецистит, холангит, папиллит и др.
- Невоспалительные заболевания органов брюшной полости: желчекаменная болезнь, стеноз желчевыводящих путей, холангиолитиаз и др.
- Врожденные аномалии: атрезия желчевыводящих путей, дуоденальные дивертикулы, кисты и др.
В редких случаях механическую желтуху могут вызывать паразитарные заболевания. Механизм развития симптома в этом случае связан с попаданием гельминтов в желчные протоки с нарушением их проходимости.

Принципы лечения механической желтухи
Главными задачами, при составлении плана лечения, являются ликвидация холестаза (застоя желчи) и профилактика печеночной недостаточности. Для этого врач составляет комплексную программу, в которую могут быть включены как консервативные, так и оперативные методы.
Диета при механической желтухе
Соблюдать определенные правила питания необходимо как до проведения основного лечения, так и после его завершения. Пациентам с механической желтухой рекомендуется соблюдать питьевой режим, так как вода ускоряет выведение билирубина, за счет чего снижается его негативное действие на организм. Также очень важно полностью отказаться от алкоголя, очень жирной и жареной пищи, майонеза, соусов, острых приправ. Пищу следует употреблять небольшими порциями 5-6 раз в день. При этом необходимо следить за температурой блюда. Она не должна быть слишком горячей или холодной. Оптимальный вариант — это теплая пища, так как она помогает регулировать секрецию желчи, что особенно актуально при механической желтухе.

Среди других общих рекомендаций, которые касаются диеты, можно отметить ограничение количества соли в рационе. Известно, что избыток соли способствует задержке жидкости в организме, вызывает отеки и затрудняет выведение вредных веществ из организма. Пациентам с механической желтухой рекомендуется употреблять не более 4 граммов соли в сутки. В целом точный план питания, калорийность и состав блюд подбираются индивидуально для каждого пациента, с учетом его предпочтений. Существуют списки разрешенных и запрещенных блюд, а также тех продуктов, которые должны быть ограничены. Именно этими списками и руководствуется врач при составлении программы питания. Например, к разрешенным продуктам относятся:
- Овощи (морковь, огурцы, капуста, помидоры, брокколи).
- Бананы и яблоки.
- Сухофрукты.
- Различные каши (гречневая, овсяная, перловая).
- Хлеб с отрубями, макароны, хлебцы.
- Варенье, мед, мармелад.
- Нежирное мясо (кролик, говядина), птица (куриные грудки, филе индейки) и рыба (минтай, хек).
- Фруктовые соки и чай.
Диета при механической желтухе подразумевает полное исключение консервированных овощей, бобовых, винограда, сдобы, белого хлеба, жирного молока, сливок, жирных сортов мяса и рыбы, копченостей, газированных напитков, кофе, животных жиров.
Медикаментозное лечение
Медикаментозная терапия при механической желтухе назначается с целью снижения выраженности симптомов, подготовки пациента к операции и уменьшению риска развития осложнений. Объем медицинской помощи во многом зависит от степени желтухи. Например, при тяжелой степени, медикаментозное лечение проводится в условиях отделения интенсивной терапии и включает в себя:
- Массивную инфузионную терапию.
- Форсированный диурез.
- Витаминотерапию.
- Гепатопротекторы.
- Аминокислоты.
- Стимуляторы метаболизма.
- Гормональные препараты.
Для снятия симптомов, при легких формах механической желтухи могут назначаться спазмолитики, обволакивающие препараты, антациды и другие лекарственные средства.
Хирургическое лечение
Хирургическое лечение является единственным эффективным способом, который позволяет восстановить проходимость желчных путей и устранить тем самым причину механической желтухи. Все известные виды операций можно разделить на две группы: малоинвазивные методики и прямые операции.
Малоинвазивные методы хирургического лечения
Данная группа методов отличается высокой эффективностью и малой травматичностью, однако применять их у всех пациентов подряд невозможно ввиду определенных ограничений. Малоинвазивное лечение механической желтухи проводится при помощи эндоскопических методик и чрескожной чреспеченочной холангиостомии. Эндоскопические операции могут быть следующих видов:
- Эндоскопическая папиллосфинктеротомия и литоэкстракция.
- Местная литотрипсия и литоэкстракция.
- Бужирование и стентирование желчных протоков.
В этих случаях для лечения механической желтухи применяется гастродуоденоскоп со специальными инструментами, которые позволяют дробить и извлекать камни, устанавливать стенты, удалять ткани. Эндоскопические операции в большинстве случаев проводятся без общего наркоза и не требуют длительного времени на реабилитацию.
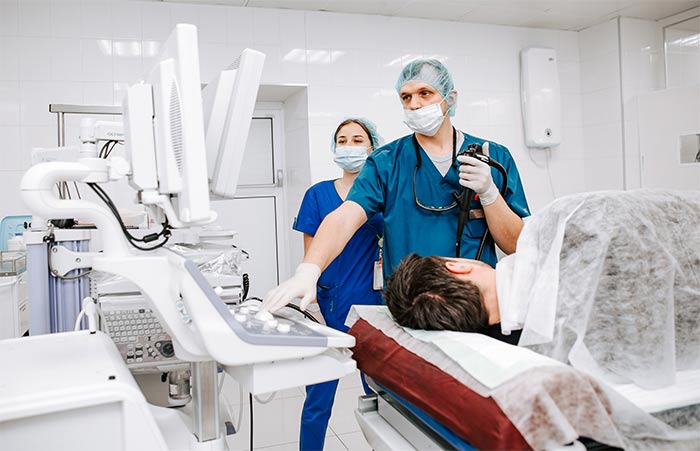
Чрескожная чреспеченочная холангиостомия применяется в тех случаях, когда невозможно выполнить декомпрессию желчевыводящих путей при помощи гастродуоденоскопа. Суть операции заключается в установке дренажной трубки под контролем УЗИ или рентгена. При этом специальной пункционной иглой прокалывается кожа, мышцы передней брюшной стенки и ткань печени. В дальнейшем дренажная трубка может использоваться не только для отвода желчи, но и для введения антибактериальных или других препаратов непосредственно в желчные протоки.
Прямые хирургические вмешательства позволяют сформировать полноценный доступ к желчному пузырю и устранить механическую желтуху любой сложности. Хирург может накладывать анастомозы, устанавливать стенты, выполнять реконструктивные операции. Вмешательство может выполняться при помощи лапароскопических инструментов, либо классическим открытым полостным методом. Последний вариант является наиболее травматичным, требует длительной реабилитации и сопровождается повышенным риском развития осложнений, поэтому его применяют только при лечении сложных случаев механической желтухи.
Общие принципы лечения механической желтухи
Если говорить в общем, то тактика лечения механической желтухи включает два этапа. На первом этапе назначается консервативная терапия и малоинвазивные методы хирургического лечения. При этом рекомендуется проводить такое лечение в первые 2-3 дня с момента поступления пациента в стационар. Если данные методы оказались неэффективными, то переходят ко второму этапу лечения механической желтухи, который подразумевает более радикальные методы. Лечение на пике желтухи связано в высоким риском развития послеоперационных осложнений, поэтому его проводят только при наличии жизненных показаний.
Другие методы лечения
Эффективное лечение желтухи подразумевает устранение основного заболевания, которое привело к развитию данного симптома. Для этого необходимо применять либо консервативные, либо оперативные методы. Другие варианты лечения механической желтухи, в частности, народная медицина, лечение в домашних условиях и самолечение не помогут достичь желаемого результата. На определенный промежуток времени они помогут скрыть симптомы и облегчить состояние пациента, но основной процесс продолжит прогрессировать и приведет к развитию осложнений. Поэтому при появлении первых признаков механической желтухи, необходимо обращаться за квалифицированной медицинской помощью, которая поможет радикально решить проблему.
Последствия и прогноз при механической желтухе
Прогноз будет благоприятным в тех случаях, когда лечение желтухи было своевременным и правильным. Большое значение имеет и поведение самого пациента. Если придерживаться принципов правильного питания и строго следовать всем указаниям врача, риск развития рецидива или осложнений будет минимален. В противном случае, вероятность повторной механической желтухи будет очень высокой. Кроме того, повысится риск развития сопутствующих заболеваний, например, печеночной недостаточности, цирроза печени, энцефалопатии, сепсиса и др.
Методы профилактики
Специфических методов, которые помогли бы предотвратить развитие механической желтухи, в настоящее время не разработано. Поэтому упор делается на раннее выявление и эффективное лечение данного состояния. С этой целью необходимо регулярно консультироваться у врача и проходить профилактическое обследование, которое назначит специалист.
Источник
Осложнения после удаления желчного пузыря
Оптимальный метод лечения желчекаменной болезни
На сегодня золотой стандарт — это лапароскопическая холецистэктомия. Выполняется через три или четыре небольших разреза (прокола) с помощью специальной видеокамеры и инструментов. Есть вариант выполнения через один несколько больший разрез в области пупка, вовсе без разреза (через желудок), и даже с помощью робота, но широкого распространения они не получили (преимущества не очевидны, а стоимость выше).
В подавляющем большинстве случаев срок пребывания в клинике — два дня: госпитализация в день операции, выписка на следующий день после контроля анализов, УЗИ. Безусловно, решение о выписке всегда совместно, если пациенту спокойнее подольше побыть под наблюдением, всегда поддержим.
В течение недели после операции обычно рекомендуем щадящий режим, несмотря на вполне хорошее самочувствие. Первые два-три дня могут беспокоить ноющие боли в плече, связано этой с остаточным газом в брюшной полости и бывает после любой лапароскопической операции.
Диета после холецистэктомии
Вопрос очень дискутабельный, на самом деле. На мой взгляд, слухи о необходимости строгой диеты сильно преувеличены.
Отсутствует резервуарная функция желчного пузыря, желчь в ее изначальном виде постоянно поступает в 12-перстную кишку. В связи с этим есть надо почаще (поступает постоянно), малыми порциями и ограничить жиры (желчи, находящейся в ДПК каждый момент времени, должно «хватить» на эмульгацию жиров). Если нарушить диету, ничего особенно страшного не случится, но пациент это поймет (будет больно, и диарея).
Про осложнения холецистэктомии
Все осложнения можно разделить на два вида: возникающие непосредственно во время или в ближайшее время после операции; и отдаленные (пресловутый постхолецистэктомический синдром).
Большинство возникающих во время или сразу после операции осложнений, к счастью, «малые», не угрожающие жизни и здоровью. Это гематомы, серомы, воспаление — суммарно в районе 5 %, чаще всего не требуют никакого особого лечения, не говоря уже о повторных операциях.
Серьезных осложнений во время операции, по большому счету, четыре — это кровотечение, травма желчных протоков, тромбоэмболия легочной артерии и резидуальный холедохолитиаз.
Несмотря на отработанную методику лапароскопической холецистэктомии, исключить их полностью пока не удается даже в клиниках, где накоплен большой опыт выполнения этих операций.
Кровотечение
С кровотечением понятно — оно может возникнуть во время любой операции. При плановой холецистэктомии риск минимальный.
Повреждение желчных протоков
Страшный сон для любого хирурга. По литературным данным частота 0,15-0,36 % и зависит от многих факторов: плановая или экстренная операция (понятно, что плановой риски значительно ниже), выраженности воспалительных и рубцовых изменений в зоне желчного пузыря, конституциональных и анатомических особенностей… Встречается целый ряд аномалий (взаимоотношений анатомических структур в зоне желчного пузыря), которые иногда ставят в тупик даже очень искушенного хирурга. Основное правило здесь — «не уверен — не обгоняй», в том смысле, что мы должны быть абсолютно уверены в понимании анатомии у конкретного пациента. Всегда. Каждый раз. Даже в самых «банальных» случаях.
Безусловно, большое значение имеет опыт хирурга и качество оборудования. Есть целый ряд приемов, которые позволяют минимизировать риск осложнений — техника critical view of safety(для меня и уже многих коллег — обязательна во время каждой операции), интраоперационная холангиография, и даже использование флюоресцентной лапароскопии (ICG). Думаю, технические особенности не очень интересны для «нехирургов», но тем не менее)
Следующее осложнение — это тромбоэмболия легочной артерии
К счастью, довольно редко при лапароскопической холецистэктомии и правильной профилактике, хотя на 100 % предотвратить его до сих пор невозможно. Очень много факторов влияют, в том числе время операции, объем кровопотери, состояние свертывающей системы, наличие варикозной болезни, возраст… Все это учитывается, определяются риски и подбор оптимального варианта профилактики.
«Забытые» камни в желчном протоке или резидуальный холедохолитиаз
Отдельная большая тема для разговоров типа «Если удалить желчный пузырь, камни продолжат образовываться в протоках». Много раз уже писали — это очень редкая история, разве что в ситуации типа персистирующего холангита или муковисцидоза. Подавляющее большинство камней в протоках после удаления желчного пузыря были там на момент удаления, но никак себя не проявляли. До недавнего времени у нас не было безопасного способа диагностики бессимптомного холедохолитиаза. Последние годы активно пользуемся МРТ (это безопасно и информативно). Думаю, это здорово уменьшит количество «забытых камней».
Отдаленные последствия удаления желчного пузыря или постхолецистэктомический синдром (ПХЭС)
Надо сказать, что мифов и страшилок по этому поводу довольно много. Попробую выразить свою точку зрения, основанную на собственном опыте и анализе мировой литературы.
Как следует из названия, под постхолецистэктомическим синдромом подразумевают любые проблемы со стороны желудочно-кишечного тракта после удаления желчного пузыря.
Напомню, что «после» не всегда означает «вследствие». В большинстве случаев к самой операции эти проблемы не имеют никакого отношения, зачастую при внимательном анализе оказывается, что они были у пациента и до операции. Это еще раз подчеркивает необходимость тщательной оценки клинической картины и индивидуального подхода при принятии решения о необходимости удаления желчного пузыря. На мой взгляд, именно недостаточно внимательная оценка симптомов и желание во что бы то ни стало удалить желчный пузырь приводит к появлению большинства комментариев типа «Удалили — только хуже стало» и пр.
Чаще всего за т.н. «ПХЭС» принимают синдром раздраженного кишечника, гастроэзофагеальную рефлюксную, язвенную болезнь и хронический панкреатит. Мышечные или неврогенные боли тоже нельзя списывать со счетов. Почему же ставят диагноз «ПХЭС»? Доктора тоже люди, а людям свойственно идти по пути наименьшего сопротивления.. «Болит? Желчный убрали? Конечно же это ПХЭС!». Выявить истинную причину не так просто, на самом деле.
Если не принимать во внимание ранее описанные осложнения в ходе операции, к реальным отдаленным последствиям холецистэктомии можно отнести две проблемы: послеоперационную диарею и дисфункцию сфинктера Одди.
Послеоперационная диарея
Мнения по поводу причин ее появления разные, большинство экспертов отводит ведущую роль отсутствии резервуарной функции желчного пузыря. При недостаточном обратном всасывании постоянно поступающей желчи, она в большем, чем обычно количестве поступает в толстую кишку, что и провоцирует диарею. Надо сказать, что при желчекаменной болезни функция пузыря уже нарушена, и часть пациентов жалуются на диарею и до операции.
Очень разные данные о частоте этого симптома, от 1 до 35 %. Большинство исследований говорит о 10-15 %. В моей практике намного ниже, но достоверность личных наблюдений, как известно, невелика. Кроме соблюдения диеты (очень важно есть понемногу несколько раз в день), с диареей помогут справиться секвестранты желчных кислот (колестирамин), иногда приходится назначать лоперамид. В подавляющем большинстве случаев диарея проходит довольно быстро.
Есть мнение, подтвержденное экспериментальными исследованиями, что при сохраненном сфинктерном аппарате, общий желчный проток в течение нескольких месяцев частично компенсирует резервуарную функцию желчного пузыря.
Дисфункция сфинктера Одди или ДСО
Проявляется эпизодами довольно интенсивных болей в правом подреберье, напоминающие боли при желчной колике. Причина — в спазме сфинктера Одди (он регулирует поступление желчи из общего желчного протока в 12-перстную кишку).
ДСО бывает двух типов:
- Тип 1 — боли в правом подреберье с расширенными жёлчными протоками и повышенными трансаминазами (АЛТ и АСТ).
- Тип 2 — боли сопровождаются чем-то одним: или расширенные протоки или повышенные трансаминазы.
Тип 1 очень эффективно лечится папиллотомией (рассечением большого дуоденального соска)
Эффективность папиллотомии при 2-м типе ДСО намного меньше (около 40 %), но все таки достаточно, чтобы возможность проведения этой процедуры была очень тщательно рассмотрена.
Резюмируя, хочу еще раз подчеркнуть важность взвешенного, индивидуального подхода к такой «банальной» операции, как холецистэктомия. Были желчные колики или острый холецистит? Безусловно надо оперировать, вероятность дальнейших серьезных проблем намного выше, чем осложнений.
«Случайно» нашли камни в желчном пузыре и нет никаких симптомов? Живите спокойно, соблюдая диету. Появятся симптомы — приходите, не дожидаясь осложнений, поможем!
Источник
Диагностика и лечение ранних билиарных осложнений после холецистэктомии
Заболеваемость желчнокаменной болезнью (ЖКБ) остается высокой среди лиц как пожилого и старческого возраста, так и молодых пациентов. В России число больных ЖКБ за последние 10 лет увеличилось в 2 раза и составляет в зависимости от региона от 5 до 20% взрослого населения [1, 2, 4].
Холецистэктомия до настоящего времени остается основным методом лечения больных ЖКБ. Ежегодно в мире выполняется более 2,5 млн операций. В Москве производится до 7000 операций в год на 100 000 населения, в целом по России холецистэктомии занимают второе место среди всех выполняемых операций [5, 9].
К традиционному лечению ЖКБ с помощью открытой холецистэктомии добавились лапароскопические варианты данного вмешательства и малотравматичные операции из минилапаротомного доступа.
Несмотря на широкое применение оперативного удаления желчного пузыря, исполняемое в различных модификациях, и большой опыт данных вмешательств, результаты этого лечения не удовлетворяют хирургическое сообщество в связи с относительно высокими показателями послеоперационных осложнений (1,5-35%) и летальности (1,1-5,4%) [3].
Наиболее частыми осложнениями раннего послеоперационного периода являются длительное желчеистечение в брюшную полость или по дренажу общего желчного протока (ОЖП) и механическая желтуха. После открытой холецистэктомии (ОХЭ) они отмечаются в 5-15% наблюдений, после холецистэктомии из минидоступа (ХЭМД) — в 3,6%, после лапароскопической холецистэктомии (ЛХЭ) в 2-5% наблюдений [6, 8, 10-12]. Эти осложнения не только утяжеляют страдания пациентов, но и могут привести к летальному исходу.
Целью настоящего исследования является оценка возможностей эндоскопических методов в диагностике и лечении ранних билиарных осложнений после использования различных видов холецистэктомии у больных ЖКБ.
В основу исследования положены результаты 4856 холецистэктомий, выполненных с 2000 по 2007 г. на клинических базах РГМУ ГКБ №12 и ГКБ №13 Москвы. Из общего количества операций холецистэктомия в классическом исполнении имела место в 2122 наблюдений, ХЭМД — в 1024, ЛХЭ — в 1710 наблюдений. Ранние билиарные осложнения в виде послеоперационного желчеистечения и синдрома механической желтухи развились у 135(2,8%) больных (47 и 88 пациентов соответственно).
Среди больных была 91 (67,4%) женщина и 44 (32,6%) мужчины. Возраст больных варьировал от 21 до 81 года (в среднем 58±14 лет). Большинство больных (64,7%) составляли лица трудоспособного возраста.
Из 135 больных 113 (83,7%) поступили в стационар в экстренном порядке по поводу различных форм острого холецистита, при этом 79 (58,5%) пациентов были оперированы в срочном, 29 (21,5%) — в экстренном порядке.
Всем больным в предоперационном периоде проводили комплекс диагностических мероприятий, который включал: общий и биохимический анализы крови с определением уровня маркеров холестаза; ультразвуковое исследование брюшной полости; лапароскопию (у пациентов с подозрением на деструкцию стенки желчного пузыря или панкреонекроз); компьютерную томографию (для оценки состояния печени и поджелудочной железы при наличии по данным УЗИ признаков патологического процесса в этих органах); диагностическую эндоскопическую ретроградную холангиопанкреатикографию (ЭРХПГ), дополненную при необходимости лечебными вмешательствами. Особое значение в предоперационном обследовании больных придавали выполнению динамической гепатобилиосцинтиграфии с фармакологической пробой, которая позволяла дифференцировать функциональные и органические изменения сфинктерного аппарата большого сосочка двенадцатиперстной кишки (БСДК) и тем самым уточнять показания к проведению лечебной ЭРХПГ [7].
Желчеистечение в раннем послеоперационном периоде имело место у 47(0,97%) больных. В табл. 1
представлена частота развития желчеистечения после различных видов операции.
В 13 наблюдениях наружное желчеистечение прекратилось самостоятельно на 2-4-е сутки после операции. У остальных 34 больных желчеистечение было длительным, что потребовало применения специальных методов диагностики и лечения.
В 41(87,2%) из 47 наблюдений отмечено наружное желчеистечение из дренажа брюшной полости (33 больных) или дренажа ОЖП (8). У 6 (12,8%) пациентов оно было внутренним и диагностировалось при ультразвуковом исследовании (табл. 2).
Наиболее часто в послеоперационном периоде отмечалось наружное желчеистечение по дренажу брюшной полости (p≤0,01), при этом его частота не зависела от вида холецистэктомии.
Источник желчеистечения устанавливали на основании данных, полученных при контрастировании желчных протоков путем выполнения ЭРХПГ или холангиографии через дренаж ОЖП. Диагностическая эффективность других методов была высокой.
У 17 из 34 больных желчь за пределы протоковой системы поступала из несостоятельной культи пузырного протока, значительно реже — из поврежденного магистрального (у 2) или аберрантного (у 3) желчного протока (табл. 3).
Если диагностика несостоятельности культи пузырного протока обычно не вызывает затруднений, то обнаружение при ЭРХПГ поврежденных аберрантных желчных протоков представляет большие трудности и основывается на выявлении поступления контрастного вещества за пределы добавочного протока из правой доли печени. При этом желчь в брюшную полость поступает не постоянно, а порционно при достижении определенного уровня давления в протоках. Выделение желчи из ложа желчного пузыря вследствие повреждения ходов Лушки диагностировать при ЭРХПГ не удается, заключение о данном виде желчеистечения устанавливали методом исключения, а также путем выполнения контрольной видеолапароскопии с осмотром зоны удаленного желчного пузыря. При ятрогенном повреждении магистрального желчного протока во время ЭРХПГ выявлялся выход контрастного вещества за пределы билиарных протоков. Если дефект стенки имел небольшие размеры и был краевым, то выявить поступление контрастного вещества в брюшную полость очень сложно. В ряде наблюдений в контрастное вещество добавляли раствор метиленового синего и наблюдали окрашивание желчи, выделяемой по страховочному дренажу.
У 25 из 34 больных причины желчеистечения были связаны с наличием патологических изменений желчных протоков, не установленных до или во время оперативного вмешательства. У 7 из 34 пациентов с послеоперационным желчеистечением при выполнении ЭРХПГ патологические изменения желчных протоков были исключены. У 4 из этих больных несостоятельность культи пузырного протока была обусловлена плохим наложением клипс вследствие анатомических особенностей пузырного протока или затруднениями, возникшими при его выделении, у 3 больных имело место повреждение аберрантного желчного протока. В табл. 4
представлены причины, приведшие к желчеистечению в раннем послеоперационном периоде.
В большинстве наблюдений желчеистечение вследствие несостоятельности культи пузырного протока было обусловлено наличием конкрементов ОЖП, стенозом БСДК или сочетанием данных патологических состояний. В 12 из 25 наблюдений с выявленными при ЭРХПГ патологическими изменениями внепеченочных желчных протоков желчеистечение было обусловлено неправильной трактовкой или недооценкой имевшихся лабораторных или ультразвуковых данных до операции. У остальных 13 больных по данным дооперационного обследования заболеваний билиарных протоков не выявлено.
Из 4856 оперированных больных развитие синдрома механической желтухи в послеоперационном периоде отмечено у 88 (1,8%), у большинства из них на 2-5-е сутки после хирургического вмешательства.
Диагностика нарушения проходимости желчных протоков, как правило, не представляет больших трудностей. Наличие жалоб и соответствующих клинических проявлений позволяет в большинстве наблюдений заподозрить неадекватность санации желчных протоков при холецистэктомии. Показатели клинического анализа крови не являются определяющими в диагностике синдрома механической желтухи. Изменения биохимических показателей крови имели более определяющий характер. Повышение уровня билирубина за счет связанной его фракции позволяет подтвердить диагноз механической желтухи, а если при этом имеет место повышение уровня α-амилазы крови, то это может свидетельствовать о наличии стеноза БСДК или об острой окклюзии конкрементом ампулы БСДК.
Ультразвуковое исследование брюшной полости для оценки состояния желчных протоков в раннем послеоперационном периоде является одной из обязательных составляющих диагностического алгоритма при подозрении на билиарные осложнения. Его выполняли всем больным в сроки от 2 до 4 сут с момента хирургического вмешательства. У 12 (13,6%) больных ультразвуковая картина состояния желчных протоков была вариантом нормы. В 32 (36,4%) наблюдениях диагностировано расширение ОЖП (более 9 мм) и долевых желчных протоков (более 4 мм), в 26 (29,5%) наблюдениях, помимо дилатации протоков, выявлены конкременты ОЖП. У 18 (20,5%) пациентов ОЖП выявить не удалось, что было обусловлено повышенной пневматизацией кишечника или выраженным ожирением.
Немаловажное значение в диагностике ранних билиарных осложнений в послеоперационном периоде имеет выполнение гастродуоденоскопии с осмотром БСДК. Исследование позволяет своевременно обнаружить острую окклюзию ампулы БСДК или терминального отдела ОЖП конкрементом, который в наших наблюдениях был отмечен у 7(8,0%) из 88 пациентов.
ЭРПХГ являлась основным методом диагностики причин механической желтухи у больных в ранние сроки после различных вариантов холецистэктомии. Это исследование было выполнено всем 88 больным с синдромом механической желтухи (табл. 5).
ЭРХПГ при наличии синдрома механической желтухи позволила во всех наблюдениях установить ее причину и выполнить вмешательства, направленные на ее устранение. В 2 наблюдениях на 2-е сутки после ЛХЭ диагностировано полное пересечение ОЖП, больным в экстренном порядке были выполнены реконструктивные операции. У 2 больных выявлены изменения устья БСДК, которые расценены как признаки самостоятельной миграции конкремента в двенадцатиперстную кишку, других конкрементов в просвете ОЖП не было.
Всем больным с длительным желчеистечением и синдромом механической желтухи, развившимся в ранние сроки после выполнения различных вариантов холецистэктомии, проводились эндоскопические транспапиллярные вмешательства, направленные на прекращение желчеистечения и восстановление оттока желчи в двенадцатиперстную кишку.
Патогенетически обоснованным методом лечения раннего послеоперационного желчеистечения является декомпрессия билиарных протоков. Это обусловлено тем, что пропускной способности терминального отдела ОЖП даже при ненарушенной функции сфинктерного аппарата БСДК бывает недостаточно для создания необходимого градиента давления между желчными протоками и двенадцатиперстной кишкой. Наличие стенотических изменений БСДК или холедохолитиаза в еще большей степени затрудняет отток желчи, отмечается быстрое нарастание внутрипротокового давления, что при определенных ситуациях приводит к негерметичности культи пузырного протока и поступлению желчи в брюшную полость или развитию синдрома механической желтухи.
Для декомпрессии билиарных протоков и создания тем самым оптимальных условий для оттока желчи в двенадцатиперстную кишку, а не через поврежденный желчный проток или несостоятельную культю пузырного протока в брюшную полость в большинстве наблюдений было достаточно выполнить эндоскопическую папиллосфинктеротомию (ЭПСТ). Однако у ряда больных, несмотря на ее проведение, желчеистечение продолжалось, что было обусловлено не только большим отверстием, через которое сбрасывалась желчь, но и невозможностью выполнения адекватного папиллотомического разреза. В подобных ситуациях мы считали целесообразным осуществлять билиодуоденальное стентирование.
Диаметр стента обычно составлял 9-11 Fr с лепестковыми фиксаторами. Длительность нахождения стента в желчном протоке при желчеистечении зависит от размера дефекта, через который осуществляется сброс желчи за пределы протоковой системы, и в случае несостоятельности культи в среднем составляет 5-7 дней. Стентирование при желчеистечении из хода Лушки или при краевом повреждении магистрального желчного протока может быть более длительным (7-14 дней). С целью декомпрессии желчных протоков возможно использование назобилиарного дренирования, однако по сравнению с билиодуоденальным стентированием данный метод проигрывает из-за ненадежной фиксации дренажа в протоке.
Из 122 пациентов с желчеистечением и синдромом механической желтухи 115 выполнены эндоскопические вмешательства (табл. 6).
Диагностическая ЭРХПГ осуществлена 7 больным, причем в 1 наблюдении при наличии показаний к выполнению ЭПСТ произвести данное вмешательство не удалось по техническим причинам (у больного после резекции желудка). ЭПСТ «в чистом виде» выполнена 34 больным, в том числе 23 с синдромом механической желтухи по поводу стеноза БСДК и терминального отдела ОЖП, 11 с желчеистечением и при отсутствии патологических изменений внепеченочных желчных протоков с целью декомпрессии билиарной системы. В 98 (85,2%) наблюдениях эндоскопическое вмешательство осуществлено за один этап, в 14 (12,2%) — за два и в 3 (2,6%) — за три этапа. В 4 из 5 наблюдений билиодуоденальное стентирование произведено по поводу длительного желчеистечения в ранние сроки после холецистэктомии.
После ЭРХПГ и эндоскопических вмешательств осложнения возникли у 4 (3,3%) больных. В одном наблюдении отмечено кровотечение из зоны разреза, которое остановлено после проведения местного эндоскопического гемостаза. У 3 (2,5%) пациентов развились явления острого отечного панкреатита, купированные консервативными мероприятиями в течение 2-4 сут.
Таким образом, анализ показал, что основными причинами развития билиарных осложнений раннего послеоперационного периода после различных вариантов холецистэктомии являлись недиагностированные до операции патологические изменения внепеченочных желчных протоков или неправильная интерпретация лабораторных и инструментальных данных. Значительно реже их причинами послужили интраоперационные ситуации, приведшие к ятрогенным повреждениям желчных протоков и ненадежному клипированию пузырного протока. Основным методом диагностики этих осложнений являлась ЭРПХГ, на основании данных которой определялась тактика лечения и выполнялись эндобилиарные вмешательства.
Источник