Вирусу оспы рнк содержащие вирусы
Содержание статьи
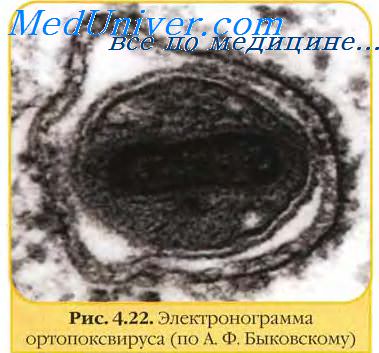
еном вирусов оспы. Антигены вирусов оспы.
Геном вирусов оспы. Антигены вирусов оспы.Геном вирусов оспы представлен одной линейной молекулой двуцепочечной ДНК с ковалентно замкнутыми концами размером 130 тпн (парапоксвирусы) — 280 тпн (авипоксвирусы). На обоих концах генома имеются идентичные, но противоположно ориентированные тандемы повторяющихся нуклеотидных последовательностей. Геномы вирусов оспы способны кодировать около 200 белков, из которых не менее 100 входят в структуру вириона. Однако функциональные особенности определены лишь у небольшого количества вирусных белков. Наиболее важными из них являются ферменты, участвующие в синтезе вирусных нуклеиновых кислот и структурных компонентов вирионов. Например, синтез ДНК-полимеразы, ДНК-лигазы, РНК-полимеразы, энзимов, связанных с кэппированием и полиаденилированием мРНК и тимидинкиназы. Инфекционные вирусные частицы содержат системы транскрипции, которые могут выполнять in vitro синтез РНК, а также способны полиаденилировать, кэппировать и метилировать. В вирусных частицах содержится большое количество кодируемых вирусом энзимов и других биологически активных факторов. Некоторые гены вирусов оспы кодируют белки, которые секретируются инфицированными клетками и вызывают ответ организма на инфекцию, в том числе и формирование иммунитета. К таким вирокинам относятся гомологичный эпидермальный фактор роста, белок, снижающий активность комплемента, вирокины, обеспечивающие устойчивость к интерферону, и другие супрессоры иммунного ответа, подавляющие действие некоторых цитокинов организма хозяина. Вирусы оспы обычно характеризуются узким спектром хозяев. Они передаются чаще респираторным путем и реже через поврежденную кожу. Вирусы оспы овец, свиней, птиц и миксоматоза передаются также через укус членистоногими. Вирусы оспы устойчивы в окружающей среде и могут сохраняться годами в высохших струпьях кожи или других вируссодержащих материалах.
Большинство вирусов оспы хорошо размножаются в культуре клеток. Исключение составляют парапоксвирусы, вирус оспы свиней и вирус контагиозного моллюска. Однако они, так же как и ортопоксвирусы, легко образуют оспины на хориоал-лантоисной оболочке куриных эмбрионов. Вирусы оспы размножаются в цитоплазме, и, в отличие от других ДНК-вирусов, их размножение происходит независимо от ядра клетки, благодаря кодированию всех ферментов, необходимых для транскрипции и репликации вирусного генома. Некоторые из этих функций выполняются вирионами как таковыми. После слияния оболочки вириона с плазматической мембраной клетки или после эндоцитоза вирусная сердцевина освобождается в цитоплазму. Транскрипция вирусного генома характеризуется каскадностью, когда каждый временной класс генов («ранние», «промежуточные» и «поздние» гены) требует наличия специфических транскрипционных факторов, которые создаются предшествующим временным классом генов. Факторы, обеспечивающие транскрипцию промежуточных генов, кодируются ранними генами, тогда как факторы транскрипции поздних генов кодируются промежуточными генами. Транскрипция начинается вирионной транскриптазой и другими факторами, находящимися в сердцевине вириона, которые способны образовывать мРНК спустя минуты после инфицирования. Белки, образующиеся в результате трансляции этих мРНК, включая ДНК-полимеразу, тимидинкиназу и несколько других ферментов, необходимы для репликации вирусной ДНК. Репликация ДНК ВО связана с синтезом конкатемерных промежуточных структур, которые затем разрезаются с образованием единиц геномной длины. Детали этого процесса недостаточно изучены. С началом репликации ДНК происходит резкий сдвиг в генной экспрессии. Транскрипция «промежуточных» и «поздних» генов контролируется специфическими вирусными белками. Некоторые продукты транскрипции ранних генов образуются на поздней стадии инфекции, упаковываются в вири-оны и используются в следующем круге инфекции. Так как в состав вирусов оспы входит большое количество белков, не является неожиданным, что сборка вирионов есть комплексный процесс, который длится несколько часов и все еще целиком не выяснен. Образование вириона связано с вхождением ДНК внутрь незрелой сердцевинной структуры, которое затем завершается включением наружных покрывающих слоев. Репликация и сборка вирионов происходят в разных местах цитоплазмы в так называемых виропластах или вирусных фабриках. Вирионы выходят из клетки почкованием (оболочечные вирионы), или путем экзоцитоза, или при лизисе клеток (вирионы без оболочки). Большинство вирионов освобождаются при цитолизе и не имеют оболочки. Вирионы с оболочкой и без нее обладают инфекционностью, но первые, вероятно, играют более значительную роль в возникновении и распространении заболевания, а также в создании иммунитета. В очищенном вирусе осповакцины (ВОВ) выявлены белки с молекулярной массой 10-250 кД. Многие из них сосредоточены в сердцевине вириона. Два структурных гликопротеина располагаются между оболочкой и сердцевиной. В оболочке ВОВ содержится около 10 белков, из которых иммунологически наиболее активны крупномолекулярные белки с молекулярной массой 58-32 кД (VP4c, VP6a, VP6b и VP7a). Белок 32 кД определяет круг хозяев и важен для репликации вируса. В составе очищенного вируса оспы птиц обнаружено 29 полипептидов с молекулярной массой 14-138 кД. Наивысшей антигенной и иммуногенной активностью обладают полипептиды с молекулярной массой 35 и 37 кД. За индукцию вируснейтрализующих антител ВО ответственны антигены, расположенные на поверхности наружной оболочки вириона, и прежде всего белок 58 кД (VP4c), являющийся основным структурным компонентом трубочек (ворсинок). Антисыворотка к этому белку нейтрализовала инфекционность вируса и предотвращала образование синцития в культуре клеток. Этот белок ответственен за выработку иммунитета. Внеклеточные вирионы покрыты дополнительной наружной оболочкой, отсутствующей у внутриклеточных вирионов. Она играет важную роль в индукции синтеза ВН-антител. Инфекционность ВОВ и ВО крупного рогатого скота, имеющих наружную оболочку, нейтрализовалась антисывороткой к имеющему эту оболочку ВОВ, но не нейтрализовалась антисывороткой к ВОВ, лишенному наружной оболочки. За гемагглютинирующую активность ортопоксвирусов ответственны полипептид 85 кД и гликопротеид 41 кД. Во внеклеточном оболочечном ВОВ гемагглютинирующие свойства связаны с полипептидом 85 кД. Внутриклеточные вирионы (без дополнительной оболочки) практически не содержали этого полипептида. Неструктурный гемагглютинин формируется на цитоплазматических мембранах. С его образованием инфицированные клетки приобретают способность адсорбировать эритроциты. Вирусспецифические белки с молекулярной массой 32 и 37 кД, экспрессируемые на поверхности клеток, инфицированных ВОВ, делают их мишенями для специфических цитотоксических Т-лимфоцитов. МАТ-реактивные против каждого из пяти (54; 34; 32; 29 и 17-25 кД) белков наружного слоя поверхности вируса осповакцины нейтрализовали его инфекционность. В структуре полипептида 54 кД обнаружено два нейтрализующих эпитопа(Аи В). Анализ антигенных детерминант поверхностных полипептидов, проведенный с помощью МАТ, выявил в составе ортопоксвирусов, наряду с видоспецифическими, группоспецифические эпитопы. Связывание ВОВ с нейтрализующими МАТ не препятствовало его прикреплению к клеткам-мишеням, но блокировало депротеинизацию вирионов. — Также рекомендуем «Оспа овец. Оспа птиц. Особенности оспы овец и птиц.» Оглавление темы «Частная вирусология.»: 1. ДНК-вакцины. Свойства и методы получения днк-вакцин. 2. Синтетические пептидные вакцины. Свойства синтетических пептидных вакцин. 3. Вирусы оспы. Виды вирусов оспы. Строение вирусов оспы. 4. Геном вирусов оспы. Антигены вирусов оспы. 5. Оспа овец. Оспа птиц. Особенности оспы овец и птиц. 6. Контагиозный пустулёзный дерматит. Эктима. Миксоматоз. 7. Асфаровирусы. Признаки и свойства асфаровирусов. 8. Иридовирусы. Герпесвирусы. Семейство герпесвирусов. 9. Эпидемиология герпесвирусов. Строение герпесвирусов. 10. Антигены вируса герпеса. Протеины герпесвирусов. |
Источник
l˜5´upè,³ŒnÕÛGн½ìk§ô’ëÚè™þ® )îídJÆ.zÃV‡§¿é-YÇÑöŒ!öLJã’d&°Z]Šñ,7öº-•nꈧ¤‹©ººD’|¼ _P¼œ2S‡Áú*E6z’+e‡aÉåjE›=©ª&žkŽY’¶Ìê¾ú áêY/bšYÅ*JêÑ)q›yyS&¤éêkfË»Çvog⢧ ®}bõ’#šýØ1€]ƒŒÖ·6ë¢%LoÝb²X…-S»Ã5^»5¸(·xóY õ’ë(TÇ͆dbz×Aao5û6*»?Ÿêk8O¬¢HuJ4И’ãudb&ßµFöÖÓ£1o/J•·£Q+¯E/ÝЛN2mÊêD´•ø©ÔXoaE _çömõ½¾êêê9D«re˜¬º`•l!ò•ÛÔW2Å)š5¾’6nªü¡6¥ep-%#r.…ÜF Çä|n-j E[ßžÑ2èš %ë2 ÚfB*-4£eÐ7’3åi>è› $3e]>øÖ·†è)ër>Ðb89-ì:6 rÊG|€]¡Ç1£e€].$ás>`-3ã;Ý3ZØå¾_>¥d ]æžsû -)»Ý²__¦Ë@Lv°Å ¹Lh30£e€ÆÃäŒ-r21 ®«0Ý2KsUÎÂw>æÆJã½57ÖHÿu-©±œ¹»c1º’tá×âÅ´mØX@U}üú»áþmò‹ÒY•ƒÝ¼åÊîû¿¶îýÔ÷aÜ7jßvk$ÈÏejþ1£e@~àÊ9‰ç¹±ˆç¹±ˆç©±ÏscÏscÏñCß쬿S~ºó-Iý²ÖûȇIØ endstream endobj 14 0 obj > endobj 15 0 obj > endobj 16 0 obj > endobj 17 0 obj [ 18 0 R] endobj 18 0 obj > endobj 19 0 obj > endobj 20 0 obj > endobj 21 0 obj >/ProcSet[/PDF/Text/ImageB/ImageC/ImageI] >>/Annots[ 23 0 R 25 0 R 29 0 R 33 0 R 36 0 R 41 0 R 44 0 R 45 0 R 52 0 R 53 0 R] /Box[ 0 0 595.32 841.92] /Contents 22 0 R/Group>/Tabs/S/StructParents 2>> endobj 22 0 obj > stream xœšKo7Çïôö˜Å×ð$Ù.Z @’ èÁÈÁp4‡:iàK¿}ùØ] %.wª¬cga™úÏpøãìW›Ý÷×/ŸŸ^»››Íîõõñé¯ç?»‡Íñë·›ã¿ßž7ï?yy|ýòõe»íö·‡n¯6÷ªóÌ›îøi½ÿD§%3õ†yÙÿ^¯x÷9þ÷Ëzõð¦ûécwüm½ºoþg½m™ua°fºÆu’Ù}^¯þø¹{!Š®ÖÇÑ£ý‡7 Yýp&Hæd©Ù•šá»»{wèºÍûÂw‡_o;^DJtBGC8TS¶³N0³ð -z¿ÕábÜö W¸?÷á÷]øá[_Úå?»M™.p¿=ù»ÊŠQ¥ÂKª0ZÌæbÍcô܇ Ï 0e¦E~ÿöø2êÈ»ºâZFG{§`ÜÁ0ÃÌMιŠè¯»-ä-¥qTŠŠàè¶oåM‡,.Ó»FíÛH×}¶‡»‘ç±U• ïx ETŠrÁœGC»·Æå™ÒÔØ°þÞáðŽ©’ô¹B[·@VãÞVzrÅjk»ÇJ1-Ñ®4úm|Û3©û×âz¬O|Fd4d#±o?Ž]ð!Aæ{5ÁÖ3å’Òž§ßšÁňÆ!6e[ BD,2G¢!'(l»I’,0îXó»0u_ÂÚ ®Ï½IË!«§ÌžöFºåÆ»>z+‹ô-ÔÂùÛ¤ÚšÜi¬cZà±dpîÓmÛ¿-)˜€E¤@IÅÂõb.éSÂÊ1Uj3n’¼àMd›èÂÓ¹äˆ;)ܴʼn]u˜IÎv¬9 ±{‹JÛK¸¼1 U«RäÒ4«Ú0áðØÒ>X¶´-öáâa)íx»`ZjŠCé#w8D3Y_‰3KˆÙ»××Èíï!æå»ùõ©å¯Q.8 sã Íä:ÌCæΈïû,±ÒÙºœ©ihsæ/dKfñÐ%À™¿l`Ú.»¥aÎÌHµó1ŽÒÛ1)ãG´M³W¬5‹=ªmóU^‰-£‰ùà Ha¬lp¡w Obã»RÒÄ:Çkf¹>wêT¸l…@e×ØÙÂVHèìSŸŸvÍýÐä_‡-˜Ëž0Zc;TFKu2FÚ·ãq«˜
«šs’Ë xgH⩼ԘϫͰËÏýRVìÏ ÍóH_¡¡£Óg¢ÅÙ,xÃTpP§ävµ‡5> Îbè‡ì†ñì†s¬w¢€’š{hÖ,’êZ$)h®fx‹Â` ¸éªºðN˜»í°m_QçǺÂêMÛfžUA»&ñˆ¢¿ÚxHym®,÷-Š@Z¹9Gˆ6ÓÒî›±‡G1ññ½MÞÛmS-ͪ©Ä»Ù’Ç~N¾þê[ð®®5þ»»G°¸ÔMlêPÙ&•»eü#Ï…}VŸfroÌf»¢ÖdÞrïÓž êž%Óÿ»ðK+šÙ 6ÀnBö†löåõ[´ ßeTû˜35Àߌ£mõ ÷¶Ún3‡Š@øöP xÛex; e^¢ÊÞÎAÊ…ÙÁ€dÕw4-»>QDENl[õáxHô´³’ÂÂ1Ž·»oÕrdÅÉ(Î~el7÷’5g$ߌd¸ Ӽʻð‹ÛL¿ÐÑà¸kˆ’Ó’.¼¶‰ ÇDdÄ$ƒ#ÅJÎÅÄÔÄ’Ê°b’Œù ¥-cP»hS¼!å¬_íï7¥, 4UãF2í¯ÑØ`îgM9KZƒÕCP,{›ÏñŸkɸ=z;˜k{÷Né¦x»÷lK;ô cŽœ»n{{‘ÂÄÞM½ºèÝDÕÚ,Ú^²‹’LeŽ×ÆKÊO€Á#Iƒ»Lòú q¥£hj|@@¥AàotHJì›}°ßª;EH-¶s=kCVéG?åï-åK`~ÿŸÂ8LÜJ,u»è:-¨aè¬Zþ«}íUcÐ7u9’ðÄ»Ñ*U½ëàòTì‰$ƻǞ²)Ë-2‡ð›l•FàGJ™‡}¼šbBn%´|’¼š®Ñ©j‹ë]Óêl§[E-ü-äsɧ%!æë-õ朻âxÓ‡ÞŽu´íª»ã]*Ý’61{Ê(µ†xô›-;†ÚMwK@.NͻӬ7Ëy> *Œ&¤SZ’£Ÿ ‘d1b¹!…иMj*»D9,Ù†´Âƒ-;Z^ ÚóŸ’r»¯X$ï$>>¤D·ƒìó™Af/# e¶§Qä ÝEæ*ÃýŸbº¢¥»gŠ®y)¡HI?ƒÖ(U!gU-pö8½cSÔ²cÅ$g@ôº¦$_È`¢SdënSyöpý|’L-á²J’ò‹ó¥ãoQ «®»Èµa5&Z-®cÜppNCâaäd±ÃÄ5yÃ7Vüæ’.…B¥‰vðÆ©Á¹ãHÅZ¢E{ÐÂa§×dGawïå@%Ù$BpàTƒóœ¶Ó•CVÖ¡®†±[gE#t°´Há3™]I’Í# :fAZ :²Z)’@K%ÎÒVù(p$ p%5a¿%»5Ъº0ƒ?Íø§×†C1³I× XŠå¢ä̱®nÏ`λ!ïaú¥«š•¥_Ò’…j¸ê£|u¥/ªYwëµàÊL71ÆáÞÓ¦ë›ñb’bø=˜d-«?+¥xËyY.åÆ»)qÍ hsZq- ±ö&PÄ(}Dßÿ5ÉQÁ¯HCeîô¿£
)’åÒØZ£ ÐÄf0 Üû¹ö´ÔØ4ALJëZÑŽ0I‹{-3sd@Ä,sˆ»ùr~a»¸XxüpcTÊ-á†Ú÷PøëpÃ¥(:îà†c}ýÎО£ˆ‹´ºÆ-ú q+ê1 >QÙŒ ùÐÀˆ3ÞáÓ»kÝ»@¡»ˆöÁù™M‡À#B+d¡1EÐìú©×Cÿ,yNd{?}ž9h¾•WϤñ6këDP?ï ›t:»²54Â@’Dl,-ã‹AÕ3…ù{å¶ZÌtàGqòÃÍú¨¡eIS‡Ìl+†ƒô$Ø÷7;©e#E9ëÅ,Œö`Õàî£X’±Øw‹µé=í7ûƒ«@4{Ï’K§c)/]8µ=qM]Õ‡ÂiŸR:C1’»ÍÚ->Ç¡Ü¡.ñðF7;]Ô%FÈÁ r|Pú,»«BYÏxýXµdjq»_5h»»$ä ÊìäŠ-ÚnŒ3Ü«PPüEozÀ¢n.$°w£ýK[ˆ-]®Úgå½c)nÊÕÐ%á_«êÂ]$’½Tª%E¸À.~¤žÓ¿m1Zlœ†*ÅžµïDïÁ[ÙíãrΧŒwC¥Bé§C‡È›¡G‹)!WAîˆL¬‰÷NwÛ C]R œãÃ~µg:Ô44£.&ȃ»Ìo0p{w@ÖfizV»Ü ¦nV¸*»ðˆÁ»(Í!P®Ù>š!Ü»‘ŠaojÒ}g!¾Ôî¦8ô¥^.㶻¹9@ÊA¯I{ú·YL(aÌ Éú{ÕÒ»ýëÂgˆ¸¹t#ª‰¥’U=iUÜ _ ¿hÉBø]Kƒ6·j!TÒñ YÐÝýFo ÷zÓJÇ›b=á ‹qóU÷žÇ¾šøUBm:{±Ÿô[¿fs;í1Í¥‰ðY5™®ŽÄi4‡,kÁ»Ýd1QƒëÕ&Í$ÁaoÛ½×!œúL’«|¨ùµÛ ܉BR25’*»´âl¨è8d˜ó»,-œÐbnRªÕlÎF§Ë†58€-UüÊ{må^-¯_{;éèòg®}£€3ß¾ÕV•Bâz»°*¾ÈU›ú•*¹‡ª*.BO|禰w†D&×à’švÁ¼h¬A‹úObP°8º¬’-ÞK‰AÝcD¶½Ø’ÚvPL/gŽ4¤ÌrýšâäqÂÞ‹}°¨{•`MW3äQh±SÔXCc$,¶Î£FÇW{Š˜…ã}SIÃésºï¤=ÚÈ`N0+zoû-KE1é¼4$5Q2Í(d´†Ó4’ÑõrÕûÒ¢&@[ŸâÒPÓªÜÖÖ/XN,˜ÜáÌ»nçÌ`QLs¤›iTÈèpºð·TÛ× Ú!’ØxŸrF aò³ÆM ‘ÍÈê†/Yλ¿øMs¾&ª7ƒLŸE^˜sP_h¾ Ój’_§{«FNjC!n;ÊÆÈPÔP¥SسŠ!mç¬)n,g.Úì7BÝ|àÍ·ÕÝØÅçïqíjþAdÍÈôH’m#t*ч š+c+øU+êŸÐ»PJö_S²ITLx( ñŒHh¤§Ë·ˆã?-K-Õ÷Y½nypÿÐB¿eý8!âûDE__£ˆF )k~J|!Ï8÷Bɧm½÷ð ƒü€Lx»Á¡¢S rÞBƒOðzd¡÷è WÃÃ_ÏùV1)¶ž÷tO¶-ýο£¡×Â=èù AÔh~«çòK«UYNò-WZÙP¥ÐdÛBìj›@AA^{Ï›n Ê‹®ÝÍTpÏH†ôh µc+$æ¬`ÕqŽ;¼D$ÃÍ tÍ2¨ R¢Ê¹7é$’Û ¾£µÑ’ ÚÁn½t¤4B€%^¼üÞØj
úkHR-Ö÷ˆª…Nîíë>³ø`‰7ÓC-‹%2²òÛìX OF+‰çþÉz»Dg÷.T0g艕¸GV9ò!çAc’´#îÖ|öWKPàjøк+ضDö¯]/þ¼-Ìqz3šláÁÛ^£÷JrôGøÁ,dge£^#qÕ´],ã2 Üó©€€%GM p Lƶ9¢Y$7ÃÊÌ˶Âã!‰¿® Î냎ÓG,3ÝhŠWÙrày’µŠÄ’¾úÂX©š†4*×ɇ?Ú§r¯â/üÑøØs±|x$ül _‹kÚðmîû ‘•WCtP@BªuÕEG¾•o’uÃkaM¨ T±V8뚇k+óÚpѸÃ%ºÂX•0ÕŲR%õcyg®8ÍpÑ ûÃIù¤vÝ,³¸ô±þ¦Ó :_·Ðç…lë•TªAM~Ã(¾W£6»®D‰[rh£kuEP õ¥¡)VÃ6é›Çι?»€®©Bb5k¦/˜(3;¹ï’sЬhŠù3†L…Û¤íšÂ ·à™h7’ab‰€4, ‘BH»fGŠW[º9j=ÁLþµFt4æùž}YÔÅ’Ÿ§¤éÍÜèU+0sʆK°kf·].ÉòÈô|Ÿ™»;Ô`áô- 7k5³-pv3´eÞhsÛì&-U±¹KEua°EÜ:ŸêBsÉÌ-‹M]2’ ¶$Â-®»§€*©ñô»µ¯OÙhb¬†¬®DktñÐÁJÊFòpÐàˆ»¼`÷Y2ié9~å@Ìü|õtŠýWiÆUë3 q¿M8㻼xg»S’×áé¼5áÄm-…S4³TáÔI6ÏÇ &å,]¾()¥]é0ù²Ã Ÿ LÐáTú,M6o¶5õšY)ÐÒÏš?)¿¥GRÓ9″¥mëá»Ƿ‡ò(Œ
®!5jf»§.^¨±ÈT-ã‡J€{XÀ{@Ã*ñ ] Šh,Nž+(ÜZ:ÁÓœ È€ìÄ¡IšhËéc!ŽñTˆ†ÂèG?*6Ïí‰ÝÀ)JKÕ|Qį(-¼õJ-ƒ¯îO³Wi-ÅêO+C¤âêcÖ5ûóª(*nµzZé×WvÐÐr0E%ÿCÆôZ¸yo¦Þ³Å˜ýCbøѵâ76ç˜Ü9’F¾Hõ-b {‡hí«°ÙÅ ÝôjHž±I{û¤Š1ÝNÚ»0ñæ¹ç™W*¤›®=¶GL»tŒ5½FAÀþ+%4ÇQYš¤éÃá»tôÀk-*ºèB•7¹G-P½Šµp²ñiŸÙö¸E>Ì»dÃÁož¨ò•¬º-W’ïÇLÌÞÒ#O†ÄQ)3õ»çÃ]Æ’Q2L¿˜’JYŸxN£€ÿÙâëTM(åq»=æAÒ² ¶`S3p’æ¹Ë54ƒêMæ»Õ¬þC5©y$&»Kµ9£ü¶qy·’À+Î]óñ-åÊpà¸yÛžºŠnpPÈÒª1Š»e_xál;›Qß•%å /¬Ô$› ‘§ÿÑ_|º»9a¥(ùŸijâ!áÛ-Ìè]Šü³(Æîy ƒÓ[Í b:åº4k0mÊßì5¢_r. ¬-êÞË[´èR¤cà†b¹Ù»»ÏKäµñÍvå9ÈÔe)Ãf뛢D'[ê’òúQàvÊm¿_ ±Z¼B.jÈ(Çw•ê㻺7=´Åùjæ…ÚN²ˆƒ/»‰w3IÛEH¨â×4[ÕPF¨éMT^5omÈ,gìýfG׺úªgøšÛË;Î/{>xGì6¼»ÚÎ2œâäðÍ8ä[GR)Ò?ç´£Ö…~ï¥vÖ ×É88²U³µ3QÒ›kÖMîå!߶y+®g½wµæ¹hµGo툧j¥Âä€Ï× !UrvÕŠsr;¯-‡ŽÛ°xô-6º¿»¬ïâÓ-V…äD]ëÁ7µÐ,ƒˆ-õ{ü},B3íf»=ÕuG²qPµù $XÑÝåà»6zÖÑýCX¯-6;ë¯gŒ€î׃áq#gŠ¯É·¼À»µ¥šxü‹ÍNçc-E3‡»žFñà5ƒ|m»ßXð(©!g[ñ6¿n,ƒP·$²^ׯ܋_ÈâkŠ»4Ç@û»«$L†:b4×#}{$ vƒb»êŸ(«[£Èüd»_™’œª™ŸlñZ-2!’ò`«ã’XIK·š¿B£7æøÖl»×…§C‰Fùzð5«H´«)S`霅ZK!_T|Âoá&zÖ»R5¥$’># àBi@Í1¼tC>(Ÿ/éAj»‰ÿ7IB endstream endobj 59 0 obj > endobj 60 0 obj [ 61 0 R] endobj 61 0 obj > endobj 62 0 obj > endobj 63 0 obj > endobj 64 0 obj > endobj 65 0 obj > endobj 66 0 obj > endobj 67 0 obj > endobj 68 0 obj > endobj 69 0 obj [ 70 0 R] endobj 70 0 obj > endobj 71 0 obj > endobj 72 0 obj > endobj 73 0 obj > endobj 74 0 obj > endobj 75 0 obj > stream xœÕYKÛ6¾ðÐ1[À4ßÔ0`k½EH€zØæ°ØnÒòÄ^úï;CR)‰íäÒ4é: 5œç÷ÍŒ·‡ï/ß?>½4»ÝöðòòøôÏóßÍÃöþË×wÛû¿>oß#N7÷ï×+ÖPø5’ݧ‰ãÍý§õŠ6ð¿W¯š›wÍýëÕ ^þ¶^)iˆ±pXÙ(BeÃQ¼ùþ¼^ýùKó¹òªÒÝÞŸîïx¥'[ß^#Sqby.³ÉeÂïæôºmšítáëö÷Û†fž’+$^»¹J ZXF´ rw»k ì~#ð3£öŒâg¾ßpü)ýg¹£»öƒ]@¦×8ÆÊìžLÿ‰æ,Ѽb9′»há 267ùíýQC˜Ì67cEÙœ¢»hž½ˆöº½wÅmt‰ nPwð§íÁÕ >š½Úy‡ù»ÆQJ…¤O{»KÜzØ;ïé½çk¼È©#Ú-X5eÎa&·ŠÒ£WC¦=z+™ÿlâ³NcémÁD Lùg»¶øÌ;ÈìJÒð’hd8¬ÚüTôÞ+rÂñcð´áá’ê%»sÇØ.ˆ¯ÌF‰Õ¤‹~œ$#?»ŒÒU™ŒÉÑÊddã;:»C2yw¼+}¶±øèJ¥^›}Ìg̘Í>Î w¹}A-.ú
Источник
НК-вирусы как причина развития рака
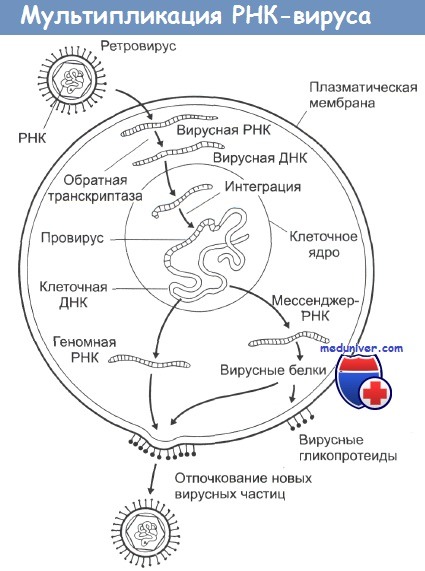
РНК-вирусы как причина развития рака — вирусный канцерогенезОткрытие вирусов, вызывающих злокачественные опухоли у животных, произошло еще на рубеже XIX и XX веков. В 1910 г. Пейтон Рауш обнаружил, что бесклеточный фильтрат из тканей птичьей саркомы может вызывать развитие аналогичной саркомы у цыплят. Примерно в это же время была доказана вирусная природа птичьего миелобластоза. Позднее было обнаружено, что часто проходит весьма значительный латентный период между инфицированием вирусом и развитием рака. Тем не менее вплоть до 1960-х годов не существовало четких доказательств того, что инкорпорация вирусной ДНК в геном клетки является необходимым условием развития злокачественной трансформации, как не было и случаев выделения вирусной ДНК из раковых клеток. В настоящее время выделяют два типа вирусных онкогенов. Оба этих типа онкогенов встраиваются в клеточную ДНК. Вирусы первого типа несут онкогены, которые вызывают быструю злокачественную «трансформацию» клеток в культурах in vitro, а в организме вызывают развитие опухолей. При втором типе вирус действует медленнее и для развития опухоли требуется значительное время. Вирусы второго типа не вызывают злокачественной трансформации клеток в культурах in vitro. РНК-содержащие вирусы вызывают развитие целого ряда различных опухолей у животных, при этом наиболее распространена индукция этими вирусами лимфом, лейкемий и сарком. Типичная структура таких вирусов — это две идентичные цепочки молекул РНК в сочетании с ферментом обратная транскриптаза, одетых в гликопротеиновую оболочку. При инфицировании вирусом его обратная транскриптаза заставляет клетки синтезировать ДНК, комплементарную вирусной РНК. Эта ДНК затем встраивается в клеточные хромосомы, и на ее основе клетка уже сама начинает синтез новых вирусных белков, вирусных обратных транскриптаз и элементов гликопротеиновой оболочки. Из-за механизма их действия этот тип вирусов получил название ретровирусы. Все они имеют весьма схожий внешний вид на электронных микрофотографиях и являются самыми маленькими из известных вирусов. Некоторые из ретровирусов (например, вирусы птичьего лейкоза, кошачьей и мышиной лейкемии) содержат в себе только три гена и обладают очень длительным инкубационным периодом с момента заражения до возникновения опухоли. Другие вирусы (например, вирус саркомы Рауса (ВСР)) вызывают очень быструю злокачественную трансформацию и могут быть выделены из культуры опухолевых клеток. Показано, что вирус ВСР содержит особый ген (v-src), способный вызывать трансформацию фибробластов in vitro. Этот ген кодирует наработку протеинкиназы, которая фосфорилирует тирозин. К сожалению, действие этой протеинкиназы запускает целый каскад различных метаболических процессов, и очень сложно оценить, какой именно из них ведет к злокачественной трансформации.
В настоящее время известно, что и нормальные, и злокачественные клетки содержат в своем генотипе участки ДНК, сходные или идентичные ряду последовательностей онкогенных РНК-содержащих вирусов. Такие участки получили название клеточных прото-онкогенов (чтобы отличать их от вирусных онкогенов). Постулируется, что активация этих участков, возникающая в результате канцерогенного воздействия, запускает целую цепочку событий, ведущую в итоге к злокачественной трансформации клетки. Считается также, что ретровирусы инкорпорировали эти клеточные участки в свой геном в процессе эволюции. В настоящее время мы лучше понимаем механизмы действия продуктов вирусной активации. Примером такого продукта является протеинкиназа, активируемая геном sre, а также целый ряд других вирус-индуцированных канцерогенов. Это и рецепторы к эпидермальному фактору роста, продуцируемые геном v-erb, и тромбоцитарный фактор роста (ТФР), кодируемый фрагментами гена v-sis, и целый ряд связывающихся с ядром клетки белков, продукцию которых вызывает вирус птичьей лейкемии. Вирусные онкогенные молекулы в большинстве случаев структурно отличаются от своих аналогов клеточного происхождения; кроме того, в них отсутствуют интроны. Например, белок, кодируемый геном v-erb, гомологичен клеточному рецептору к эпидермальному фактору роста (ЭФР), но в нем отсутствует часть экстраклеточного домена, включая ЭФК-специфичный сайт. Так как в продуцируемой вирусом молекуле отсутствует плазматический участок, ответственный за автофосфорилирование, такой вирусный рецептор все время находится во «включенном» состоянии. Как нормальные, так и раковые клетки содержат в себе участки последовательностей ДНК, гомологичные РНК онкогенных вирусов. Если происходит экспрессия или активация под действием канцерогенов этих клеточных онкогенов, это ведет к злокачественной трансформации клеток.
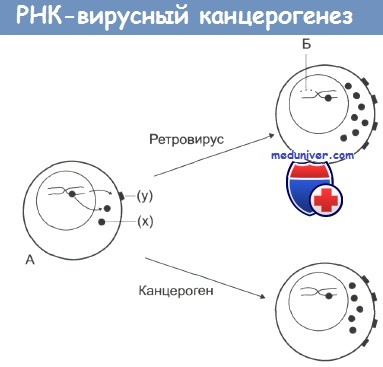
На стадии А нормальная клетка, которая характеризуется низкой протоонкогенной активностью, продуцирует фактор роста (х) или белки дифференцировки или рецепторы (у). Канцерогены повышают активность протоонкогенов, что дает начало неопластической трансформации. По другому механизму: при заражении ретровирусом происходит внедрение в ДНК клетки вирусных промоторов или онкогенов (Б), что также ведет к увеличению онкогенной активности и последующей злокачественной трансформации. Вирус может активировать процессинг в клетках путем внедрения в их ДНК специальных регуляторных последовательностей — промоторов считывания белка, нарушая таким образом нормальные процессы транскрипции. Запускаемый таким образом механизм внедренного мутагенеза может вовлекать в себя целый комплекс различных процессов. Примером может служить внедрение в ДНК клетки вирусной после довательности «многочисленных терминальных повторений» (МТП). При внедрении в клеточную ДНК данная последовательность инициирует транскрипцию в обоих направлениях цепочки ДНК, позволяя транскрибировать одновременно как клеточные, так и вирусные гены. Такой механизм действия характерен для вируса клеточного лейкоза, когда вирусная ДНК интегрируется в клеточную сразу вслед за участком с-тус, вызывая его активацию. Первым ретровирусом, для которого была однозначно доказана связь со злокачественными новообразованиями, был вирус Т-клеточной лейкемии человека (ВТКЛ-1), выделенный из клеток хронической кожной Т-лимфомы. Этот вирус довольно широко распространен, может передаваться половым путем, через кровь, особенно в среде наркоманов, и от беременной женщины к плоду. Первоначально эндемический ареал циркуляции данного вируса был в основном представлен тропическими странами, однако в настоящее время в США серопозитивная реакция на вирус обнаруживается у каждого из 4000 человек населения. Кроме Т-клеточной лейкемии вирус вызывает тропический спастический паралич. После 20 лет наблюдения за серопозитивными пациентами оценено, что риск развития последнего заболевания составляет около 5%. Один из вирусных генов, а именно tax-ген, вызывает увеличение продукции клеточного интерлейкина-2 (ИЛ-2) и его рецепторов, что является основным фактором, стимулирующим деление Т-клеток. Ретровирусы могут вызывать опухолевые заболевания не напрямую, а опосредованно, как это было показано для вируса иммунодефицита человека (ВИЧ-1), вызывающего развитие СПИДа. Случаи развития рака у ВИЧ-инфицированных рассмотрены в одном из обзоров. Отмечается, что у ВИЧ-инфицированных наиболее часто развиваются три типа опухолей: мгновенная или высокозлокачественная В-клеточная лимфома; саркома Капоши (СК, которую вызывает другой вирус — герпесвирус ГСК, или герпесвирус 8); карцинома шейки матки. До разработки эффективных методов терапии ВИЧ-инфицированных более 40% из них заболевали тем или иным видом рака. Тем не менее связь этого вируса с развитием онкологических заболеваний скорее всего косвенная и опосредована развитием общей хронической иммунодепрессии организма, которая и позволяет другим канцерогенным вирусам вызывать рак. В-клеточные лимфомы также характеризуются довольно сложным патогенезом. Хотя В-клетки не поражаются вирусом ВИЧ-1, они могут быть мишенью для других типов вирусов, например для вируса Эпштейна-Барра (ВЭБ). Рак шейки матки у женщин также развивается на основе вторичной вирусной инфекции — вируса папилломы человека (ВПЧ), на фоне общей иммунодепрессии, вызванной ВИЧ-1. По причине общего снижения иммунных реакций организма все эти опухоли развиваются особенно быстро и агрессивно. Показано, что РНК-содержащий вирус гепатита С значительно увеличивает риск заболевания гепатоклеточной карциномой. У больных, инфицированных этим вирусом, риск развития раковой опухоли возрастает в 100 раз, но механизмы его канцерогенного действия в настоящее время почти не изучены. Если больной заражен еще и вирусом гепатита В, риск развития рака печени возрастает многократно. На земном шаре одним или обоими из этих вирусов заражено около миллиарда человек. Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021 — Также рекомендуем «ДНК-вирусы как причина развития рака — вирусный канцерогенез» Оглавление темы «Канцерогенез»:
|
Источник
 Онкогенная и злокачественная трансформация.
Онкогенная и злокачественная трансформация.