Уровень блока при механической желтухе
Содержание статьи
Лечебно-диагностическая тактика при механической желтухе — Практическая медицина — Практическая медицина. Журнал для практикующих врачей и специалистов
В последнее время во всем мире отмечается значительный рост заболеваний органов гепатопанкреатобилиарной зоны (ГПБЗ). Пациенты этой группы в хирургических стационарах составляют до 25% всех больных с заболеваниями желудочно-кишечного тракта (ЖКТ). Наиболее часто встречаются заболевания, связанные с желчекаменной болезнью (ЖКБ) и опухолевыми поражениями органов этой зоны. Одним из наиболее часто встречающихся осложнений заболеваний ГПБЗ является нарушение проходимости желчевыводящих протоков (ЖВП) с развитием механической желтухи (МЖ). Частота развития МЖ при заболеваниях ГПБЗ по данным разных авторов составляет от 12,0 до 45,2% (Зверев Д.В.,1989; Дедерер Д.М. и соавт., 1990; Воробьев Г.И. и соавт., 2004). Причем при доброкачественных заболеваниях этот уровень колеблется от 4,8 до 22,5%, а при злокачественных поражениях — от 36,6 до 47,0% (Ившин В.Г., 1991; Шалимов А.А. и соавт., 1993; Скипенко О.Г., 2004 и др.)
В Казанском городском центре хирургии органов ГПБЗ (городская клиническая больница №7) с 2000 по 2007 г.г. лечились 344 больных с МЖ. Из них у 125 больных (36,3%) причиной обструкции ЖВП были заболевания неопухолевого характера, а у 219 (63,7%) — опухоли органов ГПБЗ.
По количеству наблюдений неопухолевые заболевания ГПБЗ, как причина МЖ, распределились следующим образом:
Название заболевания | Кол-во больных |
| Желчекаменная болезнь | 83 |
| Стеноз большого дуоденального сосочка | 7 |
| Хронический индуративный панкреатит | 4 |
| Киста поджелудочной железы | 5 |
| Парафатериальный дивертикул двенадцатиперстной кишки | 3 |
| Стриктура билиодигестивных анастомозов | 10 |
| Рубцовая стриктура гепатикохоледоха | 2 |
| Синдром Миризи | 4 |
| Первично-склерозирующий холангит (ПСХ) | 6 |
| Аденоматоз гепатикохоледоха | 1 |
Чаще тяжелые формы МЖ развиваются при опухолевом поражении органов ГПБЗ.
По материалам нашей клиники, по локализации опухоли больные распределились следующим образом:
Локализация опухоли | Кол-во больных |
| Рак поджелудочной железы | 116 |
| Метастатическая опухоль ворот печени и гепатохоледоха | 35 |
| Рак желчного пузыря и гепатохоледоха | 28 |
| Рак большого дуоденального сосочка | 15 |
| Опухоль Клатскина | 13 |
| Холангиокарцинома | 4 |
| Первичный рак печени | 3 |
| Метастатическая опухоль печени | 3 |
| Рак двенадцатиперстной кишки | 2 |
Как видно из таблиц, наиболее частой причиной МЖ неопухолевого генеза является ЖКБ (44,8%), а из опухолевых заболеваний — рак поджелудочной железы (52,9%).
При лечении больных с МЖ достаточно часто допускаются диагностические и тактические ошибки. По нашим данным, около 15% больных сначала были госпитализированы в инфекционные и терапевтические стационары. Их пребывание в этих стационарах затягивается от 2 до 8 недель (особенно в терапевтических). Более 41,8% больных с МЖ в наш стационар поступили с желтухой тяжелой степени тяжести. При этом развивающаяся желчная гипертензия, длительный холестаз вызывают глубокие морфологические и фукциональные изменения в печени, выражающиеся в печеночной недостаточности. Страдает функция почек, центральной нервной системы и других органов и систем жизнеобеспечения.
Наши экспериментальные и клинические исследования методом проточной цитометрии (Давыдов В.Г., Бойчук С.В., Шаймарданов Р.Ш., 2006) показали, что при МЖ длительностью 30 дней и более погибает до 30% гепатоцитов. Поэтому ранняя диагностика и декомпрессия ЖВП при МЖ имеет исключительно важное значение.
Наш опыт показывает, что при лечении больных с МЖ нередко допускаются тактические ошибки. Одной из них, по нашему мнению, является то, что в хирургических стационарах иногда устанавливают показания к операции без предварительной декомпрессии ЖВП, разрешения желтухи, нормализации функции печени и других органов и систем. По данным И.И.Шиманко, С.Г.Мусслиус (1993) и И.И.Затевахина (2004), у 40% умерших на фоне МЖ незлокачественного генеза и 2/3 случаев опухолевой обструкции ЖВП, причиной летальности является печеночная и почечная недостаточность.
Еще одной из хирургических тактических ошибок при лечении больных с МЖ является выполнение оперативных вмешательств без установления причины желтухи. Как правило, в таких случаях накладывают один из вариантов билиодигестивных анастомозов, чаще холецистоеюно- или холедоходуоденостомию. Таким образом, лечат симптом (желтуху), а не болезнь. Подобная тактика совершенно недопустима при МЖ опухолевого генеза.
Как показывает практика, тщательно собранный анамнез, сопоставление анамнеза физикального обследования и лабораторных тестов позволяет правильно определить обструктивный или необструктивный характер желтухи примерно у 70 — 75% больных.
Ведущее место в диагностике обструкции ЖВП принадлежит инструментальным методам исследования.
Методы диагностики.
Определение уровня блока ЖВП является одним из ключевых пунктов в выборе дальнейшей тактики лечения. Основным ориентирующим неинвазивным методом в этом плане является ультразвуковое исследование (УЗИ). По нашим данным, чувствительность УЗИ в определении уровня обструкции ЖВП составляет 91,2%, что совпадает с данными других авторов (Куцевич Г.И., 1993; Jugiyama М. et all, 1997 и др.). Основным ультразвуковым признаком обструкции ЖВП является расширение вне- и внутрипеченочных желчных протоков — симптом билиарной гипертензии. На наш взгляд, в начальном этапе верификация причины обструкции — опухолевая или неопухолевая — не является главным вопросом. Важно установить наличие билиарной гипертензии и уровень блока.
Для дистального блока ЖВП характерны расширение гепатикохоледоха, а в более поздних сроках и расширение внутрипеченочных протоков, увеличение размеров желчного пузыря (симптом Курвуазье). Желчный проток считаем расширенным, если его диаметр превышает 10 мм. Он бывает более выраженным при опухолевом блоке.
При высоком блоке (проксимальных желчных путей — ПЖП) выявляется расширение внутрипеченочных протоков, отсутствие ниже стриктуры участков протоковой системы, которые еще ниже принимают нормальные очертания и размеры, а также наличие спавшегося желчного пузыря. Для опухолевого блока ПЖП характерны увеличение ширины сегментарных протоков до 5 мм и более. Саму опухоль удается визуализировать в 51,3% наблюдений. Примерно такие же данные (45,8%) дают и другие авторы (Вишневский В.А., Тарасюк Т.И., 2004). При УЗИ органов ГПБЗ определяется и способ декомпрессии ЖВП.
При компьютерной томографии (КТ) выявляются те же признаки, что и при УЗИ. По данным В.А.Вишневского и Т.И.Тарасюка (2004), при КТ уровень обструкции определяется в 98,1%, а R.N.Gibson (1986) и D.H.Carr (1990) — в 90% случаев.
Высокоинформативным способом является магнитно-резонансная томография (МРТ), так как позволяет визуализировать опухоль, протоковую систему и сосудистые структуры.
Зарубежные и отечественные специалисты сообщают об эффективном применении трехмерной магнитно-резонансной холангиопанкреатографии (Бахтиозин Р.Ф. и соавт., 1998; Lee M.G. et all, 1997). Этот вид МРТ позволяет получить нативное изображение желчных протоков, сопоставимое по диагностической ценности с прямым рентгенконтрастированием желчных протоков. Такая информативность тем более значима в связи с неинвазивностью этого исследования (Jshiazaki Y. еt all, 1993).
Наиболее диагностически значимым при МЖ являются методы прямого рентгенконтрастирования желчного дерева. К ним относятся чрескоскожно-чреспеченочная холангиография (ЧЧХГ) и чрескожно-чреспеченочная холецистография (ЧЧХцГ). В настоящее время от ЧЧХГ и ЧЧХцГ без дренирования ЖВП (только с целью диагностики) мы отказались. При пункции сразу устанавливаются дренажи в виде чрескожно-чреспечоночной холангиостомии (ЧЧХС) или чрескожно-чреспеченочной холецистостомии (ЧЧХцС). А рентгеноконтрастные исследования проводим через дренажные трубки — фистулохолангиография или фистулохолецистохолангиография.
Несмотря на инвазивный характер, ЧЧХС и ЧЧХцС остаются «золотым стандартом» в определении характера поражения билиарного тракта как опухолевого, так и неопухолевого генеза. Неоспоримым преимуществом этих методов является то, что кроме диагностического назначения они являются методом превентивной декомпрессии билиарного тракта, а у больных с проксимальным опухолевым блоком — единственным реальным путем разрешения желтухи перед возможной радикальной операцией. ЧЧХГ и ЧЧХцГ в 100% случаев позволяют определить уровень блока, в большинстве случаев и его этиологию.
Одним из способов прямого рентгенконтрастирования ЖВП является эндоскопическая ретроградная пакреатохолангиография (ЭРПХГ). В определении проксимального блока чувствительность методики достигает 95-97%. Однако, методика позволяет определить только уровень обтурации, а данных о состоянии протоков выше обтурации получить не удается. А при низком блоке, на уровне БДС, поджелудочной железы, выполнить ЭРПХГ технически невозможно.
Бесспорно, ЭРПХГ является ценным диагностическим способом при ПСХ, синдроме Миризи, холедохолитиазе, стриктуре гепатикохоледоха.
Из эндоскопических методов диагностики при МЖ применяется дуоденоскопия. Мы это исследование называем дуоденопапиллоскопией, тем самым подчеркивая, что объектом исследования является большой дуоденальный сосок и околососковая зона. При ряде заболеваний неопухолевого генеза (стеноз БДС, ущемленный камень БДС, холедохолитиаз) она становится и лечебным методом, выполняя при этом эндоскопическую папиллосфинктеротомию (ЭПСТ) и холедолитоэкстракцию. При помощи дуоденопапиллоскопии диагносцируются и морфологически верифицируются опухоли БДС, 12 п.к., поджелудочной железы (при наличии прорастания стенки 12 п.к.).
В нашей клинике при низком блоке ЖВП дуоденопапиллоскопия является обязательным методом исследования.
Лабораторная диагностика. Лабораторные исследования при МЖ, кроме вирусных маркеров, в аспекте установления характера желтухи (механическая или другого генеза), этиологии (причина блока) практического значения не имеют. Общепринятые лабораторные исследования используются для определения степени тяжести желтухи (холестаза), активности патологического процесса (цитолиза) и состояния синтетической функции печени.
Степень холестаза оценивается по количеству циркулирующего в плазме крове общего билирубина (Bi) и его фракций. Маркерами холестаза являются щелочная фосфатаза (ЩФ) и Y-глютамилтранспептидаза (ГГТП). При холестазе нарушается экскреция этих ферментов в желчь и нарастает их концентрация в сыворотке крови.
Активность патологического процесса в печени (цитолиз) оценивается по уровню активности аспартат- и аланинаминотрансаминаз (АсТ, АлТ). АсТ является митохондриальным, а АсТ цитоплазматическим ферментами. При выраженной активности патологического процесса — цитолиза — показатели активности АсТ и АлТ увеличиваются в несколько раз. При тяжелой печеночно-клеточной недостаточности их активность может резко снижаться.
Состояние синтетической функции печени определяется по количеству белков плазмы крови, их фракций и показателю протромбинового индекса (ПТИ). В печени синтезируются весь альбумин и 80% глобулинов. Снижение количества белков плазмы крови является показателем нарушения синтетической функции печени. Более чувствительным тестом является показатель ПТИ.
Для верификации опухолевых заболваний печени и ЖВП рекомендуют определение опухолевых маркеров — а-фетопротеина и углеводного антигена СА 19-9. Но нужно помнить, что СА 19-9 выводится исключительно желчью. Поэтому, даже незначительное повышение уровня Bi в сывортоке крови может быть причиной повышения уровня этого маркера
Из лабораторных методов исследования обязательным для каждого больного с желтухой является определение серологических маркеров вирусного гепатита.
Лечебная программа при МЖ. Первостепенной задачей при лечении больных с МЖ является декомпрессия ЖВП или, при наличии возможности, восстановление желчеоттока, разрешение желтухи, нормализация функции печени.
При МЖ неопухолевого генеза (стеноз БДС, холедохолитиаз) в ряде случаев удается восстановить желчеотток в кишечную трубку без предварительной декомпрессии ЖВП путем применения эндоскопических вмешательств — ЭПСТ и эндоскопической холедолитоэкстракции. ЭПСТ применена нами в 5 наблюдениях при стриктуре БДС, когда его протяженность не превышала 2,0 см. В 19 наблюдениях желчеотток восстановлен путем холедохолитоэкстракции.
В подавляющем большинстве случаев МЖ неопухолевого генеза и у всех больных опухолевым блоком ЖВП возникает необходимость декомпрессии ЖВП малоинвазивными методами.
В настоящее время двухэтапное лечение МЖ общепринято и не дискутируется.
Первым этапом выполняется дренирование ЖВП малоинвазивными способами под лучевым контролем. Вторым этапом, после разрешения желтухи, выполняются радикальная или паллиативная операции. Сроки оперативных вмешательств определяются индивидуально. Двухэтапная схема лечения больных с МЖ позволила снизить послеоперационную летальность до 1,5 — 14,3% (Борисов А.Е. и соавт., 1997; Hotincanu V. Et all, 2005; Bhati S. Et all., 2007).
Выбор способа дренирования ЖВП зависит от уровня блока. При низком блоке, если ранее больной не перенес холецистэктомию, методом выбора является холецистостомия. Холецистостому можно наложить операционным путем, под лапароскопическим и УЗ-контролем. Холецистостомия, как метод декомпрессии при МЖ, нами применена в 83 случаях. Их них у 8 больных она наложена операционным путем (все они выполнены в других ЛПУ, потом больные переведены в нашу клинику), у 3-х больных под лапароскопическим контролем и у 72 пациентов — под УЗ-контролем. Микрохолецистостомии под лапароскопическим контролем выполнены в тех случаях, когда лапароскопия выполнялась с диагностической целью, при котором установлены показания к холецистостомии.
При высоком блоке единственным способом декомпрессии ЖВП является ЧЧХС. ЧЧХС под УЗ-контролем нами применена у 114 больных. Показаниями были: холедохолангиолитиаз — 12, низкий опухолевый блок при ранее перенесенной холецистэктомии — 3, стеноз гепатико-еюноанастомоза — 13 и опухолевая обструкция гепатикохоледоха различного уровня и печеночных протоков — 86.
Нами предложен троакарный способ ЧЧХС для которого разработаны специальные инструменты (патент РФ №72139 от 10.04.2008)
Одним из недостатков длительного наружного отведения желчи является развитие синдрома ахолии. Отсутствие поступления желчных кислот в кишечник приводит к избыточному размножению в его просвете грамотрицательной флоры и способствует всасыванию бактерий и их токсинов в портальный кровоток.
При ахолии нарушаются белковый (без желчи нет активации протеаз), жировой (нет эмульгации жиров) и углеводный обмены. Нарушается экскреторная функция поджелудочной железы, так как желчь является одним из стимуляторов секреции поджелудочной железы. Больные при отсутствии поступления желчи в кишечник быстро истощаются. Поэтому возникает необходимость возврата желчи в кишечник. Возврат желчи в кишечную трубку мы осуществляем через назодуоденальный катетер устанавливаемый эндоскопическим путем.
После разрешения желтухи, восстановления функции печени и верификации диагноза путем дополнительных исследований выполняются радикальные или паллиативные оперативные вмешательства, направленные на восстановление оттока желчи в кишечную трубку.
При лечении больных с МЖ в клинике разработан следующий лечебно-диагностический алгоритм:
1. Каждый больной с желтухой до госпитализации в хирургический стационар должен быть консультирован инфекционистом и исключен вирусный гепатит.
2. Уточнение характера желтухи и ее тяжести (УЗИ, дуоденопаиллоскопия, лабораторная диагностика, ЭРПХГ — по показаниям)
3. Декомпрессия ЖВП или восстановление желчеоттока:
— ЧЧХцС — при низком блоке
— ЧЧХС — при высоком блоке
— ЭПСТ — при стенозе БДС
— эндоскопическая холедохолитэксткракция — при холедохолитиазе
4. Назодуоденальное зондирование с последующим возвратом желчи в кишечник
5. Уточняющая диагностика (фистулохолецистохолангиография, фистулохолангиография, ЭРПХГ, КТ)
6. Радикальное или паллиативное оперативное вмешательство (после разрешения желтухи).
Р.Ш. Шаймарданов, В.А. Филиппов, С.З. Шарафиев
Казанская государственная медицинская академия
Литература:
1. Бахтиозин Р.Ф., Джорджикия Р.К., Чугунов А.Н. Магнитно-резонансная холангиопанкреатография в диагностике билиарной и панкреатической гипертензии // Анналы хир. гепатол. — 1998. — Т.3(3) — с.35.
2. Блохин Н.Н., Штин А.Б., Клименков А.А. Рак поджелудочной железы и внепеченочных желчных путей. — М.: Медицина, 1982. — 270 с.
3. Вишневский В.А., Тарасюк Т.И. Диагностика и хирургическое лечение рака проксимальных отделов печеночных протоков // Практическая онкология. — Т.5, №2. — 2004, — с.126-132.
4. Давыдов В.Г., Бойчук С.В., Шаймарданов Р.Ш., Миннебаев М.М. Молекулярные механизмы апоптоза и некроза гепатоцитов. Особенности гибели гепатоцитов при обструктивном холестазе // Российский журнал Гастроэнтерологии, Гепатологии, Колопроктологии. — Т.XVI, №5. — 2006, — с.11-19.
5. Ившин В.Г., Лукичев О.Д. Малоинвазивные методы декомпрессии желчных путей у больных механической желтухой. — Тула: ГРифик, 2003, — 182 с., ил.
6. Шалимов А.А., Шалимов С.А., Нечитайло М.Е., Доманский Б.З. Хирургия печени и желчных путей. — Киев, 1993. — 508 с.
7. Шиманко И.И., Мусселиус С.Г. Острая печеночно-почечная недостаточность. — М.: Медицина, 1993. — 228 с.
8. Car D.H., Hadjis N.S., Hemigway A.P., Blumgart L.H. Computer tomography of hilar cholangiocarcinoma: a new // AJK. — 1990 july 1985. — Vol.145.- P.53-56.
9. Gibson R.N., Yeung E., Teompson J.N. et al. Bill duct obstraction: radiologic evalution of level, cause and tumor reseetability // Radilogy, — 1986. — Vol.160. — P.43-47.
10. Ishizaki V., Wakayma T., Okada V., Kobayashi T. Magnitic resonance for evalution of obstructive jaundice // Amer.J.Gastroenterol. — 1993. — Vol.88 — P.2072-2077.
11. Iugiyama M. et al. Bile duct carcinoma with out jaundice: clues to early diagnosis // Hepato — Gastroenterol. — 1997. — Vol.44, 107, N6 — P.597-603.
Источник
Некоторые аспекты диагностики и дифференциальной диагностики механической желтухи
УЗИ сканер HS60
Профессиональные диагностические инструменты. Оценка эластичности тканей, расширенные возможности 3D/4D/5D сканирования, классификатор BI-RADS, опции для экспертных кардиологических исследований.
Введение
Механическая желтуха (МЖ) — патологический синдром, обусловленный нарушением оттока желчи из желчных протоков печени в двенадцатиперстную кишку (ДПК). Проблема диагностики и дифференциальной диагностики причин обтурации желчных путей не потеряла актуальности и в настоящее время. Хирургические вмешательства у больных МЖ, выполняемые по экстренным показаниям, сопровождаются большим числом осложнений, а летальность достигает 15-30%, что в 4 раза выше, чем в тех случаях, когда МЖ удается ликвидировать до операции. Декомпрессия билиарной системы является одной из главных целей и важнейшим компонентом лечебных мероприятий у этих пациентов [1-3].
Этиологические факторы механической желтухи
- Пороки развития: атрезии желчевыводящих путей; гипоплазия желчных ходов; врожденные кисты холедоха; дивертикулы ДПК, расположенные вблизи большого дуоденального сосочка (БДС).
- Доброкачественные заболевания желчных путей: желчнокаменная болезнь (ЖКБ), осложненная холедохолитиазом; вколоченные камни БДС; воспалительные стриктуры желчевыводящих путей; стеноз БДС.
- Воспалительные заболевания: острый холецистит с перипроцессом; склерозирующий холангит; псевдотуморозный панкреатит; паразитарные поражения печени в области ворот печени; воспалительные инфильтраты в области ворот печени; острый папиллит; увеличение лимфатических узлов печеночнодвенадцатиперстной связки.
- Опухоли: папилломатоз желчных ходов; рак печеночных и общего желчного протоков (ОЖП); объемные образования БДС; рак головки поджелудочной железы (ПЖ); метастазы и лимфомы в воротах печени.
- Структуры магистральных желчных протоков, развивающиеся в результате операционной травмы.
Инструментальная диагностика механической желтухи
- Ультразвуковое исследование (УЗИ). Основным признаком МЖ при УЗИ является расширение внутрипеченочных желчных протоков (рис. 1). УЗИ позволяет не только выявить билиарную гипертензию, но и установить уровень блока.
При высоком билиарном блоке (обтурация на уровне ворот печени) при УЗИ визуализируются расширенные внутрипеченочные протоки при нормальном диаметре ОЖП (до 6 мм), желчный пузырь чаще нормальных размеров или уменьшен, возможно выявление в воротах печени объемного образования.
При низком билиарном блоке (обтурация на уровне холедоха, головки ПЖ, БДС) кроме расширенных внутрипеченочных протоков визуализируются расширенные внепеченочные протоки, желчный пузырь увеличен (рис. 2).
Если низкий блок обусловлен индуративным панкреатитом, при УЗИ имеет место увеличение органа в размере, могут выявляться кальцинаты в ПЖ (рис. 3). При опухоли головки ПЖ на фоне билиарной гипертензии визуализируется объемное образование в ПЖ (рис. 4). Критериями гипертензии главного панкреатического протока служит его расширение более 2 мм в теле и более 3 мм в головке ПЖ.
При ЖКБ, осложненной холедохолитиазом, выявляется увеличенный желчный пузырь с конкрементами, а также конкременты в холедохе (рис. 5).
Диагностируют очаговые поражения печени: эхинококковые и альвеококковые кисты; увеличенные лимфоузлы; местатазы.
- Эндоскопическая ретроградная холангиопанкреатография (ЭРХПГ).
- Чрескожная чреспеченочная холангиография.
ЭРХПГ и холангиография под контролем УЗИ [1-3] могут сопровождаться и последующим лечебным эффектом (установкой потерянного дренажа,папиллотомией, холангиостомией).
- Компьютерная томография — КТ и магнитно-резонансная томография (МРТ) печени и желчевыводящих путей.
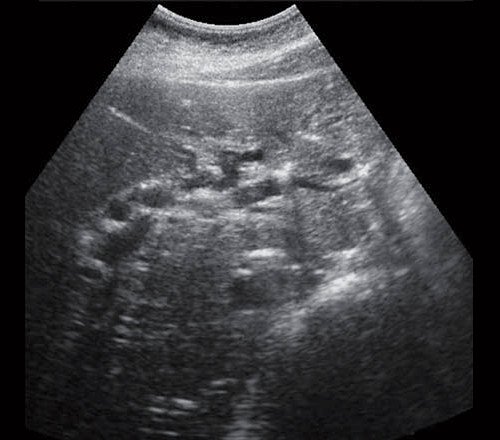
Рис. 1. Ультразвуковая картина билиарной гипертензии при механической желтухе.
Рис. 2. Эхографическая картина низкого печеночного блока, обусловленного опухолью головки ПЖ.
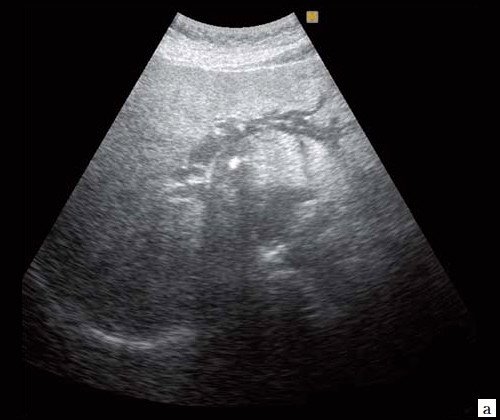
а) Расширенные внутрипеченочные протоки.
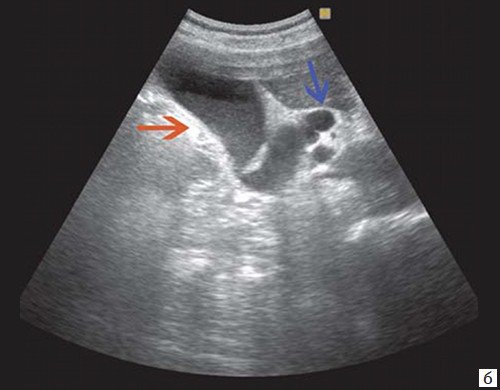
б) Увеличенный желчный пузырь с густой взвесью (красная стрелка) и расширенный ОЖП (синяя стрелка).
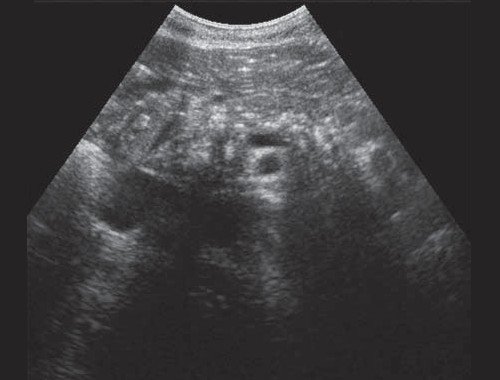
Рис. 3. Эхографическая картина хронического псевдотуморозного панкреатита. Кальцинаты в паренхиме ПЖ.
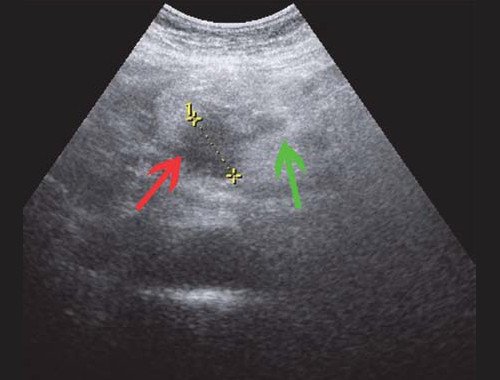
Рис. 4. Ультразвуковая картина опухоли головки ПЖ: образование в головке ПЖ (красная стрелка), расширенный панкреатический проток (зеленая стрелка).
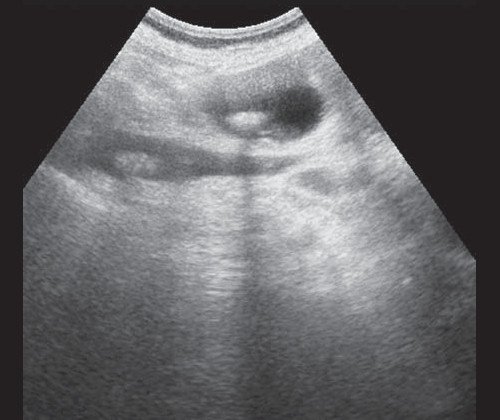
Рис. 5. Ультразвуковая картина билиарной гипертензии при механической желтухе, обусловленной ЖКБ, осложненной холедохолитиазом, конкременты в желчном пузыре и ОЖП.
Дифференциальный диагноз механической желтухи
Дифференциальную диагностику механической желтухи, в первую очередь, нужно проводить с паренхиматозной желтухой.
Паренхиматозная желтуха возникает при гепатитах и циррозах печени, развивается постепенно. Основной отличительный ультразвуковой признак паренхиматозной желтухи от механической — отсутствие расширения внутри- и внепеченочных желчных протоков.
Ультразвуковые признаки острого вирусного гепатита [4] включают увеличение размеров печени за счет обеих долей; в поздних стадиях возможно уменьшение размеров печени (симптом тающей льдинки); эхогенность паренхимы низкая (симптом темной печени); структура может быть однородной за счет выраженного отека паренхимы либо неоднородная (симптом выделяющихся сосудов); более выраженное обогащение сосудистого рисунка; уменьшение диаметра магистральных стволов печеночных вен; незначительное увеличение диаметра основного ствола воротной вены; снижение показателей скоростного и объемного кровотока по воротной вене; увеличение лимфоузлов в области гепатодуоденальной связки; спленомегалия (увеличение площади селезенки более 50 см²).
Ультразвуковые признаки хронического гепатита [4] включают увеличение размеров печени; контур печени четкий и ровный; закругление краев и увеличение углов; структура органа диффузно неоднородна; эхогенность паренхимы повышена; обеднение сосудистого рисунка на периферии; основной ствол воротной вены не расширен.
Ультразвуковые признаки цирроза печени [5-7] включают увеличение размеров печени на начальной стадии и уменьшение в терминальной; гипертрофию хвостатой доли печени; контуры становятся неровными, бугристыми; капсула четко не дифференцируется; структура паренхимы диффузно неоднородной со множественными участками повышенной эхогенности (очаги фиброза) и пониженной эхогенности (очаги регенерации); обеднение сосудистого рисунка на периферии.
При развитии портальной гипертензии [5, 7, 8] выявляются типичные эхографические признаки: увеличение диаметра портальной вены со снижением линейной скорости кровотока; изменение просвета портальной вены при глубоком вдохе не более 10%; увеличение диаметра селезеночной (свыше 8 мм), верхней и нижней брыжеечных вен; увеличение диаметра внепеченочной части воротной вены свыше 15 мм; гепатофугальное направление кровотока; выявление различных порто-портальных и порто-кавальных коллатералей (рис. 6); спленомегалия; асцит.
Рис. 6. Эхограмма портальных коллатералей воротной вены.
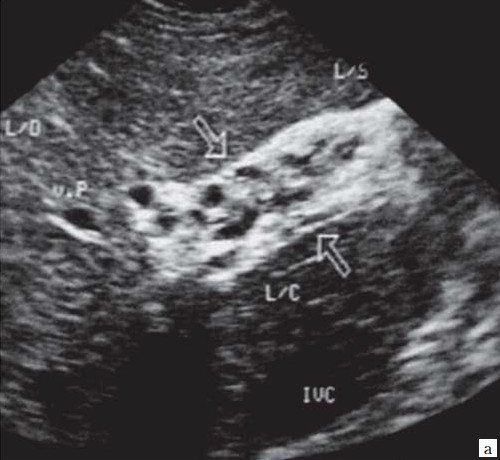
а) В-режим. Отсутствие типичного трубчатого анэхогенного ствола воротной вены с гиперэхогенными стенками. Ствол воротной вены виден как неоднородной структуры образование с множеством эхогенных, параллельно идущих стенкам сосуда перегородок (стрелка). Наличие гиперэхогенных участков в паравенозной области воротной вены.
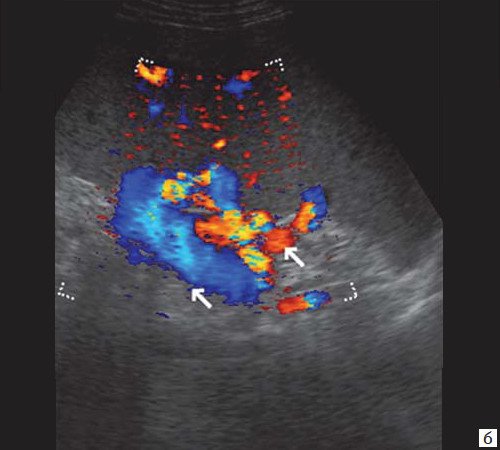
б) Режим ЦДК. Выраженные крупные коллатерали в проекции воротной вены.
При паренхиматозной желтухе желательна гистологическая верификация диагноза. С этой целью рекомендовано выполнение пункционно-аспирационной биопсии (ПАБ) печени под контролем УЗИ.
Клиническое наблюдение
Пациентка Л., 73 лет, поступила в стационар с жалобами на пожелтение кожных покровов.
При УЗИ брюшной полости: расширены внутрипеченочные протоки (сегментарные до 6 мм, долевые до 10 мм). ОЖП 14-15 мм. Желчный пузырь 120 30 мм, стенка 3 мм, конкрементов не выявлено. ПЖ нормальных размеров, контуры ровные, четкие. Структура диффузно неоднородная, повышенной эхогенности. Панкреатический проток расширен до 5 мм. Заключение: ультразвуковая картина низкого печеночного блока с билиарной гипертензией, блок на уровне БДС, терминального отдела ОЖП (рис. 7).
Рис. 7. Эхографическая картина опухоли БДС.
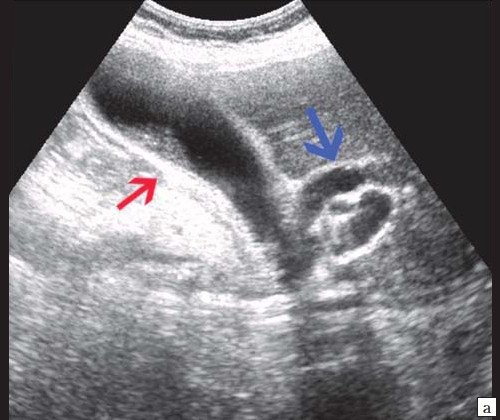
а) Увеличенный желчный пузырь с густой взвесью внутри (красная стрелка) и расширенный ОЖП (синяя стрелка).
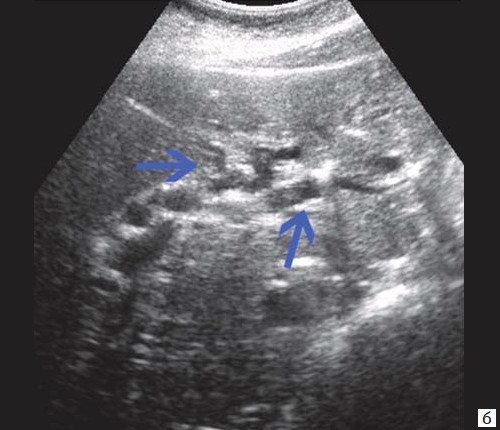
б) Расширение внутрипечоночных протоков (синяя стрелка).
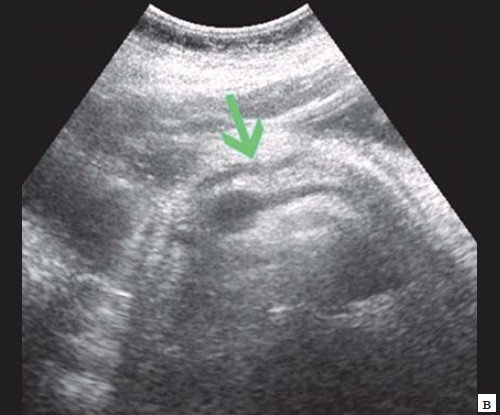
в) Расширение панкреатического протока (зеленая стрелка).
Мультиспиральная КТ с болюсным контрастированием: внутри- и внепеченочные желчные протоки расширены (долевые до 9 мм, общий печеночный проток (ОПП) 14 мм, интрапанкреатическая часть холедоха 12 мм). Вирсунгов проток расширен на всем протяжении до 6 мм. В проекции БДС визуализируется мягкотканое образование до 11 мм, накапливает контраст. Заключение: опухоль БДС с низким печеночным блоком.
Проведенные ЭРХПГ с эндоскопической папиллосфинктеротомией (ЭПСТ) установили: БДС значительно увеличен в размере, напряжен, в области устья инфильтрация слизистой, бесструктурные мелкобугристые разрастания, контактная ранимость, катетеризация боковым папиллотомом безуспешна. Выполнено рассечение продольной складки торцевым папиллотомом с формированием супрапапиллярной фистулы. При ЭРХПГ контрастируется расширенный холедох, прерывающийся на уровне интрапанкреатического отдела, без эвакуации контраста. В фистулу по проводнику установлен «потерянный» дренаж холедоха (7 см), получен отток контраста в кишку. Заключение: эндоскопическая картина опухоли БДС. Состояние после ЭРХПГ, ЭПСТ. Установка «потерянного» дренажа холедоха.
Таким образом, был установлен диагноз: папиллярная аденома БДС. Острый холецистит. Паравезикальный абсцесс. Механическая желтуха.
Выводы
- Методы лучевой диагностики оказывают существенную помощь в диагностике и дифференциальной диагностике МЖ.
- Решающая роль в диагностике и дифференциальной диагностике МЖ первичного звена принадлежит УЗИ.
- На втором этапе исследования в зависимости от уровня блока показаны ЭРХПГ (возможно, в сочетании с ЭПСТ), КТ, МРТ, чрескожная чреспеченочная холангиография под контролем УЗИ.
- Малоинвазивные эндоскопические и чрескожные чреспеченочные декомпрессионные вмешательства представляют собой эффективный способ восстановления желчеоттока при обструкции билиарной системы. Эти методики позволяют достаточно быстро и эффективно ликвидировать желтуху и холангит, дают возможность проводить хирургические вмешательства в наиболее благоприятных условиях, в плановом порядке, а у больных пожилого возраста с тяжелой сопутствующей патологией могут служить альтернативой хирургическому лечению.
Литература
- Tannapfel A., Wittekind C. (2004). Gallbladder and bile duct carcinoma. Biology and pathology. Internist 45: 33-41.
- Valle J., Wasan H. et al. (2010). Cisplatin plus gemcitabine versus gemcitabine alone for billiary tract cancer. N Engl J Med 362: 1273-1281.
- Wiedmann M.W., Mossner J. (2010). Molecular targeted therapy of biliary tract cancer — results of the first clinical studies. Curr Drug Targets 11: 834-850.
- Балашов А.Т. Возможность использования ультразвукового исследования при определении степени тяжести острого вирусного гепатита (обзор литературы) // Медицинская визуализация. 2007, N 1. С. 32-37.
- Михайлов М.К. Эхография в диагностике цирроза. М.: МЕДпресс-информ. 2003.
- Шипов О.Ю., Сюткин В.Е., Матюхина А.П., Иваников И.О. Особенности ультразвуковой картины у больных циррозом печени с разной степенью активности алкогольного гепатита // Медицинский журнал «SonoAce-Ultrasound». 2007. N 16. С. 46-51.
- Annet L., Materne R., Danse E. et al. Hepatic flow parameters measured with MR imaging and Doppler US: Correlations with degree of cirrhosis and portal hypertension // Radiology. 2003. V. 229. P. 409-414.
- Васильев В.А., Лисаченко Н.А., Цеханович К.Б. Возможности ультразвуковой допплерографии портальной системы в диагностике вирусных гепатитов // Материалы III научно-практической конференции с международным участием. Петрозаводск. 2004. С. 82-83.

УЗИ сканер HS60
Профессиональные диагностические инструменты. Оценка эластичности тканей, расширенные возможности 3D/4D/5D сканирования, классификатор BI-RADS, опции для экспертных кардиологических исследований.
Источник