При каком виде желтухи не показана ретроградная холангиография
Содержание статьи
Холангиография
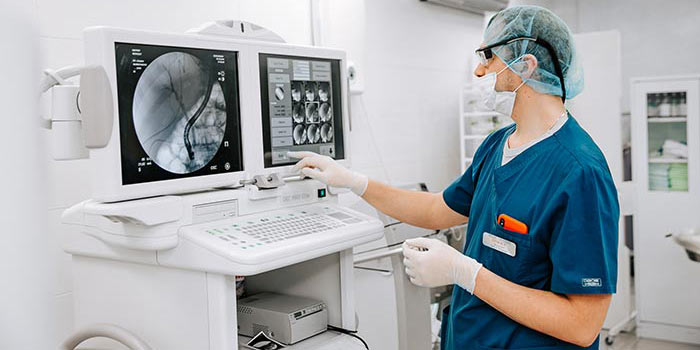
Холангиография — обследование желчных путей под рентгеном или МРТ с помощью контрастирования специальным веществом. Фактически холангиография «рисует» картину выведения желчи в данный конкретный период времени и показывает внутренние препятствия для нормального функционирования системы — камни, опухоль, рубцовое сужение. Холангиография — процесс обследования, а зафиксированная рентгеном картинка — холангиограмма.
Показания
Желчь синтезируется клетками печени и по внутрипеченочным протокам собирается в желчном пузыре, лежащим на нижней поверхности печени. Через некоторое время после еды желчь из пузыря подается в двенадцатиперстную кишку, где она взаимодействует с полупереваренной пищей, расщепляя её компоненты на составные части. Желчный пузырь и двенадцатиперстная кишка соединены общим желчным протоком, куда чуть выше кишки впадает проток поджелудочной железы.
При холангиографии контрастное для рентгена вещество окрашивает внепеченочные протоки, показывая их структуру и проходимость, фиксируя места сужения и причину сужения. Поэтому к холангиографии прибегают в случаях:
- Желтухи неинфекционной природы, когда из-за механического препятствия нормальному току желчи желчные кислоты попадают не в кишку, а всасываются в кровь, что возможно при закупорке главного желчного протока — холедоха камнем, сдавлении его рубцами, а также блокировке опухолью дуоденального сосочка — места впадения протока в двенадцатиперстную кишку.
- Рака поджелудочной железы, когда необходимо восстановить проходимость сдавленного раковым конгломератом холедоха специальным дренажом или стентом, чтобы улучшилось состояние, регрессировала механическая желтуха и больного подготовили к плановой операции.
- Воспаления поджелудочной железы с частыми обострениями для поиска причины хронизации патологии.
- Наличия патологических гнойных ходов — свищей между поджелудочной и двенадцатиперстной, сформировавшихся после тяжелого панкреатита.
После установления точной причины патологии желчевыведения, холангиография из диагностического мероприятия может стать лечебной процедурой, ликвидирующей это патологическое препятствие.
Виды холангиографии
Контрастное вещество в желчь может попасть двумя путями — непосредственно смешиваясь с желчью в протоке или после внутривенного введения первоначально попадая в печеночный кровоток, а оттуда выделяясь с желчью.
Непосредственное смешивание контраста с желчью возможно несколькими способами:
- ретроградная или, по-русски, противоточная холангиография (РХПГ, ЭРХПГ) сегодня «золотой стандарт» обследования при патологии желчевыведения, осуществляется при одновременной эндоскопии двенадцатиперстной кишки и рентгеновском обследовании;
- чреспеченочная холангиография предполагает введение контраста в крупный желчный проток при пункции через брюшную стенку, процедура не свободна от непосредственных осложнений, поэтому предпочтительно проводить её перед операцией;
- чрескожная холангиография выполняется при лапароскопии, и контрастное вещество сначала иглой вводят в желчный пузырь, манипуляция чревата последующим истечением желчи по сформированному толстой иглой ходу;
- фистулохолангиография возможна при наличии свищей, потому что контрастируется свищевой ход и далее прослеживается выделение препарата соединённым с ним протоком.
Выделение контраста при введении его в кровеносную систему осуществляется:
- при внутривенной холангиографии, сегодня признанной не сильно результативной т точной манипуляцией, вследствие чего от неё отказались в пользу более точного обследования;
- магнитно-резонансная холангиография исключает прокол пузыря и желчных путей, гарантируя высокое качество обследования и 90% точность диагностики, но при крошечных камушках уступает эффективности ЭРХПГ, да и довольно дорогая процедура, требующая специального оборудования.
По времени выполнения холангиография подразделяется на следующие виды:
- предоперационную, чаще всего выполняется именно ЭРХПГ, реже — чрескожная-чреспеченочная диагностическая манипуляция;
- интраоперационную — во время хирургического вмешательства путём введения катетера в проток;
- послеоперационную, как правило используемую для контроля результата оперативного вмешательства, когда подача контраста осуществляется через ранее установленный дренажный катетер.
Безусловное лидерство принадлежит ЭРХПГ, сочетающей высокую чувствительность и такую же точность диагностики, возможность детального эндоскопического осмотра верхних отделов желудочно-кишечного тракта и выполнения лечебной процедуры сразу же после выявления причины патологии.
Подготовка к ЭРХПГ
Эндоскопическая ретроградная холангиопанкреатография не проводится амбулаторно в поликлинике, необходима кратковременная госпитализация пациента, поскольку требуется предварительная медикаментозная подготовка к процедуре. Вмешательство требует хорошей анестезии или даже наркотизации, а после манипуляции осуществляется мониторинг состояния и своевременное выявление осложнений, если таковые случились.

Накануне процедуры пациенту даются успокоительные средства, позитивно действующие на центральную и периферическую нервную систему, и расслабляющие мышечные слои желудочно-кишечного тракта спазмолитические препараты. Очень выраженная перистальтика кишечника купируется введением лекарственных средств. Перед введением гастроскопа обезболивается глотка, но также возможно выполнение диагностической манипуляции под наркозом, что облегчает переносимость пациентом и повышает возможности визуализации патологии.
Что касается личной подготовки пациента, то он должен отказаться от еды как минимум за 12 часов.
Методика ЭРХПГ
Совмещение эндоскопии с рентгеновским обследованием оптимально во всех отношениях: максимально возможная диагностика и доступность для осмотра «укромных уголков» при фиксации всего процесса выявления патологии на рентгеновском снимке и диске, что позволит последующее консультирование привлечёнными специалистами не в слепую, а по видео.
Первым этапом выполняется последовательная эндоскопия пищевода, желудка, двенадцатиперстной кишки. Далее по специальному каналу эндоскопа вводится катетер, кончик которого направляется в общий желчный проток, куда и подается контрастное вещество. Расположение контраста в анатомической зоне снимается на рентгеновскую пленку, а процесс движения эндоскопической аппаратуры фиксируется на видео. При обнаружении какого-либо новообразования внутри кишки или протока щипчиками берётся кусочек ткани — биопсия, если камень блокирует проток — тоже щипчиками крошится и удаляется. При сужении протока устанавливается стент или дренажный катетер.
Осложнения
ЭРХПГ сопряжена с внедрением внутрь, то есть инвазивная процедура, плюс используется инородное для организма контрастного вещества. Самое частое, но по факту очень редкое осложнение — воспалительные изменения нежной ткани поджелудочной железы — в среднем у трёх на сотню пациентов. Проявляется клинически панкреатитом — боль в животе, втрое повышение специфического фермента крови — амилазы. Как правило, осложнение развивается уже на первые сутки, за пару дней купируется. В нашей клинике разработана методика снижения и профилактики этого вида осложнений ЭРХПГ.
Вдвое реже возникает кровотечение из места манипуляции, когда при рассечении дуоденального сосочка повреждается сосуд у пациента с нарушениями свёртывания крови, что нередко возникает при длительной или выраженной желтухе.
Разрыв протока возможен у одного-двух пациентов из сотни, что обусловлено рыхлостью тканей при сниженной из-за рубцов растяжимости. Осложнение успешно лечится при своевременном выявлении.
И самое банальное и частое — аллергическая реакция на контрастное вещество. Причём неоднократное обследование с использованием контраста не гарантирует её отсутствие в последующем, аллергия возникает по принципу: вчера не было, а сегодня возникла.
Холангиографияю в Европейской клинике проводят опытные врачи-специалисты на современном оборудовании. Узнайте больше, свяжитесь с нами.
Список литературы:
- Винник Ю.С., Теплякова О.В., Серова Е.В., Пахомова Р.А./ Дооперационная диагностика патологии билиопанкреатодуоденальной зоны// Вестн. хир. гастроэнтер.; 2012, № 1.
- Линденбратен Л.Д./ Рентгенология печени и желчных путей, Руководство для рентгенологов// М.: Медицина; 1980.
- Тимошин А.Д., Шестаков А.Л., Юрасов А.В./ Малоинвазивные вмешательства в абдоминальной хирургии// М.: Триада-Х; 2013
Источник
МЕХАНИЧЕСКАЯ ЖЕЛТУХА: диагностический алгоритм и лечение
Cреди хирургических заболеваний печени и внепеченочных желчных путей наиболее тяжелыми могут быть признаны те, которые сопровождаются стойкой непроходимостью магистральных желчных протоков с последующим развитием механической желтухи (МЖ). Проблемы диагностики и дифференциальной диагностики причин обтурации желчных путей не потеряли актуальности и в настоящее время. Хирургические вмешательства у больных МЖ, выполняемые по экстренным показаниям, сопровождаются большим числом осложнений, а летальность достигает 15-30%, что в 4 раза выше, чем в тех случаях, когда МЖ удается ликвидировать до операции [3, 7]. Огромный опыт, накопленный зарубежными и отечественными хирургами, показывает, что синдром МЖ возникает у 15-40% больных с желчнокаменной болезнью (ЖКБ) и у всех больных, имеющих опухолевое поражение желчных путей [1, 5, 9]. Декомпрессия билиарной системы является одной из главных целей и важнейшим компонентом лечебных мероприятий у этих пациентов.
Людей, страдающих МЖ, следует относить к группе пациентов с острыми хирургическими заболеваниями. В настоящее время большинство зарубежных и отечественных авторов считают оптимальным проведение лечения больных МЖ в два этапа [1, 2, 3, 7, 9, 10]. На первом этапе выполняют временную наружную или внутреннюю декомпрессию билиарных путей с помощью различных методов желчеотведения, а на втором, после ликвидации МЖ, при плановой операции стараются устранить причину, вызвавшую МЖ. Такая тактика лечения позволяет добиться уменьшения количества послеоперационных осложнений и снижения уровня общей летальности.
Вместе с тем в ходе разработки способов желчеотведения у больных МЖ возникает ряд проблем и спорных вопросов. Тяжелыми осложнениями МЖ являются холангит и печеночная недостаточность (ПН). Ведущие факторы в патогенезе холангита — холестаз с последующим присоединением инфекции.
В последнее время для декомпрессии желчных путей используют малоинвазивные эндоскопические или чрескожные чреспеченочные методы желчеотведения под контролем рентгенологического аппарата, ультразвукового аппарата (УЗИ), компьютерного томографа (КТ) или лапароскопа [2, 4, 6, 8, 10]. В 2001 году исполнилось 75 лет с начала применения чрескожных методов контрастирования билиарной системы (Burckhardt H., Muller W., 1921) и 40 лет — чрескожного чреспеченочного желчеотведения у больных МЖ (Remolar I. et al., 1956).
Узловыми вопросами в лечении МЖ остаются сроки и виды декомпрессивных вмешательств, методы профилактики и лечения послеоперационной ПН. Кроме того, оценки эффективности, преимуществ и недостатков различных «закрытых» и «открытых» методов декомпрессии желчных путей при МЖ не проводилось. Поэтому проблема выбора инструментальной дооперационной декомпрессии желчных протоков при МЖ и гнойном холангите остается предметом дискуссии.
Итак, основная цель хирургического вмешательства при МЖ — декомпрессия желчевыводящих путей, устранение обтурации, ликвидация желтухи и профилактика возникновения или прогрессирования ПН. В настоящее время арсенал желчеотводящих методов при МЖ достаточно велик и включает в себя:
- эндоскопическую ретроградную холангиопанкреатографию (ЭРХПГ) с эндоскопической папиллосфинктеротомией (ЭПСТ);
- чрескожную чреспеченочную холангиографию (ЧЧХГ) с чрескожной чреспеченочной холангиостомией (ЧЧХС);
- холецистостомию под контролем УЗИ, КТ или лапароскопа;
- назобилиарное дренирование;
- различные варианты эндопротезирования желчных протоков;
- различные интраоперационные методы декомпрессии желчных протоков.
МЖ может быть доброкачественного (наблюдается у 45-55% больных) и злокачественного генеза. Среди МЖ доброкачественного генеза наиболее часто встречается холедохолитиаз, в остальных случаях речь идет о рубцовых стриктурах внепеченочных желчных путей, панкреатитах, паразитарных заболеваниях гепатобилиарной зоны, дивертикулах и доброкачественных опухолях большого дуоденального сосочка (БДС). Опухолевая природа заболевания обусловлена раком головки поджелудочной железы (ПЖ), БДС, желчного пузыря, гепатикохоледоха, ворот печени и метастазами рака другой локализации в печень.
Накопленный опыт лечения больных МЖ позволил нам разработать и внедрить новый алгоритм диагностики и лечения данной категории больных. В алгоритм диагностики МЖ кроме стандартного клинико-лабораторного исследования входят УЗИ, эзофагогастродуоденоскопия (ЭГДС), ЭРХПГ, КТ, ЧЧХГ и лапароскопия. Каждое исследование при необходимости можно превратить из диагностической процедуры в лечебную. При разработке алгоритма мы исходили из того, что МЖ должна быть ликвидирована как можно раньше от начала заболевания из-за опасности развития холангита и ПН. При этом процесс диагностики МЖ не должен отодвигать сроки начала ее лечения. Целесообразно диагностику и лечение МЖ проводить одновременно, хотя нередко лечение опережает по времени дифференциальную диагностику причины и уровня обтурации желчных путей.
Лечение больных с МЖ должно носить комплексный характер. Консервативные мероприятия кроме нормализации гомеостаза и инфузионной терапии включают следующие мероприятия:
- удаление из организма токсических веществ. Это достигается проведением форсированного диуреза, а также введением гемодеза и аналогичных ему препаратов;
- введение пластических веществ, необходимых для репаративных процессов печеночной паренхимы. При этом необходимо иметь в виду два основных момента: во-первых, до устранения желчной гипертензии пластические вещества усваиваются гепатоцитами плохо и в небольших количествах; во-вторых, перегрузка ими организма больного до восстановления нормального оттока желчи предъявляет повышенные требования к гепатоцитам и вследствие этого может вызвать срыв адаптационных процессов и ухудшить функцию печени. В связи с этим пластические вещества должны назначаться в дозах на уровне минимальных терапевтических (если предварительно не проводилась холецисто- или холангиостомия) и не слишком продолжительными курсами (до 7-10 дней). К этой группе препаратов относятся нуклеинат натрия и другие пуриновые и пирмидиновые основания: метацин, пентоксил, оротат калия и др.;
- улучшение обмена веществ в гепатоцитах. С этой целью целесообразно введение АТФ, коэнзима А, комплекса витаминов группы В, аскорбиновой кислоты, мексидола и др. Для нормализации сниженного уровня факторов свертывания крови, протромбинового комплекса обязательно введение викасола;
- применение анаболических гормонов. Дозы препаратов не должны быть большими, чтобы не вызвать срыва компенсаторных процессов в гепатоцитах. Следует предостеречь от применения гипербарической оксигенации, которая эффективна лишь после устранения желчной гипертензии. Для улучшения кровоснабжения паренхимы печени обязательно введение препаратов, улучшающих микроциркуляцию (реополиглюкина и др.);
- борьба с инфекцией. Введение антибактериальных препаратов у больных с длительной МЖ и сниженным вследствие этого иммунитетом должно сочетаться с проведением курса стимулирующей терапии продигиозаном, имунофаном или левамизолом.
Все существующие малоинвазивные методы декомпрессии билиарной системы можно разделить на две группы: эндоскопические (без нарушения целостности кожного покрова) и чрескожные. К первой группе относятся ЭРХПГ с ЭПСТ, назобилиарное дренирование, различные варианты эндопротезирования желчных путей. ЭРХПГ с ЭПСТ на протяжении многих лет остается основным методом эндоскопического лечения холедохолитиаза. Этот метод позволяет в 85-90% случаев удалять конкременты из общего желчного протока и восстанавливать желчеотток. ЭРХПГ дает возможность не только контрастировать протоки, но и визуально оценить состояние БДС, а также периампулярной области. С этой точки зрения возможности ЭРХПГ, безусловно, шире по сравнению с другими методами исследования желчевыводящих путей. При наличии крупных фиксированных камней по ходу магистральных желчных протоков к ретроградному контрастированию последних прибегать не следует, ограничившись проведением УЗИ или КТ. Ретроградное контрастирование в этом случае ведет к ухудшению состояния больного в связи с увеличением гипертензии во внутрипеченочных протоках, инфицированием и затрудненной эвакуацией контрастного вещества и желчи. В такой ситуации показана чрескожная чреспеченочная декомпрессия желчных путей. Если размер камня больше диаметра образованного устья общего желчного протока, прибегают к внутрипротоковому разрушению камня с помощью ретроградной механической литотрипсии. Эта методика, по данным многих зарубежных авторов, может быть признана высокоэффективной. Иногда ЭРХПГ с ЭПСТ недоступна — после резекции желудка по Бильрот-II, наличие крупных дивертикулов и непреодолимых препятствий в устье общего желчного протока.
Необходимость во временном эндопротезировании гепатикохоледоха и назобилиарном дренировании вызвана наличием у пациентов выраженной желтухи и холангита в условиях, когда санация гепатикохоледоха оказалась неполной и желчеотток не был окончательно восстановлен. Назобилиарное дренирование в этих случаях помимо желчеотведения позволяет также промывать желчные пути растворами антибиотиков, что способствует быстрой ликвидации холангита и дает возможность выполнять рентгеноконтрастные исследования для контроля за отхождением фрагментов разрушенного камня и мелких конкрементов.
Транспапиллярное эндопротезирование гепатикохоледоха нами выполняется в основном при опухолях панкреатобилиарной зоны, стриктурах. Для этой цели используются стандартные эндопротезы фирм «Olimpus» (Япония) и «Willson-Cook» (США), сроки функционирования которых составляют 4-5 месяцев. Перед эндопротезированием выполняется ЭПСТ в целях профилактики острого панкреатита, который может возникнуть при обтурации устья панкреатического протока концом эндопротеза.
Ко второй группе малоинвазивных методов декомпрессии желчных путей относят ЧЧХГ с ЧЧХС, чрескожную чреспеченочную холецистостомию под контролем УЗИ, КТ или лапароскопа. Несмотря на совершенствование УЗИ диагностики и КТ, объективная информация о патологии желчных протоков, достаточная для принятия решения о методе декомпрессии, может быть получена только при прямом контрастировании желчных путей. В последние 10 лет широкое распространение получили методы чрескожных чреспеченочных эндобилиарных вмешательств [2, 5, 7, 8, 10]. Их удается осуществить независимо от уровня и протяженности обтурации желчных путей. Осложнения и летальность при них составляют от 3 до 10%. На начальном этапе ЧЧХГ проводили в целях дифференциальной диагностики МЖ, определения уровня блока желчных протоков, решения вопроса о возможности выполнения наружного дренирования. Абсолютными противопоказаниями к ЧЧХГ мы считаем непереносимость контрастных препаратов и выраженные нарушения свертывающей системы крови.
С внедрением в клиническую практику УЗИ, КТ потребность в выполнении ЧЧХГ сократилась. В настоящее время мы выполняем ЧЧХГ у больных с незначительной дилятацией желчных протоков, а также при подозрении на доброкачественную стриктуру желчных протоков и вентильный камень дистального отдела гепатикохоледоха у пациентов, которым невозможно выполнить ЭРХПГ.
В последние годы наложение чрескожной чреспеченочной холецистостомы под контролем УЗИ, КТ или лапароскопа стало наиболее распространенным методом, позволяющим не только сразу установить характер и место обтурации желчных путей, но и осуществить их декомпрессию. Рентгенологический вид блока при заболеваниях, вызывающих обтурационную желтуху, не является строго специфичным, что может быть объяснено различной распространенностью процесса, наличием мелких включений, замазкоподобных масс и воспалительного отека. Противопоказания к чрескожным чреспеченочным вмешательствам — множественные метастазы в печень, крайне тяжелое состояние больных с некорригируемой ПН, выраженная гипокоагуляция с угрозой кровотечения.
Целесообразность применения каждого метода декомпрессии определяется несколькими факторами, основными из которых являются:
- информативность диагностической методики;
- возможность трансформации диагностической процедуры в эффективное лечебное вмешательство;
- безопасность метода (вероятность осложнений и степень их тяжести);
- ехническая сложность метода.
Преимущественное значение, определяющее лечебный результат, имеют два первых фактора.
С учетом накопленного нами опыта мы рекомендуем придерживаться следующей схемы лечебно-диагностических малоинвазивных инструментальных вмешательств при МЖ: клинико-лабораторные данные, УЗИ, КТ Ѓ ЭРХПГ или ЧЧХГЃ ЭПСТ или ЧЧХС или холецистостомия Ѓ лапаротомия.
Если возможности малоинвазивных методов декомпрессии желчных протоков исчерпаны или ограничены, то в срочном порядке больному показана лапаротомия с выполнением одного из методов интраоперационного желчеотведения.
Адекватность декомпрессии оценивается нами путем изучения функционального состояния печени и изменения пейзажа микрофлоры. О степени нарушения функционального состояния печени позволяют судить данные радиоизотопной гепатографии, антипириновой и биливердиновой проб, которые выявляют снижение поглотительно-выделительной и обезвреживающей функций печени, повышение уровня билирубина в крови. Для выявления степени инфицированности желчи и определения эффективности антибактериальной терапии проводится изучение микрофлоры и количественного бактериологического анализа желчи методом газовой хроматографии и масс-спектрометрии.
Таким образом, малоинвазивные эндоскопические и чрескожные чреспеченочные декомпрессионные вмешательства представляют собой эффективный способ восстановления желчеоттока при обструкции билиарной системы. Эти методики позволяют достаточно быстро и эффективно ликвидировать МЖ и холангит, дают возможность проводить хирургические вмешательства в наиболее благоприятных условиях, в плановом порядке, а у больных пожилого возраста с тяжелой сопутствующей патологией могут служить альтернативой хирургическому лечению. Эти вмешательства малотравматичны и сопровождаются небольшим числом осложнений. Применение этих методов позволяет значительно улучшить результаты лечения больных МЖ.
Литература
1. Данилов М. В., Глабай В. П., Кустов А. Е. и др. Хирургическое лечение больных механической желтухой опухолевой этиологии //Анналы хир. гепатологии. 1997. Т. 2. С. 110-116.
2. Ившин В. Г., Якунин А. Ю., Макаров Ю. И. Чрескожные чреспеченочные диагностические и лечебные вмешательства у больных с механической желтухой //Анналы хир. гепатологии. 1996. Т. 1. С. 121-131.
3. Каримов Ш. И. Эндобилиарные вмешательства в диагностике и лечении больных с механической желтухой. Ташкент: Издательство им. Ибн Сины, 1994. 239 с.
4. Прокубовский В. И., Капранов С. А. Чреспеченочное эндопротезирование желчных протоков //Хирургия. 1990. № 1. С.18-23.
5. Савельев В. С., Прокубовский В. И., Филимонов М. И. и др. Чрескожное чреспеченочное дренирование желчных путей при механической желтухе //Хирургия. 1988. № 1. С. 3-7.
6. Хрусталева М. В. Современные эндоскопические транспапиллярные методы лечения механической желтухи //Анналы НЦХ РАМН. 1997. С. 39-42.
7. Шаповальянц С. Г., Цкаев А. Ю., Грушко Г. В. Выбор метода декомпрессии желчных путей при механической желтухе //Анналы хир. гепатологии. 1997. Т. 2. С. 117-122.
8. Cotton P. B. Endoscopic management of biliary strictures //Annu gastrointes. endoscopy. 1993. P. 6.
9. Guschieri A., Buess G., Perissat J. Operative manual of endoscopic surgery //Springer-Verlag. 1993. V. 2. P. 273.
10. Murai R., Hashig Ch., Kusujama A. Percutaneus stenting for malignant biliary stenosis //Surgical endoscopy. 1991. V. 5. P. 140.
Обратите внимание!
- Механическая желтуха должна быть ликвидирована в течение первых 10 суток от момента возникновения в связи с угрозой развития холангита и печеночной недостаточности.
- Лечение больных механической желтухой должно быть комплексным.
- Лечение механической желтухи может быть более эффективным за счет применения малоинвазивных методов, основная цель которых — не только диагностика, но и лечение, проводимые одновременно.
- На первом этапе лечения необходимо осуществить временную декомпрессию желчных путей в качестве подготовки к основному (второму) этапу лечения; в ряде случаев эта процедура полностью заменит собой хирургическое лечение.
Источник