Пневмококковый менингит у детей последствия
Содержание статьи
Пневмококковый менингит — симптомы и лечение
Развитие менингита у ребенка всегда приводит любящих родителей в шоковое состояние и некоторую потерю «функций самосохранения», а ведь малейшее промедление может привести к серьезным последствиям и нередко к летальному исходу малыша. Одной из таких опасных форм заболевания является пневмококковый менингит. Это воспаление головного мозга имеет стремительный характер протекания, в результате чего статистика смертельных случаев выглядит угрожающе.
Понятие пневмококкового менингита
Пневмококковый менингит– опасное заболевание, связанное с воспалением головного мозга вследствие заражения человека возбудителями группы Streptococcus pneumonie. Опасность заболевания заключена в способах заражения, поскольку бактерии передаются от больных, которые являются носителями пневмококковой инфекции и пневмококка, воздушно-капельным путем. Сами же распространители, в  свою очередь, могут и не знать о своем заболевании.
свою очередь, могут и не знать о своем заболевании.
Пневмококковый менингит у детей развивается посредством заражения от носителя. Сегодня ученые предполагают, что каждый четвертый ребенок до 7 лет, а также каждый 5 взрослый является носителем бацилл. Внешне и внутренне они никак себя не проявляют до определенного момента. Если перенести стрессовую ситуацию или просто простудиться, можно активизировать деятельность возбудителя. В результате уже через несколько часов больной может страдать от симптомов в тяжелой форме его проявления. У новорожденных и грудных детей эта форма заболевания протекает молниеносно, что и влечет печальные последствия. Ребенок может умереть за несколько часов после проявления первых симптомов.
Согласно статистике пневмококковый менингит развивается в 3 случаев на 100 тыс. детей. При этом умирает каждый 10 заболевший малыш. Почему речь идет только о детях? Потому что больше всего заболеванию подвержены именно грудные дети или же дети старше 10 лет.
Группа риска к заражению пневмококкового менингита
Как уже упоминалось, заражению подвержены маленькие дети. Однако в группу риска включены все граждане любых возрастов, но с ослабленным иммунитетом.
Итак, в группе риска выделяют:
- Дети от полугода до 2 лет. Посредством наличия материнских антител в организме новорожденного его иммунитет имеет определенную защиту. В течение полугода со дня рождения дети утрачивают антитела, а соответственно их иммунитет уже не может защититься от проникшего возбудителя.
- Дети в возрасте от 10 лет и взрослые, у которых был зафиксирован иммунодефицит вследствие различных заболеваний.
- Возрастной иммунодефицит характеризуется группой лиц старше 65 лет.
- В группу риска попадают люди с наличием алкогольной зависимости, а также заядлые курильщики.
Проявление пневмококкового менингита может быть опасным вследствие его длительного инкубационного периода. Причем имеется характерное подразделение описываемого заболевания на две формы: первичный и вторичный. Первичная форма не выявляется путем стандартных бактериологических исследований: взяв посев с носовой или ротовой полости, обнаружения пневмококка не происходит. Это значит, что после событий, провоцирующих представленную форму заболевания, течение болезни будет очень тяжелым, а главное, может иметь стремительный характер и увеличивает вероятность летального исхода.
Симптоматика пневмококкового менингита
Пневмококковый менингит имеет следующие ярко выраженные симптомы:
- Головная боль и болевой синдром всех мышц тела.
- Судороги.
- Потеря сознания, бред больного и галлюцинации.
- По всему телу появляется геморрагическая сыпь, что впоследствии несколько затрудняет диагностику представленного заболевания.
- Нередко повышается температура тела до критических отметок.
- Наблюдается нарушение дыхания вплоть до приступов удушья.
Симптомы могут появиться неожиданно и стремительно наращивать темп проявления. В некоторых же случаях симптоматика имеет плавный и медленный характер течения, занимающего от 2 до 5 дней. Это приводит к длительному течению, а также увеличивает показатели вероятности смерти больного, поскольку необратимые последствия с воспалением головного мозга больше его же и разрушают.
Диагностирование заболевания зависит от той стадии, на которой больной поступил в клинику. Так, малышам проводят первичный осмотр с проведением своеобразного тестирования. Если положить больного на спину и поднять ему голову так, что подбородком он будет касаться груди, произойдет непроизвольное сгибание ног в коленных суставах. Самостоятельное разгибание в дальнейшем невозможно. Это первый признак воспаления головного мозга посредством развития пневмококкового менингита.
Лечение пневмококкового менингита
Лечение представленного заболевания проводится в строгом соответствии с предписаниями специалиста, а также в условиях реанимационного отделения. Здесь больному проводят люмбальную пункцию для выявления степени заболевания и определения возбудителя. После процедуры больной должен в течение 3 дней не вставать с постели и принимать соответствующее лечение. В некоторых случаях при тяжелых формах проявления заболевания потребуется подключение искусственной 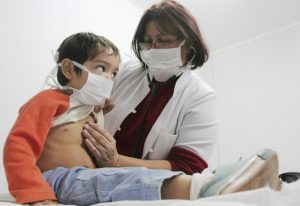 вентиляции легких.
вентиляции легких.
Пациент в зависимости от стадии заболевания подвергается:
- Патогенической терапии – назначаются лекарственные препараты, которые способны устранить и остановить интоксикацию, восстановить нормальное внутричерепное давление. При устранении интоксикации больной должен выпивать больше жидкости. Если больной находится без сознания, ему осуществляют внутривенное введение глюкозо-солевых растворов.
- Дегидратационную терапию – выведение жидкости из организма с целью нормализовать внутреннее черепное давление. Преимущественное назначение отводится препарату Лазикс, действие которого начинается через 3-5 минут после употребления.
- При дегидратационной терапии важно обеспечить больному хорошее кровоснабжение, для чего назначаются сосудистые средства.
Больному важно сохранять спокойствие, режим, правильное и рациональное питание. Все приведенные действия назначаются с целью предотвратить отек и кровоизлияние головного мозга.
Последствия пневмококкового менингита
Последствияперенесенного заболевания могут быть самыми необратимыми. Лишь в нескольких случаях больного беспокоят головные боли посредством смены атмосферного давления. В основном же последствия заключены в потере или нарушении слуха и зрения, снижении умственных способностей, а также нарушениях речи (заикание, полная потеря голоса). Также отмечается косоглазие и различные изменения психики.
Из представленного выше можно сделать один простой, но важный вывод: чем раньше обратиться к врачу за помощью, тем безопасней пройдет заболевание. При своевременном диагностировании заболевания последствий может быть значительно меньше и в незначительных проявлениях.
Источник
Пневмококковый менингит. Проблема высокой летальности | #05/13 | «Лечащий врач» – профессиональное медицинское издание для врачей. Научные статьи.
Пневмококковый менингит (ПМ) по данным бактериологических исследований занимает второе, после менингококкового менингита (ММ), место в этиологической структуре бактериальных гнойных менингитов (БГМ). Так, в РФ удельный вес ПМ среди других гнойных менингитов составляет 9,5–26%, в г. Москве за период 2005–2011 гг. — от 10,4% до 21% [1–5]. Учитывая то, что ПМ не входит в РФ в число инфекционных заболеваний, подлежащих официальной регистрации, а также то, что частота бактериологического подтверждения диагноза БГМ составляет по РФ от 16% до 38%, истинная заболеваемость и смертность, а также многие актуальные аспекты патогенеза, клиники и лечения ПМ изучены недостаточно [6–11].
ПМ отличается тяжелым течением, высокими показателями летальности, развитием осложнений, нередко приводящих к инвалидизации больных [4, 12–14]. Особенности ПМ обусловлены свойствами возбудителя и характером патологического процесса. Наиболее контрастно эти различия видны при сравнении с ММ. Основными факторами патогенности пневмококка являются капсула и тейхоевая кислота клеточной стенки. Капсула препятствует фагоцитозу, поэтому в патологическом материале пневмококк всегда располагается внеклеточно. Таким образом, при пневмококковой инфекции фагоцитоз не выполняет своей роли — самого раннего механизма защиты при бактериальных инфекциях. Тейхоевая кислота взаимодействует с С-реактивным белком и таким образом инициирует активацию системы комплемента и продукцию медиаторов острой фазы воспаления. Это сопровождается резким повышением сосудистой проницаемости и формированием экссудата с высоким содержанием фибриногена, который в результате активации системы гемостаза образует сгустки фибрина. В их толще пневмококк не доступен действию антител против антигенов его капсулы, которые являются основным фактором защиты при пневмококковой инфекции. При менингококковой инфекции капсула менингококка не препятствует его фагоцитозу, поэтому менингококк располагается внутриклеточно, в цитоплазме лейкоцитов, причем, как было установлено нами иммунофлюоресцентным методом на раннем этапе инфекции, при низком содержании липополисахарида (ЛПС) фагоцитоз является завершенным и только при потреблении миелопероксидазы лейкоцитов становится незавершенным, а при потреблении компонентов системы комплемента при фульминантных формах менингококковой инфекции вообще подавляется. Основной фактор патогенности менингококка — ЛПС — является мощным инициатором системного воспаления, обладает высокой фибринолитической активностью, поэтому значительного образования фибрина не происходит и менингококк более доступен действию факторов защиты и тяжесть течения инфекционного процесса в большей степени обусловлена токсикозом, вплоть до развития инфекционно-токсического шока (ИТШ) [14, 15]. В связи с подавлением фагоцитоза пневмококк из оболочек мозга рано проникает по периваскулярным пространствам в вещество мозга. Экссудат формируется непосредственно на поверхности мозга, и, в отличие от ММ, при ПМ уже в ранние сроки развивается картина менингоэнцефалита с выраженным отеком-набуханием головного мозга (ОНГМ), снижением мозгового кровотока и повреждением вещества мозга (рис. 1).
_575.jpg)
В то же время лихорадочно-интоксикационный синдром и поражение центральной нервной системы (ЦНС), свойственные менингококковой инфекции, при ПМ развиваются не столь бурно, как при ММ, примерно у половины больных развитию ПМ предшествует риносинусит, отит, пневмония, поэтому больные госпитализируются позже, что также отрицательно влияет на эффективность лечения. Так, при ММ больные госпитализируются в среднем через 1,7 ± 0,3 суток от начала болезни, при ПМ через 3,4 ± 0,4 суток (р < 0,01).
До разработки методов этиотропной терапии летальность при ММ была близка к 50%, а при ПМ составляла почти 100%, однако применение сульфаниламидов, а затем антибиотиков не привело при ПМ к столь впечатляющим, как при ММ, результатам. Показатели летальности при БГМ в зависимости от возраста пациента, клинических форм болезни и от этиологического агента в развитых странах составляют в среднем 3–19%, а в развивающихся — от 37% до 69%. По нашим данным (проанализированы 1876 историй болезни больных ММ и 384 истории болезни ПМ) за последние 40 лет летальность при ПМ снизилась с 27,6% до 17,9% за счет внедрения методов реанимации и интенсивной терапии. За тот же период времени летальность при ММ снизилась с 9,8% до 4,2%, однако при ММ летальность в основном связана с ИТШ, а менингит является причиной летальных исходов примерно у 1 из 10 умерших. При ПМ около 45% больным требуется оказание помощи в условиях отделения реанимации и интенсивной терапии [1, 16, 17].
Как уже говорилось, высокая летальность при ПМ обусловлена тяжестью поражения головного мозга, что видно при сравнении симптоматики с ММ в табл. 1.
.gif)
Важно отметить, что при ПМ пролонгированность общемозгового синдрома и очаговых симптомов была в несколько раз больше, а остаточные явления наблюдались у 20,4% больных, в виде парезов конечностей, нарушений психики и др. [5, 8, 13, 16]. Некоторыми существенными особенностями отличалась и картина спинномозговой жидкости (СМЖ). Так, при ПМ у 44,7% больных цитоз был менее 1000 в 1 мкл, то есть умеренный, часто нейтрофилы находились в состоянии распада. При ММ плеоцитоз менее 1000 в 1 мкл был у 21,4% (р < 0,001), причем главным образом за счет больных, поступивших в связи с развитием менингококкцемии в начальной стадии менингита. При слабо выраженной клеточной реакции при ПМ содержание белка составило 3,6 ± 0,5 г/л (при ММ 1,5 ± 0,4 г/л), что свидетельствует о резком повышении проницаемости гематоэнцефалического барьера. В периферической крови при ПМ также отмечалась более слабая клеточная реакция, лейкоцитоз в среднем был в 1 мл на 4 тыс. ниже, чем при ММ. При 2-значном плеоцитозе в СМЖ при ПМ и отсутствии лейкоцитоза в крови в 90% случаев исход был летальным. Несмотря на то, что в течение многих лет, включая 2012 г., от 95% до 100% ликворных штаммов пневмококка, выделенных у наблюдавшихся нами больных, сохраняют чувствительность к бензилпенициллину, цефтриаксону, фторхинолонам, ванкомицину, меропенему, линезолиду [13, 15, 16, 18], даже в благоприятно закончившихся случаях терапевтический эффект при ПМ достигался гораздо медленнее, чем при ММ, и, соответственно, продолжительность антибиотикотерапии составляла при ПМ 18,6 ± 1,2 суток, что почти в 2 раза больше, чем при ММ (10,2 ± 1,3 суток) (р < 0,001).
Основной причиной этих различий является низкая биодоступность возбудителя при ПМ, что подтверждается исследованиями динамики уровня лактата СМЖ, наиболее информативного показателя биологической активности возбудителя, так как лактат является продуктом анаэробного гликолиза [19, 20]. Данные об уровне лактата СМЖ у 28 больных ПМ и 50 больных ММ представлены на рис. 2.
.gif)
Как видно из рис. 2, при ПМ уровень лактата не снижается на 4–7 дни лечения, а на 2–3 неделе значительно превышает норму, в то время как при ММ наблюдается быстрое и резкое снижение уровня лактата и на 2–3 неделе он достигает референсного значения. Низкая доступность пневмококка обусловлена двумя факторами: 1) снижением мозгового кровотока в результате резко выраженного ОНГМ и уменьшения вследствие этого пассажа антибиотиков через гематоэнцефалический барьер, а также наличием зон бионедоступности возбудителя: очагов размягчения мозгового вещества, гематом, и особенно наличием фибринозно-гнойного экссудата на поверхности и в оболочках мозга, что хорошо подтверждается патоморфологическими данными (рис. 1) и исследованиями концентрации Д-димера фибрина (ДДФ) в СМЖ, который является основным продуктом фибринолиза и наиболее информативным показателем наличия фибринового сгустка в исследуемом субстрате [11, 21]. Результаты определения ДДФ в СМЖ у 28 больных ПМ и 49 больных ММ представлены на рис. 3.
При ПМ фибринолиз длительно находится на высоком уровне без тенденции к снижению, что говорит о сохранении большого количества фибрина в поздние сроки и хорошо соотносится с патоморфологической картиной ПМ. Следует также остановиться на значительном различии уровня летальности при симптоматическом лечении ММ и ПМ, что может быть связано с низкой эффективностью естественных факторов саногенеза. Как говорилось, при ПМ по сравнению с ММ имеет место более слабая лейкоцитарная реакция, отсутствует фагоцитоз. В отечественной и зарубежной литературе широко представлены работы об особенностях иммунопатогенеза БГМ [3, 10, 14, 22). Установленно значительное снижение фагоцитарной активности нейтрофилов, дефицит компонентов комплемента, клеток С0З+, С04+, С08+, что указывает на важную роль в патогенезе ПМ нарушения иммунного гомеостаза с депрессией местного и системного иммунитета. Нами исследованы показатели местного иммунитета в СМЖ. В табл. 2 представлены наиболее существенные различия показателей иммунитета у 22 больных ПМ и 36 больных ММ.
Как видно из табл. 1, при ПМ провоспалительная активность в СМЖ ниже. Снижение ИРИ за счет меньшей пролиферации Т-хелперов, снижения местной продукции иммуноглобулинов также может способствовать более тяжелому течению болезни. Представленные данные указывают на основные направления совершенствования терапии ПМ. Во-первых, учитывая низкую биодоступность возбудителя, следует использовать препараты, хорошо проникающие через гематоэнцефалический барьер (фторхинолоны, меропенем) или позволяющие использование сверхвысоких доз (бензилпенициллин до 500–1,0 мкл/кг массы, меропенем 6 г в сутки), при низкой проницаемости сочетать внутривенное и эндолюмбальное введение препарата (ванкомицин). Во-вторых, даже при отсутствии явного клинического эффекта не производить замены другим препаратом в течение 5–7 суток. Абсолютное показание для смены препарата — устойчивость к нему возбудителя, выявленная при определении чувствительности данного штамма возбудителя. В-третьих, при чувствительности возбудителя к применяемому препарату и отсутствии явного эффекта следует дополнительно назначить второй препарат из группы альтернативных или резервных препаратов. В-четвертых, отказаться от применения кортикостероидов, так как они снижают пассаж антибиотиков через гематоэнцефалический барьер. Важнейшее значение имеет раннее применение искусственной вентиляции легких до развития гипоксемии, по клиническим показаниям: глубокие расстройства сознания, судороги, снижение биоэлектрической активности мозга. Необходимо также применение препаратов, улучшающих мозговой кровоток (пентоксифиллин и др.). Необходимо проведение целенаправленных исследований о влиянии средств патогенетической терапии на проницаемость гематоэнцефалического барьера для антибиотиков, повышение биодоступности возбудителя, использование фибринолитиков, препаратов, активизирующих местные факторы саногенеза. Наконец, следует учитывать, что при наличии гнойного очага (отит, синусит и др.) необходима его экстренная хирургическая санация.
Литература
- Венгеров Ю. Я., Ченцов В. Б., Нагибина М. В. и соавт. Современные принципы диагностики и лечения больных БГМ // Consilium medicum. Хирургия (приложение), 2009, № 1, с. 26–38.
- Ералиева Л. Т. Ронколейкин в терапии гнойных бактериальных менингитов // Цитокины и воспаление. 2009, № 2, с. 11–19.
- Зенькова С. К., Семенов В. М., Скворцова В. В. Эпидемиологическая особенность гнойных менингитов и менингоэнцефалитов не менингококковой этиологии. В кн.: Актуальные аспекты военной медицины. Сб. научных трудов главного военно-медицинского клинического центра «ГВКГ» Украины. Киев, 2010, с. 147–152.
- Мартынова А. В., Туркутюков В. Б. Эпидемиологический анализ заболеваемости инвазивными и неинвазивными формами пневмококковых инфекций в различных группах населения // Вестник Российской АМН. 2007, № 9, с. 12–16.
- Kaplan S. L. Management of pneumococcal meningitis // Pediatr Infect Dis J. 2002. Vol. 21. № 6. P. 589–91; discussion P. 613–614.
- Белошицкий Г. В., Королева И. С., Кошкина Н. А. Менингиты пневмококковой этиологии в Российской Федерации. В кн.: Актуальные проблемы менингококковой инфекции и гнойных бактериальных менингитов. М., 2008, с. 15–16.
- Брико Н. И. Распространенность и возможности профилактики пневмококковой инфекции в мире и России. Бюллетень «Вакцинация». Пневмококковая инфекция. 2009, № 2.
- Шишов А. С., Григоревская У. Б., Гурьянов А. В. и др. Некоторые клинические особенности бактериальных инфекций с синдромом гнойного менингита // Журн. неврол. и психиат. 2011; 111: 4: 90–95.
- Tebruegge M., Curtis N. Epidemiology, etiology, pathogenesis, and diagnosis of recurrent bacterial meningitis // Clinical Microbiology Reviews. 2008, 21 (3): 519–537.
- Van de Beek D., de Gans J., Tunkel A. R., Wijdicks E. F. Community-acquired bacterial meningitis in adults // The New England Journal of Medicine. 2006, 354 (1): 44–53.
- Weisfelt M. et al. Procoagulant and fibrinolytic activity in cerebrospinal fluid from adults with bacterial meningitis // Journ. of Infection. 2007. Vol. 54, iss. 6. P. 545–550.
- Платонов А. Е., Николаев М. К. и др. Заболеваемость гнойными менингитами у детей в возрасте до 5 лет в регионах России // Жур. эпидемиология и инфекционные болезни. 2007, № 3, с. 11.
- Thabet F., Tilouche S., Tabarki B., Amri F. et al. Pneumococcal meningitis mortality in children. Prognostic factors in a series of 73 cases // Arch de Pediatric. 2007; 14: 334–337.
- Scheld W. M., Koedel U., Nathan B., Pfister H. W. Pathophysiology of bacterial meningitis: mechanisms of neuronal injury // J Infect Dis. 2002. Vol. 186. P. 225–533.
- Поздеев О. К. Медицинская микробиология / Под ред. В. И. Покровского. 2-е изд., испр. М.: Геотар-Мед. 2004, 768 с.
- Chavez-Bueno S., Mc. Cracken G. H. Bacterial meningitis in children // Pediatr. Clin. North Am. 2005. Vol. 52. P. 795–810.
- Pollard R. F., Pace D. Pneumococcal meningitis in children: prognostic indicators and outcome // Arch Dis Chil. 2007. Vol. 92. P. 909–915.
- Davis. L. E., Greenlee J. E. Pneumococcal meningitis: antibiotics essential but insufficient // Brain. 2003, May 1, 126 (5): 1013–1014.
- Венгеров Ю. Я., Нагибина М. В. и др. Клиническое значение лактат-ацидоза при гнойных менингитах // Клиническая медицина. 2008. Т. 86. № 10. С. 43–46.
- Венгеров Ю. Я., Нагибина М. В., Свистунова Т. С., Молотилова Т. Н. и др. Ликворологические исследования при нейроинфекциях. Материалы 1-го Всероссийского конгресса по инфекционным болезням «Инфекционные болезни» 2009, т. 7, пр. № 1, с. 41–42.
- Гильманов А. Ж. Д-димер: что? Как? У кого? С какой целью? // Клинико-лаб. консилиум. 2009. № 6 (31). С. 38–46.
- Лесков В. П., Чередееев А. Н., Горлина Н. К., Новоженов В. Г. В кн.: Клиническая иммунология для врачей. М., 2005. 144 с.
Ю. Я. Венгеров*, доктор медицинских наук, профессор
М. В. Нагибина*, кандидат медицинских наук
Е. П. Михалинова*
С. Е. Раздобарина*
Т. Н. Молотилова**, кандидат медицинских наук
Ю. Г. Пархоменко**, доктор медицинских наук, профессор
Н. В. Мозгалева**
Т. Ю. Смирнова**
Т. С. Свистунова**, кандидат медицинских наук
* ГБОУ ВПО МГМСУ им. А. И. Евдокимова МЗ РФ, ** ГКУЗ ИКБ № 2 ДЗМ, Москва
Контактная информация об авторах для переписки: infektor03@gmail.com
Источник