Оспа днк или рнк
еном вирусов оспы. Антигены вирусов оспы.
Геном вирусов оспы. Антигены вирусов оспы.Геном вирусов оспы представлен одной линейной молекулой двуцепочечной ДНК с ковалентно замкнутыми концами размером 130 тпн (парапоксвирусы) — 280 тпн (авипоксвирусы). На обоих концах генома имеются идентичные, но противоположно ориентированные тандемы повторяющихся нуклеотидных последовательностей. Геномы вирусов оспы способны кодировать около 200 белков, из которых не менее 100 входят в структуру вириона. Однако функциональные особенности определены лишь у небольшого количества вирусных белков. Наиболее важными из них являются ферменты, участвующие в синтезе вирусных нуклеиновых кислот и структурных компонентов вирионов. Например, синтез ДНК-полимеразы, ДНК-лигазы, РНК-полимеразы, энзимов, связанных с кэппированием и полиаденилированием мРНК и тимидинкиназы. Инфекционные вирусные частицы содержат системы транскрипции, которые могут выполнять in vitro синтез РНК, а также способны полиаденилировать, кэппировать и метилировать. В вирусных частицах содержится большое количество кодируемых вирусом энзимов и других биологически активных факторов. Некоторые гены вирусов оспы кодируют белки, которые секретируются инфицированными клетками и вызывают ответ организма на инфекцию, в том числе и формирование иммунитета. К таким вирокинам относятся гомологичный эпидермальный фактор роста, белок, снижающий активность комплемента, вирокины, обеспечивающие устойчивость к интерферону, и другие супрессоры иммунного ответа, подавляющие действие некоторых цитокинов организма хозяина. Вирусы оспы обычно характеризуются узким спектром хозяев. Они передаются чаще респираторным путем и реже через поврежденную кожу. Вирусы оспы овец, свиней, птиц и миксоматоза передаются также через укус членистоногими. Вирусы оспы устойчивы в окружающей среде и могут сохраняться годами в высохших струпьях кожи или других вируссодержащих материалах.
Большинство вирусов оспы хорошо размножаются в культуре клеток. Исключение составляют парапоксвирусы, вирус оспы свиней и вирус контагиозного моллюска. Однако они, так же как и ортопоксвирусы, легко образуют оспины на хориоал-лантоисной оболочке куриных эмбрионов. Вирусы оспы размножаются в цитоплазме, и, в отличие от других ДНК-вирусов, их размножение происходит независимо от ядра клетки, благодаря кодированию всех ферментов, необходимых для транскрипции и репликации вирусного генома. Некоторые из этих функций выполняются вирионами как таковыми. После слияния оболочки вириона с плазматической мембраной клетки или после эндоцитоза вирусная сердцевина освобождается в цитоплазму. Транскрипция вирусного генома характеризуется каскадностью, когда каждый временной класс генов («ранние», «промежуточные» и «поздние» гены) требует наличия специфических транскрипционных факторов, которые создаются предшествующим временным классом генов. Факторы, обеспечивающие транскрипцию промежуточных генов, кодируются ранними генами, тогда как факторы транскрипции поздних генов кодируются промежуточными генами. Транскрипция начинается вирионной транскриптазой и другими факторами, находящимися в сердцевине вириона, которые способны образовывать мРНК спустя минуты после инфицирования. Белки, образующиеся в результате трансляции этих мРНК, включая ДНК-полимеразу, тимидинкиназу и несколько других ферментов, необходимы для репликации вирусной ДНК. Репликация ДНК ВО связана с синтезом конкатемерных промежуточных структур, которые затем разрезаются с образованием единиц геномной длины. Детали этого процесса недостаточно изучены. С началом репликации ДНК происходит резкий сдвиг в генной экспрессии. Транскрипция «промежуточных» и «поздних» генов контролируется специфическими вирусными белками. Некоторые продукты транскрипции ранних генов образуются на поздней стадии инфекции, упаковываются в вири-оны и используются в следующем круге инфекции. Так как в состав вирусов оспы входит большое количество белков, не является неожиданным, что сборка вирионов есть комплексный процесс, который длится несколько часов и все еще целиком не выяснен. Образование вириона связано с вхождением ДНК внутрь незрелой сердцевинной структуры, которое затем завершается включением наружных покрывающих слоев. Репликация и сборка вирионов происходят в разных местах цитоплазмы в так называемых виропластах или вирусных фабриках. Вирионы выходят из клетки почкованием (оболочечные вирионы), или путем экзоцитоза, или при лизисе клеток (вирионы без оболочки). Большинство вирионов освобождаются при цитолизе и не имеют оболочки. Вирионы с оболочкой и без нее обладают инфекционностью, но первые, вероятно, играют более значительную роль в возникновении и распространении заболевания, а также в создании иммунитета. В очищенном вирусе осповакцины (ВОВ) выявлены белки с молекулярной массой 10-250 кД. Многие из них сосредоточены в сердцевине вириона. Два структурных гликопротеина располагаются между оболочкой и сердцевиной. В оболочке ВОВ содержится около 10 белков, из которых иммунологически наиболее активны крупномолекулярные белки с молекулярной массой 58—32 кД (VP4c, VP6a, VP6b и VP7a). Белок 32 кД определяет круг хозяев и важен для репликации вируса. В составе очищенного вируса оспы птиц обнаружено 29 полипептидов с молекулярной массой 14-138 кД. Наивысшей антигенной и иммуногенной активностью обладают полипептиды с молекулярной массой 35 и 37 кД. За индукцию вируснейтрализующих антител ВО ответственны антигены, расположенные на поверхности наружной оболочки вириона, и прежде всего белок 58 кД (VP4c), являющийся основным структурным компонентом трубочек (ворсинок). Антисыворотка к этому белку нейтрализовала инфекционность вируса и предотвращала образование синцития в культуре клеток. Этот белок ответственен за выработку иммунитета. Внеклеточные вирионы покрыты дополнительной наружной оболочкой, отсутствующей у внутриклеточных вирионов. Она играет важную роль в индукции синтеза ВН-антител. Инфекционность ВОВ и ВО крупного рогатого скота, имеющих наружную оболочку, нейтрализовалась антисывороткой к имеющему эту оболочку ВОВ, но не нейтрализовалась антисывороткой к ВОВ, лишенному наружной оболочки. За гемагглютинирующую активность ортопоксвирусов ответственны полипептид 85 кД и гликопротеид 41 кД. Во внеклеточном оболочечном ВОВ гемагглютинирующие свойства связаны с полипептидом 85 кД. Внутриклеточные вирионы (без дополнительной оболочки) практически не содержали этого полипептида. Неструктурный гемагглютинин формируется на цитоплазматических мембранах. С его образованием инфицированные клетки приобретают способность адсорбировать эритроциты. Вирусспецифические белки с молекулярной массой 32 и 37 кД, экспрессируемые на поверхности клеток, инфицированных ВОВ, делают их мишенями для специфических цитотоксических Т-лимфоцитов. МАТ-реактивные против каждого из пяти (54; 34; 32; 29 и 17—25 кД) белков наружного слоя поверхности вируса осповакцины нейтрализовали его инфекционность. В структуре полипептида 54 кД обнаружено два нейтрализующих эпитопа(Аи В). Анализ антигенных детерминант поверхностных полипептидов, проведенный с помощью МАТ, выявил в составе ортопоксвирусов, наряду с видоспецифическими, группоспецифические эпитопы. — Также рекомендуем «Оспа овец. Оспа птиц. Особенности оспы овец и птиц.» Оглавление темы «Частная вирусология.»: |
Источник
Как устроен вирус: типы, виды и строение вирусов, а также методы борьбы с ними

Вирусы у всех на слуху. С одними мы неизбежно сталкиваемся лично, например, с вирусами гриппа или теми, что вызывают простуду. Другие будоражат медицинское сообщество, наводняют новости и становятся зловещими прообразами для популярной литературы и кино.
И это неудивительно хотя бы потому, что вирусы — штука довольно непонятная. Неясно даже, считать их живыми или нет. С одной стороны, это просто хрупкий набор молекул, который не может существовать автономно, без живой клетки. Он не производит и не накапливает энергии, а также не поддерживает постоянства внутренней среды — ее попросту нет. Но когда вирус попадает в клетку, он проходит жизненный цикл, копирует себя и эволюционирует. Невидимое глазу нечто существует в огромном количестве, постоянно меняется, переходит от одних хозяев к другим и причиняет страдания разной степени тяжести всему человечеству.
Как устроены вирусы?
Вирусная частица, или вирион, — это нуклеиновая кислота (ДНК или РНК) в обертке из белков. В некоторых случаях она покрыта дополнительным слоем липидов, «украденных» у клетки-хозяина. У вирусов есть своя классификация: царства, семейства и прочие таксоны (группы), за списком которых следит Международный комитет по таксономии вирусов. Самый большой таксон — реалм. Сейчас ученые выделяют четыре реалма, из которых три — ДНК-содержащие вирусы. К ним относятся, например, вирусы оспы, герпеса и папилломавирусы.
РНК-содержащие вирусы можно разделить на собственно РНК-вирусы и ретровирусы. Первые — это вирусы гриппа, бешенства, гепатита С, а также коронавирусы и вирус Эбола. Они содержат РНК и используют для размножения РНК-зависимую РНК-полимеразу, с ее помощью на исходной молекуле РНК сразу синтезируется новая. А к ретровирусам относится, например, ВИЧ. Он содержит РНК, но в ходе жизненного цикла она превращается в ДНК и встраивается в геном клетки-хозяина. После чего новая РНК синтезируется уже на основе молекулы ДНК — то есть так же, как у нас.
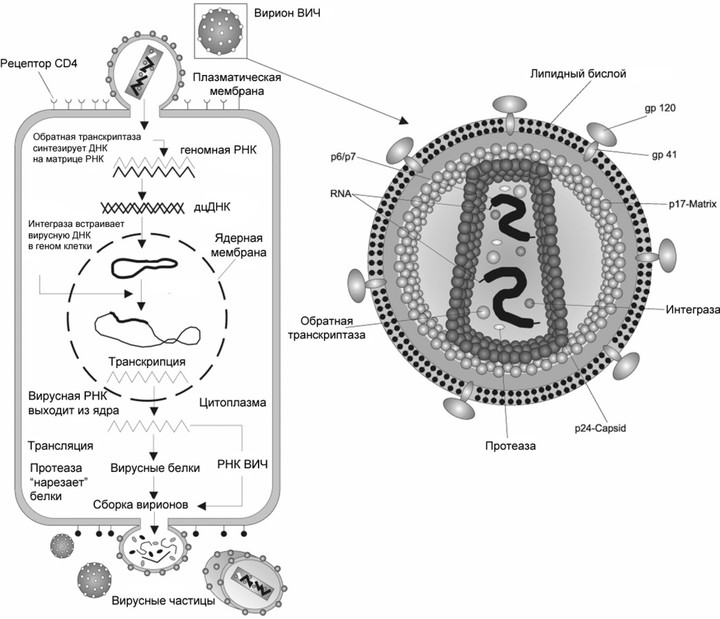 Жизненный цикл вируса, на примере вируса иммунодефицита
Жизненный цикл вируса, на примере вируса иммунодефицитаКак с ними бороться?
Можно выделить три стратегии борьбы с вирусами. Первая — «пожар проще предотвратить, чем потушить». Защититься от заражения можно по-разному, например, избегать незащищенного секса или контакта с зараженной кровью. Более изощренный способ — контроль природных резервуаров вируса: осушение болот (чтобы предотвратить вспышки желтой лихорадки), карантин, вакцинация или отстрел животных.
Еще одна стратегия — активная и пассивная иммунопрофилактика. Активная — это простая и всем знакомая вакцинация. Человеку вводят неактивную форму вируса или его кусочек, в организме срабатывает иммунный ответ и синтезируются антитела, которые защитят человека в будущем, если он когда-нибудь встретится с настоящим живым вирусом. Но вакцину не всегда можно создать, да и уже существующие порой не работают на все сто. Так, вакцина от гриппа защищает только от нескольких — самых распространенных в текущем сезоне — штаммов (видов) вируса. Пассивная иммунопрофилактика — это введение готовых антител тем, кто уже встретился с вирусом или с большой вероятностью сделает это. Такие лекарства существуют для респираторно-синцитиального вируса (рекомендованы недоношенным младенцам) и ветряной оспы (для людей с подавленным иммунитетом).
И, наконец, последняя стратегия на случай, если ничто не помогло и человек заболел, — антивирусные препараты. Их развитие подстегивали научный прогресс и насущные проблемы. Чтобы придумать противовирусный препарат, нужно сначала изучить вирус и его жизненный цикл и выбрать возможные мишени для атаки. Причем такие, чтобы они как можно сильнее отличались от человеческих аналогов. Иначе лекарство будет бороться и с вирусами, и с невинными человеческими клетками, вызывая сильные побочные эффекты.
Первые клеточные культуры, в которых можно было имитировать взаимодействие вируса с хозяином, появились в 1950-х годах. До этого удобных моделей in vitro (в пробирке) не существовало, и изучение вирусов было затруднено. Уже в 1963 году появился первый антивирусный препарат — идоксуридин. Это был нуклеозидный аналог дезоксиуридина — одного из четырех «кирпичиков» молекулы ДНК. Препарат до сих пор используется при лечении герпеса.
В 80-е произошло другое громкое открытие — вирус иммунодефицита человека. Это породило шквал научных работ, посвященных разработке новых противовирусных лекарств. К тому времени связанный с ним СПИД уже распространился по миру, а в США началась эпидемия.
Какие бывают антивирусные препараты?
Их можно разделить на 13 групп, причем к шести относятся различные лекарства против ВИЧ. Это ингибиторы входа вируса в клетку, вирусных ферментов интегразы и протеазы, а также три вида ингибиторов вирусного фермента обратной транскриптазы, или ревертазы. Все они действуют на разные этапы жизненного цикла вируса:
1. Проникновение в клетку
Это первое, что должен сделать вирус, попав в организм. То, какую клетку он поразит, определяется рецептором на ее поверхности. У ВИЧ это рецептор CD4, который есть у Т-хелперов, макрофагов, а также некоторых других видов клеток. Кроме него в связывании вируса и его проникновении участвуют: рецепторы CXCR4 и CCR5 со стороны клетки и поверхностные гликопротеины gp120 и gp41 — со стороны вируса.
Сейчас FDA (американское Управление по санитарному надзору за качеством пищевых продуктов и медикаментов) одобряет четыре лекарства, работающие на этой стадии. Каждый связывается с каким-то из участников процесса и мешает его работе. Например, к этой группе принадлежит самый новый препарат против ВИЧ — фостемсавир, его одобрили в США в июле 2020 года. В организме он превращается в активную форму темсавир, соединяется с вирусным гликопротеином gp120 и мешает ему связаться с клеточным рецептором CD4. Другой препарат — ибализумаб — связывается с самим CD4, причем так, что рецептор не может участвовать в проникновении вируса, но выполняет свою нормальную иммунную функцию — связывает и узнает антигены на поверхности антигенпрезентирующих клеток.
Подобные препараты также используются для лечения респираторно-синцитиального вируса, вирусов ветряной оспы и простого герпеса. Они тоже действуют на вирусные гликопротеины и их связывание с клеточными рецепторами. К этой же группе можно отнести препараты для пассивной иммунопрофилактики антителами.
2. Подготовка к размножению, часть 1
Когда вирус попал в клетку, он должен в ней размножиться, то есть создать копии себя, используя ресурсы самой клетки. Так как ВИЧ — ретровирус, его генетический материал — РНК, которая должна достроиться до двухцепочечной ДНК и встроиться в ДНК клетки. Процесс достраивания называется обратной транскрипцией, и для него необходим вирусный фермент обратная транскриптаза, ее еще называют ревертазой. Это самая популярная мишень препаратов против ВИЧ, которые делятся на две группы: нуклеозидные и ненуклеозидные.
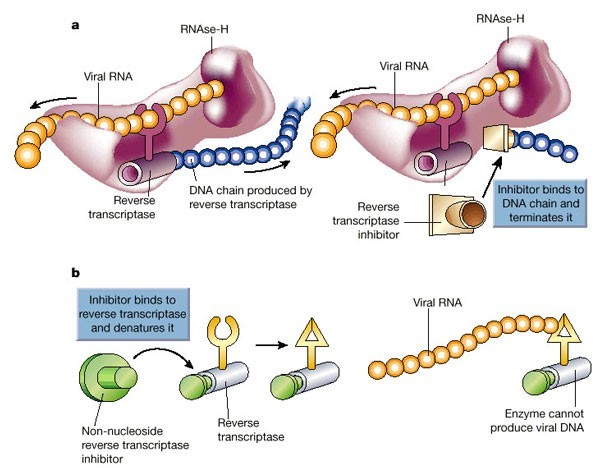 Механизм дейсвтия ингибиторов обратной транскриптазы
Механизм дейсвтия ингибиторов обратной транскриптазы3. Подготовка к размножению, часть 2
Чтобы наконец размножиться, ВИЧ, уже в виде молекулы ДНК, необходимо встроиться в геном клетки-хозяина. В этом участвует другой вирусный фермент — интеграза. Ее ингибируют несколько одобренных лекарств, причем они часто используются вместе с другим препаратом — кобицистатом. Он никак не действует на вирус, но ингибирует некоторые ферменты печени и увеличивает биодоступность самих антивирусных препаратов.
Попав в геном, вирус может запустить транскрипцию и синтезировать новые РНК и белки. А может и «заснуть». Именно поэтому ВИЧ почти нельзя вылечить: всегда останутся клетки со «спящим» вирусом, который себя не проявляет, а значит, не может быть мишенью для атаки. Активация вируса связана с активацией клетки. Так как ВИЧ инфицирует в основном иммунные клетки, именно те из них, что борются с инфекцией, и становятся его жертвой.
4. Созревание
Белки ВИЧ синтезируются в виде длинных полипротеинов, которые нужно «нарезать», чтобы получить зрелые формы. Для этого необходим вирусный фермент протеаза. Это — вторая по популярности мишень антивирусных препаратов. Большинство из них — белковые аналоги вирусного полипептида. Они ингибируют работу фермента, и зрелые вирусные белки и новые вирусные частицы не образуются. Подобно ингибиторам обратной транскриптазы, к препаратам из этой группы тоже очень быстро развивается резистентность. И, как и с ингибиторами вирусной интегразы, с ними часто используется кобицистат.
Препараты ингибирования вирусной протеазы также существуют для лечения вируса гепатита С. Несмотря на большие отличия в структуре и способе репликации, белки этого вируса тоже синтезируются в незрелой форме, которую нужно «нарезать».
Другие препараты
Есть три группы антивирусных препаратов, которые мы еще не упоминали. Во-первых, это ингибиторы белков NS5A и NS5B вируса гепатита С, которые играют важную роль в репликации РНК вируса. Во-вторых, лекарства против вируса гриппа: три ингибитора вирусного белка нейраминидазы и один ингибитор РНК-полимеразы вируса. И, наконец, сборная солянка препаратов, которые не действуют прицельно на вирусные компоненты. Это интерфероны, а также иммуностимуляторы и ингибиторы митоза клеток.
Первые заслуживают особого внимания из-за обилия отечественных лекарств против гриппа и простуды на их основе. FDA одобряет инъекции (!) интерферонов только для лечения гепатита B и С, причем на практике они используются очень осторожно из-за серьезных побочных эффектов. Отечественные противовирусные препараты с интерферонами, которые выпускаются в форме мазей, спреев и суппозиториев, вряд ли работают. И слава богу. Иммуностимуляторы и ингибиторы митоза клеток выпускаются в виде мазей и используются для лечения генитальных бородавок, то есть папилломавируса человека.
Наука не стоит на месте, и разработка противовирусных препаратов продолжается, подстегиваемая новыми вирусами, эпидемиями, а также развитием резистентности к существующим лекарствам. Но по-прежнему самыми изученными и многочисленными препаратами остаются ингибиторы вирусных обратной транскриптазы или ДНК-полимеразы и протеазы. Для разработки других стратегий борьбы ученым еще предстоит изучить детали работы вирусов — как давно известных, так и совершенно новых.
Да, вирусы остаются источником зловещих идей в популярной культуре. Но существующих препаратов и методов уже достаточно, чтобы мы могли избежать заражения, быстро вылечиться или свести негативные последствия болезни к нулю.
Источник