Обмен лактата в печени и мышцах цикл кори
Содержание статьи
Пути обмена лактата в печени и мышцах
Лактат не является конечным продуктом метаболизма. Дальнейшее использование лактата связано с его превращением в печени в пируват. Направление лактатдегидрогеназной реакции в работающих мышцах и печени обусловлено различным отношением концентраций восстановленной и окисленной форм NAD+ Отношение NAI+/NADH в сокращающейся мышце больше, чем в печени.
Цикл Кори (глюкозолактатный цикл) можно представить в виде последовательности событий (рис 9).
Цикл Кори. 1 — поступление лактата из сокращающейся мышцы с током крови в печень; 2,3- синтез глюкозы из лактата в печени; 4 — поступление глюкозы из печени с током крови в работающую мышцу; 5,6- использование глюкозы как энергетического субстрата сокращающейся мышцей и образование лактата.
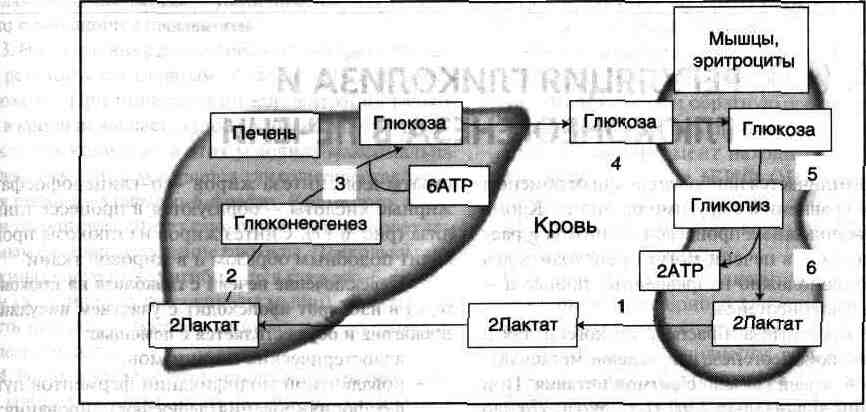
Рисунок 9
В мышцах пируват может превращаться также и в аланин. Аланин с кровью транспортируется в печень и там, теряя аминогруппу, превращается в пируват. Эта цепь превращений называетсяглюкозоаланиновым циклом.
Снижение использования лактата в качестве субстрата в синтезе глюкозы, вызванное дефектом ферментов глюконеогенеза, может приводит к повышению концентрации лактата и, следовательно, к понижению рН — лактатацидозу.
Синтез глюкозы в печени (глюконеогенез)
Глюконеогенез — это процесс синтеза глюкозы из веществ неуглеводной природы. У млекопитающих эту функцию выполняет в основном печень, в меньшей мере — почки и клетки слизистой кишечника. Главными субстратами глюконеогенеза являютсяпируват, лактат, глицерин, аминокислоты (рис.10).
Рисунок 10
Глюконеогенез обеспечивает потребности организма в глюкозе в тех случаях, когда диета содержит недостаточное количество углеводов (физическая нагрузка, голодание). Постоянное поступление глюкозы особенно необходимо для нервной системы и эритроцитов. При понижении концентрации глюкозы в крови ниже определенного критического уровня нарушается функционирование мозга; при тяжелой гипогликемии возникает коматозное состояние и может наступить летальный исход.
Запасов гликогена в организме достаточно для удовлетворения потребностей в глюкозе в период между приемами пищи. При углеводном или полном голодании, а также в условиях длительной физической работы концентрация глюкозы в крови поддерживается за счет глюконеогенеза. В этот процесс могут быть вовлечены вещества, которые способны превратиться в пируват или любой другой метаболит глюконеогенеза. На рисунке показаны пункты включения первичных субстратов в глюконеогенез:
Глюкоза необходима для жировой ткани как источник глицерола, входящего в состав глицеридов; она играет существенную роль в поддержании эффективных концентраций метаболитов цикла лимонной кислоты во многих тканях. Даже в условиях, когда большая часть потребностей организма в калориях обеспечивается за счет жира, всегда сохраняется определенная потребность в глюкозе. Кроме того, глюкоза служит единственным видом топлива для работы скелетной мышцы в анаэробных условиях. Она является предшественником молочного сахара (лактозы) в молочных железах и активно потребляется плодом в период развития. Механизм глюконеогенеза используется для удаления из крови продуктов тканевого метаболизма, например лактата, образующегося в мышцах и эритроцитах, глицерола, непрерывно образующегося в жировой ткани
Включение различных субстратов в глюконеогенез зависит от физиологического состояния организма. Лактат является продуктом анаэробного гликолиза в эритроцитах и работающих мышцах. Глицерин высвобождается при гидролизе жиров в жировой ткани в постабсорбтивный период или при физической нагрузке. Аминокислоты образуются в результате распада мышечных белков.
Рисунок 11. Глюконеогенез. Ферменты: 1- пируваткарбоксилаза, 2- фосфоенолпируваткарбоксикиназа, 3- фосфатаза фру-1,6-дифосфата, 4- глюкозо-6-фосфатаза. |
Семь реакций гликолиза легко обратимы и используются в глюконеогенезе. Но три киназные реакции необратимы и должны шунтироваться (рис. 12). Так, фруктозо-1,6-дифосфат и глюкозо-6-фосфат дефосфорилируются специфическими фосфатазами, а пируват фосфорилируется до образования фосфоенолпирувата посредством двух промежуточных стадий через оксалоацетат. Образование оксалоацетата катализируется пируваткарбоксилазой. Этот фермент содержит в качестве кофермента биотин. Оксалоацетат образуется в митохондриях, транспортируется в цитозоль и включается в глюконеогенез. Следует обратить внимание на то, что каждая из необратимых реакций гликолиза вместе с соответствующей ей необратимой реакцией глюконеогенеза составляют цикл, называемый субстратным:
Рисунок 12
Таких циклов существует три — соответственно трем необратимым реакциям. Эти циклы служат точками приложения регуляторных механизмов, в результате чего изменяется поток метаболитов либо по пути распада глюкозы, либо по пути ее синтеза.
Направление реакцийпервого субстратного цикла регулируется главным образом концентрацией глюкозы. При пищеварении концентрация глюкозы в крови повышается. Активность глюкокиназы в этих условиях максимальна. Вследствие этого ускоряется гликолитическая реакцияглюкоза глюкозо-6-фосфат. Кроме того, инсулин индуцирует синтез глюкокиназы и ускоряет тем самым фосфорилирование глюкозы. Поскольку глюкокиназа печени не ингибируется глюкозо-6-фосфатом (в отличие от гексокиназы мышц), то основная часть глюкозо-6-фосфата направляется по гликолитическому пути.
Превращение глюкозо-6-фосфата в глюкозу катализируется другой специфической фосфатазой-глюкозо-6-фосфатазой. Она присутствует в печени и почках, но отсутствует в мышцах и жировой ткани. Наличие этого фермента позволяет ткани поставлять глюкозу в кровь.
Распад гликогена с образованием глюкозо-1-фосфата осуществляется фосфорилазой. Синтез гликогена идет по совершенно другому пути, через образование уридиндифосфатглюкозы, и катализируетсягликогенсинтазой.
Второй субстратный цикл: превращение фруктозо-1,6-бисфосфата во фруктозо-6-фосфат, катализируется специфическим ферментом фруктозо-1,6-бисфосфатазой. Этот фермент имеется в печени и почках, он был также обнаружен в поперечнополосатых мышцах.
Направление реакцийвторого субстратного цикла зависит от активности фосфофруктокиназы и фосфатазы фруктозо-1,6-бисфосфата. Активность этих ферментов зависит от концентрации фруктозо-2,6-бисфосфата.
Фруктозо-2,6-бисфосфат образуется путем фосфорилирования фруктозо-6-фосфата при участии бифункционального фермента (БИФ), который катализирует также и обратную реакцию.
Киназная активность проявляется, когда бифункциональный фермент находится в дефосфорилированной форме (БИФ-ОН). Дефосфорилированная форма БИФ характерна для абсорбтивного периода, когда инсулин-глюкагоновый индекс высокий.
При низком инсулин-глюкагоновом индексе, характерном для периода длительного голодания, происходят фосфорилирование БИФ и проявление его фосфатазной активности, результатом чего являются снижение количества фруктозо-2,6-бисфосфата, замедление гликолиза и переключение на глюконеогенез.
Киназная и фосфатазная реакции катализируются разными активными центрами БИФ, но в каждом из двух состояний фермента — фосфорилиро-ванном и дефосфорилированном — один из активных центров ингибирован.
Третий субстратный цикл — между пируватом и фосфоенолпируватом.
В митохондриях имеется ферментпируваткарбоксилаза. который при участии АТР, биотина (витамина группы В) и СО2, превращает пируват в оксалоацетат. В цитозоле имеется второй фермент- фосфоенолпируваткарбоксикиназа, который катализирует превращение оксалоацетата в фосфоенолпируват.
Существенное препятствие, однако, заключается в том, что выход оксалоацетата из митохондрии весьма затруднен. Оно преодолевается следующим образом: оксалоацетат превращается в соединение, легко транспортирующееся из митохондрии во цитозоль, где это соединение снова превращается в оксалоацетат. Таким соединением служит малат или аспартат. В регуляциитретьего субстратного цикла основная роль принадлежит пируваткиназе, фосфорилированная форма которой неактивна, а дефосфорилированная активна. Реакции глюконеогенезапируват оксалоацетат фосфоенолпируват, однако, могут протекать при любых состояниях организма. Это объясняется необходимостью поддерживать концентрацию оксалоацетата на определенном уровне, потому что оксалоацетат используется не только в глюконеогенезе, но и в других процессах, таких, как цитратный цикл, трансмембранный перенос веществ, синтез аминокислот.
Суммарное уравнение глюконеогенеза из пирувата: 2 пируват + 4 ATP + 2 GTP + 2(NADH) + 4 Н2О Глюкоза + 4 ADP + 2 GDP + 2 NAD+ + 6 Н3РО4
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Источник
7.6. Цикл кори
Цикл Кори (глюкозо-лактатный цикл) открыла чешская ученая, лауреат Нобелевской премии Тереза Кори. Он представляет собой биохимический транспорт лактата из мышц в печень и дальнейший синтез глюкозы из лактата, катализируемый ферментами глюконеогенеза:
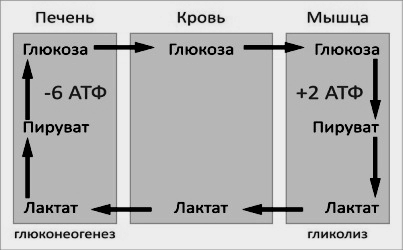
При интенсивной мышечной работе и в условиях отсутствия или недостаточного числа митохондрий (например, в эритроцитах) глюкоза подвергается анаэробному гликолизу с образованием лактата. При накоплении лактата в мышцах возникает лактат-ацидоз, раздражаются чувствительные нервные окончания, что вызывает боль в мышцах.
Лактат переносится кровью в печень и превращается в пируват, а затем в глюкозу (глюконеогенез), которая с током крови может возвращаться в работающую мышцу.
Направление лактатдегидрогеназной реакции в работающих мышцах и печени обусловлено отношением концентраций восстановленной и окисленной форм НАД+: отношение НАД+/НАДН в сокращающейся мышце больше, чем в печени.
7.7. Спиртовое брожение
Спиртовое брожение осуществляется дрожжеподобными организмами, а также некоторыми плесневыми грибками:
Механизм реакции близок к гликолизу. Расхождение начинается после этапа образования пирувата. При гликолизе пируват при участии фермента ЛДГ и кофермента НАДН восстанавливается в лактат. При спиртовом брожении пируват подвергается декарбоксилированию, в результате образуется ацетальдегид, а затем при восстановлении его — этанол:
При молочнокислом брожении ПВК не декарбоксилируется, а, как и при гликолизе в животных тканях, восстанавливается при участии ЛДГ за счет водорода НАДН.
7.8. Пентозофосфатный путь превращения глюкозы
Пентозофосфатный путь — альтернативный путь окисления глюкозы. Его функции:
— поставляет клеткам кофермент НАДФН, использующийся как донор водорода в реакциях восстановления;
— обеспечивает клетки пентозофосфатами для синтеза нуклеотидов и нуклеиновых кислот.
Пентозофосфатный путь не приводит к синтезу АТФ.
Ферменты пути локализованы в цитозоле.
В пентозофосфатном пути превращения глюкозы выделяют окислительный и неокислительный пути образования пентоз.
Окислительный путь включает две реакции дегидрирования. Коферментом дегидрогеназ является НАДФ+, восстанавливающийся в НАДФН. Пентозы образуются при окислительном декарбоксилировании.
Неокислительный путь включает реакции переноса 2- и 3-х углеродный фрагментов с одной молекулы на другую. Этот путь служит для синтеза пентоз. Процесс обратим, и из пентоз могут образовываться гексозы.
Пентозофосфатный путь образования пентоз протекает в печени, жировой ткани, молочной железе, коре надпочечников, эритроцитах.
1). Дегидрирование глюкозо-6-фосфата при участии глюкозо-6-фос-фатдегидрогеназы и кофермента НАДФ+ с образованием 6-фосфоглюконо--лактона и НАДФН:
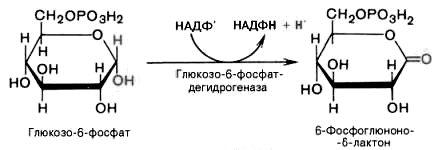
2). 6-фосфоглюконо--лактон нестабилен и гидролизуется с образованием 6-фосфоглюконата (фермент — 6-фосфоглюконолактоназа):
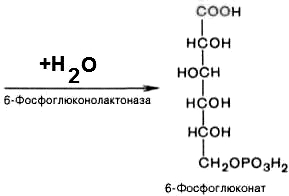
3). Дегидрирование и декарбоксилирование 6-фосфоглюконата с образованием рибулозо-5-фосфата (пентоза) и НАДФН при участии декарбоксилирующей 6-фосфоглюконатдегидрогеназы:
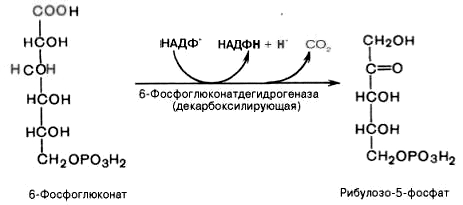
4). Под действием эпимеразы из рибулозо-5-фосфата образуется ксилулозо-5-фосфат (пентоза). Под влиянием изомеразы рибулозо-5-фосфат превращается в рибозо-5-фосфат (пентоза). Между формами пентозофосфатов устанавливается равновесие:
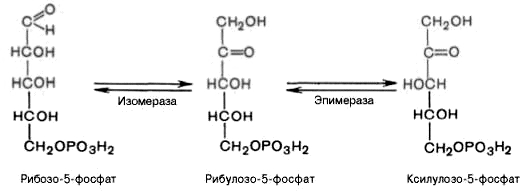
На этом этапе пентозофосфатный путь может быть завершен. При других условиях наступает неокислительная стадия пентозофосфатного цикла, протекающая в анаэробных условиях. Она заключается в переносе двух- и трехуглеродных фрагментов от одной молекулы к другой. При этом образуются вещества, характерные для гликолиза (фруктозо-6-фосфат, фруктозо-1,6-бисфосфат, фосфотриозы), и вещества, специфические для пентозофосфатного пути (седогептулозо-7-фосфат, пентозо-5-фосфаты, эритрозо-4-фосфат).
Шесть молекул глюкозо-6-фосфата в пентозофосфатном цикле образуют 6 молекул рибулозо-5-фосфата и 6 молекул СО2. Из 6 молекул рибулозо-5-фосфата регенерируется 5 молекул глюкозо-6-фосфата:
Промежуточные продукты цикла (фруктозо-6-фосфат и глицеральдегид-3-фосфат) включаются в гликолиз.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Источник
Цикл Кори — Cori cycle
Цикл Кори (также известный как цикл молочной кислоты ), названный в честь его первооткрывателей, Карла Фердинанда Кори и Герти Кори , представляет собой метаболический путь, в котором лактат вырабатывается анаэробным гликолизом в мышцах транспортируется в печень и превращается в глюкозу, которая затем возвращается в мышцы и циклически метаболизируется обратно в лактат.
Процесс
Мышечная активность требует АТФ , который обеспечивается расщеплением гликогена в скелете мышцы . Распад гликогена, известный как гликогенолиз , высвобождает глюкозу в форме глюкозо-1-фосфата (G1P). G1P превращается в G6P с помощью фосфоглюкомутазы . G6P легко вводится в гликолиз (или может переходить в пентозофосфатный путь , если концентрация G6P высока) процесс, который обеспечивает АТФ мышечными клетками в виде источник энергии. Во время мышечной активности необходимо постоянно пополнять запасы АТФ. Когда подача кислорода достаточна, эта энергия поступает от подачи пирувата , одного продукта гликолиза, в цикл лимонной кислоты .
. Когда подача кислорода недостаточна, обычно во время интенсивной мышечной активности энергия должна высвобождаться посредством анаэробного метаболизма . Молочнокислая ферментация превращает пируват в лактат с помощью лактатдегидрогеназы . Что наиболее важно, ферментация регенерирует NAD , поддерживая его концентрацию, поэтому могут происходить дополнительные реакции гликолиза. На стадии ферментации НАДН , полученный в результате гликолиза, окисляется обратно до НАД, передавая два электрона от НАДН для восстановления пирувата до лактата. (За подробностями обращайтесь к основным статьям по гликолизу и ферментации .)
Вместо того, чтобы накапливаться внутри мышечных клеток, лактат, произведенный анаэробной ферментацией, поглощается печень . Это инициирует вторую половину цикла Кори. В печени происходит глюконеогенез . С интуитивной точки зрения глюконеогенез обращает вспять как гликолиз, так и ферментацию, превращая лактат сначала в пируват, а затем обратно в глюкозу. Затем глюкоза поступает в мышцы через кровоток ; он готов к дальнейшим реакциям гликолиза. Если мышечная активность прекратилась, глюкоза используется для пополнения запасов гликогена посредством гликогенеза .
В целом на этапах гликолиза цикла вырабатываются 2 молекулы АТФ при затратах 6 молекул АТФ, потребляемых на этапах глюконеогенеза. Каждая итерация цикла должна поддерживаться чистым потреблением 4 молекул АТФ. В результате цикл не может продолжаться бесконечно. Интенсивное потребление молекул АТФ в цикле Кори сдвигает метаболическую нагрузку с мышц на печень.
Значение
Важность цикла основана на предотвращении лактоацидоза в мышцах в анаэробных условиях. Однако обычно, прежде чем это произойдет, молочная кислота перемещается из мышц в печень.
Цикл также важен для производства АТФ, источника энергии, во время мышечной активности. Цикл Кори функционирует более эффективно, когда мышечная активность прекращается. Это позволяет погашать кислородный долг, так что цикл лимонной кислоты и цепь переноса электронов могут производить энергию с максимальной эффективностью.
Цикл Кори является гораздо более важным источником субстрата для глюконеогенеза чем еда. Вклад лактата цикла Кори в общую продукцию глюкозы увеличивается с периодом голодания до выхода на плато. В частности, через 12, 20 и 40 часов голодания добровольцев-людей на глюконеогенез приходится 41%, 71% и 92% продукции глюкозы, но вклад лактата цикла Кори в глюконеогенез составляет 18%, 35% и 36%. % соответственно. Оставшееся производство глюкозы происходит за счет распада белка, мышечного гликогена и глицерина в результате липолиза .
Препарат метформин может вызывать лактоацидоз у пациентов с почечной недостаточностью потому что метформин ингибирует печеночный глюконеогенез цикла Кори, особенно комплекс 1 дыхательной цепи митохондрий. Накопление лактата и его субстратов для производства лактата, пирувата и аланина, приводит к избытку лактата. Обычно избыток лактата выводится почками, но у пациентов с почечной недостаточностью почки не могут справиться с избытком молочной кислоты.
См. Также
- цикл аланина
- цикл лимонной кислоты
Ссылки
- ^«Карл и Герти Кори и метаболизм углеводов» . Американское химическое общество. 2004. Проверено 12 мая 2020 г.
- ^Нельсон, Дэвид Л. и Кокс, Майкл М. (2005) Принципы биохимии Ленингера, четвертое издание. Нью-Йорк: W.H. Фримен и компания, стр. 543.
- ^ «Cori Cycle Архивировано 23 апреля 2008 г. на Wayback Machine «. Получено 3 мая 2008 г., из Элмхерста, стр. 1-3.
- ^Gerich JE, Meyer C, Woerle HJ, Stumvoll M (2001). «Почечный глюконеогенез: его значение в гомеостазе глюкозы человека» . Уход за диабетом . 24(2): 382-391 . doi : 10.2337 / diacare.24.2.382 . PMID11213896 .
- ^Nuttall FQ, Ngo A, Gannon MC (2008). «Регулирование выработки глюкозы в печени и роль глюконеогенеза у людей: постоянна ли скорость глюконеогенеза?» . Исследования и обзоры диабета / метаболизма. 24 (6): 438-458. doi : 10.1002 / dmrr.863 . PMID18561209 . S2CID24330397 .
- ^ Кац J, Tayek JA (1998). «Глюконеогенез и цикл Кори у людей, голодавших в течение 12, 20 и 40 часов» . Американский журнал физиологии . 275 (3 Pt 1): E537 — E542. doi : 10.1152 / ajpendo.1998.275.3.E537 . PMID9725823 .
- ^Кэхилл GF (2006). «Топливный обмен при голодании» (PDF). Ежегодный обзор питания . 26: 1-22. doi : 10.1146 / annurev.nutr.26.061505.111258 . PMID16848698 .
- ^Vecchio, S. et al. «Накопление метформина: лактоацидоз и высокие уровни метформина в плазме в серии ретроспективных клинических случаев у 66 пациентов, получающих хроническую терапию», Clin Toxicol. 2014; 52 (2).
- ^Сиртори С.Р., Пасик К. «Повторная оценка бигуанида, метформина: механизм действия и переносимость». Pharmacol Res 1994; 30.
Источники
- Smith, A.D., Datta, S.P., Smith, G. Howard, Campbell, P.N., Bentley, R., (Eds.) Et al. (1997) Oxford Dictionary of Biochemistry and Molecular Biology. Нью-Йорк: Oxford University Press.
Источник