Необратимо подавляет иммунную систему человека вирус гриппа оспы вич
Содержание статьи
Вирусы и иммунитет: кто кого?
Видео на конкурс «Био/Мол/Текст»: На фоне пандемии вырос интерес не только к научным данным, но и к альтернативной медицине и всяческим теориям заговора. Но некоторые из них не выдерживают даже проверки школьным учебником биологии.
Конкурс «Био/Мол/Текст»-2020/2021
Эта работа опубликована в номинации «Наглядно о ненаглядном» конкурса «Био/Мол/Текст»-2020/2021.
Генеральный партнер конкурса — ежегодная биотехнологическая конференция BiotechClub, организованная международной инновационной биотехнологической компанией BIOCAD.
Спонсор конкурса — компания SkyGen: передовой дистрибьютор продукции для life science на российском рынке.

Спонсор конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.

«Книжный» спонсор конкурса — «Альпина нон-фикшн»
Чтобы защитить нас от опасных заблуждений, давайте разберемся:
- как устроен вирус ;
- зачем вирусу попадать в организм человека;
- как иммунитет реагирует на вирусы;
- как медицина может помочь иммунитету, если сам он не справляется.
Видео. Вирусы и иммунитет: кто кого?
Как устроен вирус
Человек состоит из клеток, в которых очень важную роль играют белки. В ядре клетки хранится ДНК: все вы, наверное, видели картинки с этими переплетенными нитями из разноцветных кусочков.
Кусочки эти одинаковые у всех: и у людей, и у животных, и у растений, и у вирусов. Именно последовательность кусочков ДНК определяет особенности белков в нашем организме, а значит, влияет на наш внешний вид, работу органов и состояние здоровья.
Чтобы разобраться, как клетки производят белки, давайте представим следующее.
Допустим, вы производите посуду. Суперценный образец хранится в сейфе, и вы не готовы вынимать свой эталон из сейфа, даже чтобы сделать новый экземпляр. Поэтому специальный человек прямо в сейфе делает слепок кружки и приносит этот слепок рабочим, которые изготовят новую кружку по форме, получая от курьеров необходимые кусочки материала.

В ядре клетки, как в сейфе, хранится ДНК. С помощью белков-ферментов с ДНК снимается копия — информационная РНК. РНК попадает в рибосому, где начинается сборка белка. А транспортная РНК подносит фрагменты, из которых и собираются белки .

Так работает производство белка не только у человека, но и у многих других живых существ.
Все они адаптируются к среде, как могут, чтобы выжить и дать потомство. Человек тоже приспособился, и в этом ему сильно помог головной мозг. Он позволил ему придумывать приспособления для выживания и передавать информацию другим людям. Благодаря обмену знаниями и их накоплению человек может жить очень долго, потому что поселился в прочных зданиях, изобрел множество приспособлений и научился справляться с болезнями [1].
Раньше людям с рождения угрожали хищники, погодные катаклизмы, огромное количество вирусов и бактерий. Оспа, чума, грипп, малярия, бешенство, энцефалит, столбняк — люди умирали сотнями и тысячами и от эпидемий, и от банальных царапин. Но благодаря достижениям медицины мы научились лечить и предотвращать многие из них [2], [3].
Сейчас может показаться, что этих угроз вообще никогда не существовало. А если окажется, что они существуют до сих пор, очень хочется обвинить кого-нибудь в их создании, как будто они сами не могли появиться из природы. Но вообще-то могли.
Зачем вирусу попадать в организм человека
Вирус отличается от других живых организмов, потому что не питается, не выдает отходы жизнедеятельности, не стареет (вокруг вирусов до сих пор идет дискуссия, стоит ли их вообще считать формой жизни). Но, как и мы, вирус размножается и может умереть. Вирус похож на флешку: снаружи оболочка с шипиками-разъемами для подключения, а внутри информация (ДНК или РНК).
С помощью шипиков вирус пытается попасть внутрь клетки организма, как флешка пытается подключиться к компьютеру. Если все получилось, вирус забирается внутрь, раздевается и начинает диверсию [4].
Если у вируса внутри ДНК, он контрабандой доставляет ее в ядро, запускает копирование этой ДНК, создание РНК и далее по порядку. Если это РНК, он просто подменяет родную РНК клетки на свою [5].
В обоих случаях клетка делает белки не для себя, а для новеньких вирусов.
Когда клетка изжила весь свой ресурс, она лопается. Оттуда прут детки-вирусы, которые с помощью своих шипиков проникают в другие клетки, и процесс повторяется [6], [7].
Как иммунитет реагирует на вирусы
Итак, в организм ворвался чужак, использует наши клетки. Организм должен как-то отреагировать.
Иммунная система как раз отвечает за способность человека противостоять внешним угрозам. Как происходит иммунная реакция именно на вирусы?
Ключевые иммунные клетки — это фагоциты, B-лимфоциты , T-хелперы и T-киллеры.
Когда вирус попадает в клетку, та выставляет на поверхности сигнал о том, что она болеет. На этот сигнал тревоги приходят T-киллеры и фагоциты и пытаются уничтожить зараженные клетки и вирусы.

По пути фагоциты хватают сигнальную метку и передают ее T-хелперам. Это клетки-курьеры, которые отправляют полученный материал на изучение B-лимфоцитам. Они разрабатывают специальное оружие против вирусов и зараженных клеток — антитела. Антитела, как черная метка, цепляются за пораженную клетку, и T-киллеры могут быстрее ее обнаружить.
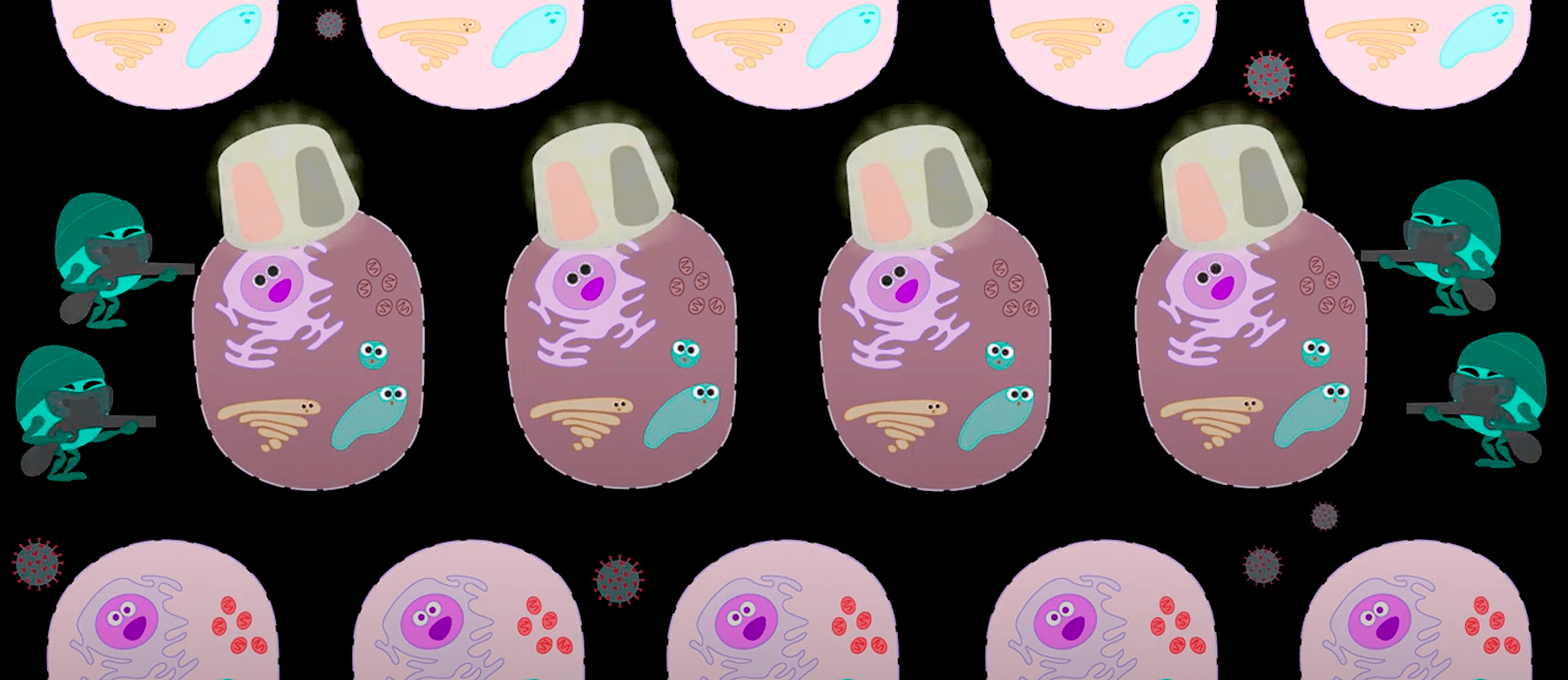
Если метка зацепилась за вирус, на сигнал приходит еще одно оружие — система комплемента, похожая на гранату, которая срабатывает, если два кусочка гранаты соединить вместе.
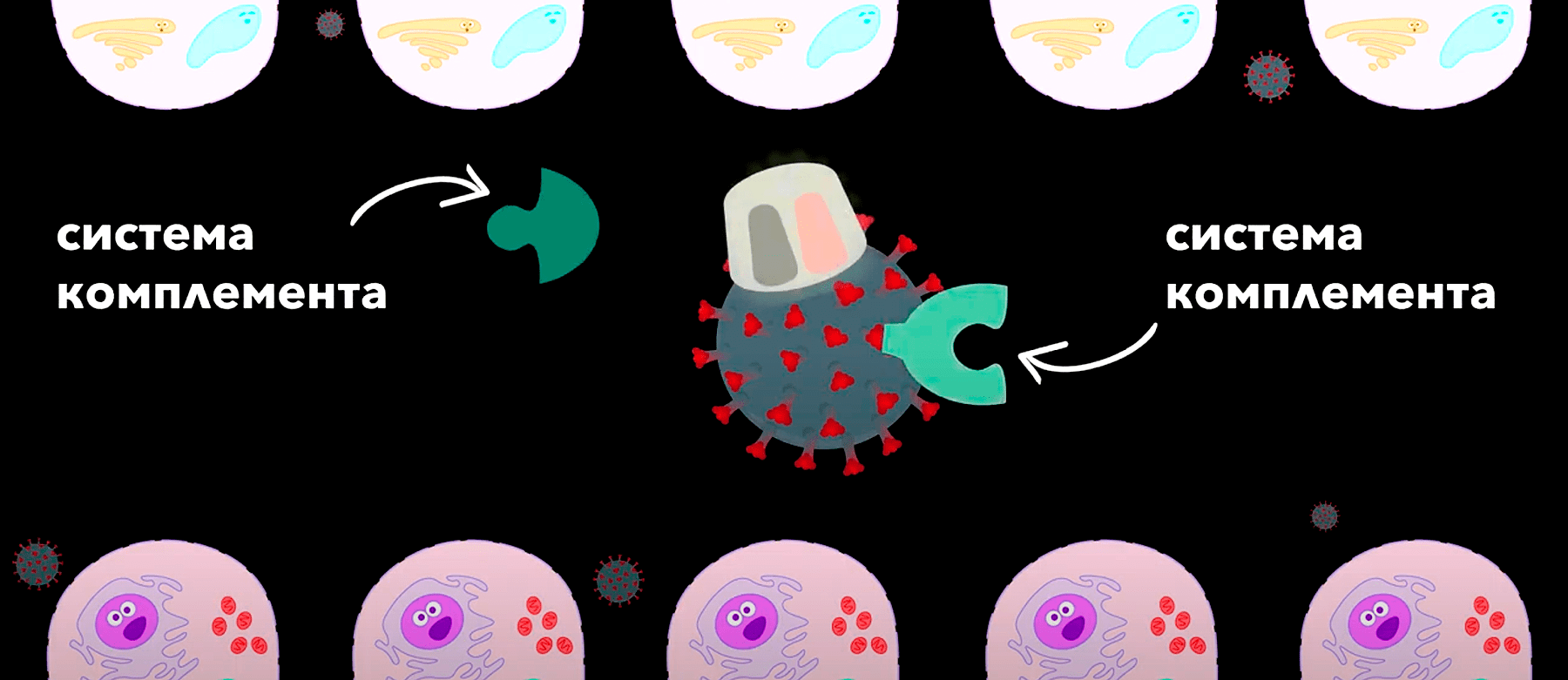
То есть антитела — это ускоритель иммунной реакции, который обращает внимание T-киллеров на зараженные клетки и подключает систему комплемента. Таким образом организм справляется гораздо быстрее и теряет меньше здоровых клеток.
Часть B-лимфоцитов, изучив вирус, вместо того чтобы создавать антитела прямо сейчас, остается с новыми знаниями про запас, на случай повторного заражения, и превращаются в клетки памяти. Если организм столкнется с вирусом еще раз, то просто активирует клетки памяти. И мы получим моментальные точные выстрелы снайперов и гранатометчиков [8], [9].

Пока вся эта канитель происходит, человеку может стать так плохо, что потребуется госпитализация или даже реанимация. Но накопленный опыт, технологии и медицина как-то должны помогать таким пациентам.
Как медицина может помочь иммунитету, если сам он не справляется
На каком этапе иммунной реакции человек может вмешаться?
Начнем с этапа, когда вирус пытается взломать клетку. У коронавируса есть ключики от слизистых: можно потрогать зараженный объект руками и перенести заразу себе, прикоснувшись к лицу. Носители могут чихнуть или кашлянуть на вас. Капельки слюны распыляются, когда вы разговариваете или смеетесь [10].
С руками все просто: можно смыть верхний слой кожного жира, на котором остаются вирусные частицы. А вот клетки слизистых надо как-то отгородить, например, маской . Но она не защищает глаза. Вирусы, попадая на маску, никуда не исчезают — они там копятся. Важно не занести их, когда вы будете поправлять или снимать маску. А самодельные тканевые маски могут быть бесполезны, если у них широкие поры.
Кардинальный метод защиты (и пока лучший) — уйти на карантин. Но в таком случае плохо становится не здоровью людей, а экономике.
Поможет ли молитва? Нет, клетки устроены одинаково и у церковнослужителя, и у бабули, и у знаменитости.
Поможет ли водка от вируса? Нет. Когда вы пьете алкоголь, вы не дезинфицируете организм, а ослабляете его. Так иммунным клеткам придется даже сложнее [12].
Чеснок, имбирь и другие чудеса народной медицины не работают антисептиком [11]. Чтобы разрушить вирусную частицу, нужен раствор с содержанием спирта не менее 60%, например, специальный антисептик для рук. Им логично протирать руки, поручни, дверные ручки и мобильные телефоны.
Допустим, попадание вируса в организм предотвратить не удалось. Начинается месиво: фагоциты и T-киллеры не справляются, B-лимфоциты стараются делать антитела и клетки памяти, пока вирус вовсю использует наши клетки. За это время человеку может стать очень плохо.
Можно ли помочь B-лимфоцитам? Да, можно еще до заражения ввести мертвый вирус, кусок вируса или подобие вируса, чтобы B-лимфоциты потренировались и заранее сделали антитела. Такой метод называется прививкой [13-16].
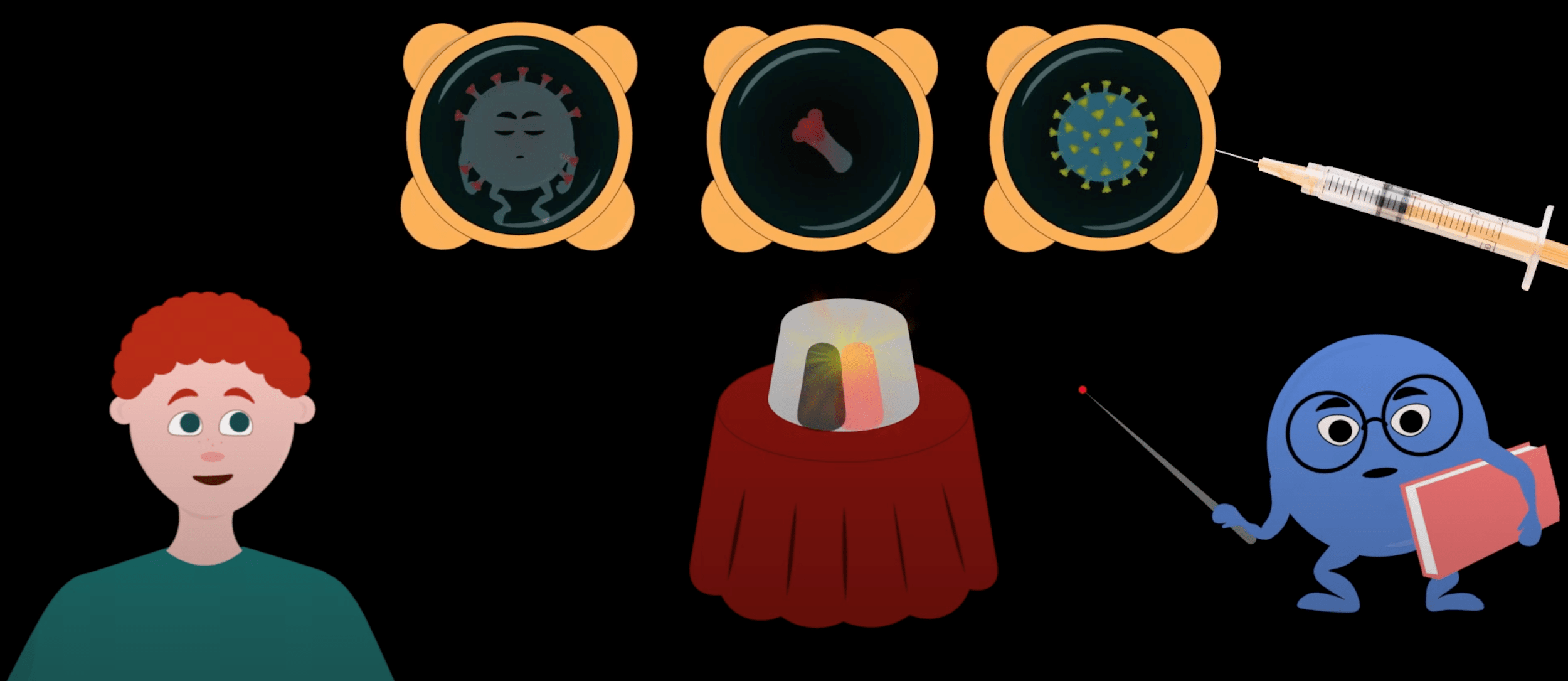
Еще можно поставить антитела «из-за рубежа». Когда B-лимфоциты не справляются, можно ввести в организм чужие антитела [17]. В некоторых больницах уже переливают плазму крови от тех, кто переболел, — пока это неофициальный метод («офф-лейбл») [18].

Создание лекарств занимает годы. Нужно найти действующее вещество, способ доставлять его в клетки, сделать из него препарат, который не испортится при хранении и не убьет побочными эффектами .
Если человеку стало очень плохо, нужно поддержать его организм, чтобы он выжил, пока побеждает вирус. Для этого людям нужны койки в больницах, аппараты ИВЛ и врачи. Но если инфекция быстро распространяется, много людей одновременно нуждаются в помощи.

Чтобы люди не умирали без помощи медиков, нужно искусственно замедлить скорость распространения вируса — сидеть дома. Чем больше людей игнорируют карантин, тем больше тех, кому не хватит медицинской помощи, а значит, будет больше смертей [18].
Если организм справился с инфекцией, у него появляются клетки памяти, поэтому он не будет носителем и не заразит других людей. Если клетки памяти будут у большинства, появится коллективный иммунитет. В таких условиях человек из группы риска вряд ли встретит носителя. Когда все носители переболеют, вирус среди людей не будет встречаться.

Некоторые страны уже снимают карантин. Но еще не понятно, есть ли коллективный иммунитет и не вызовет ли это новую волну заражений. В случае с коронавирусом пока неизвестно, сколько живут клетки памяти [19].
В России все еще каждый день заболевает по 8-10 тысяч человек. Возможно, в вашем регионе пандемия только набирает обороты . А значит, любой человек на улице может оказаться носителем.
В наших силах если не остановить, то хотя бы замедлить темпы, чтобы люди не умирали без помощи медиков.
Что же делать людям в борьбе с вирусом?
Защищаться мытьем рук и антисептиками? Искать вакцину или лекарство? Ждать, когда появится коллективный иммунитет? Или замедлять социальную активность, чтобы одновременно не заболело много людей? Сейчас мы делаем всё сразу.
Большинство стран мира следуют рекомендациям ВОЗ. Сайт этой организации переведен на русский язык. Там можно найти комментарии к мифам о коронавирусе и официальные рекомендации как для медиков, так и для населения. Если кто-то предлагает вам чудесное лекарство от болезни, проверьте, написали ли о нем эксперты ВОЗ.
- Харари Ю.Н. Sapiens. Краткая история человечества. М.: «Синдбад», 2016. — 570 с.;
- Коротяев А.И. и Бабичев С.А. Медицинская микробиология, иммунология и вирусология. СПб.: «СпецЛит», 2012. — 760 с.;
- История медицины. МГМСУ;
- Alexander Dömling, Li Gao. (2020). Chemistry and Biology of SARS-CoV-2. Chem. 6, 1283-1295;
- Калинин В.Л. Введение в молекулярную вирусологию. СПб.: Изд-во СПбГТУ, 2002. — 301 с.;
- Indwiani Astuti, Ysrafil. (2020). Severe Acute Respiratory Syndrome Coroirus 2 (SARS-CoV-2): An overview of viral structure and host response. Diabetes & bolic Syndrome: Clinical Re & Reviews. 14, 407-412;
- Pampel J. (2020). SARS-CoV-2 life cycle: stages and inhibition targets. antibodies-online network;
- How the body reacts to viruses. (2020). Harvard Medical School;
- Klimpel G.R. Immune defenses. In: Baron S. Medical microbiology (4th Edition). Galveston (TX): University of Texas Medical Branch at Galveston, 1996;
- COVID-19: отвечаем на вопросы;
- Рекомендации ВОЗ для населения в связи c распространением нового коронавируса (2019-nCoV): мифы и ложные представления. (2020). ВОЗ;
- Алкоголь и COVID-19: что нужно знать. (2020). ВОЗ;
- Зверев В.В. Вакцины и вакцинация: национальное руководство. Краткое издание. М.: «ГЭОТАР-Медиа», 2014. — 640 с.;
- Разработка вакцин: чем и как имитировать болезнь?;
- Мир до и после изобретения вакцин;
- История вакцинации;
- Saxena S.K. Coroirus disease 2019 (COVID-19). Springer Singapore, 2020;
- Временные рекомендации Минздрава по профилактике, диагностике и лечению новой коронавирусной инфекции (COVID-19). (2020). Минздрав РФ;
- Критерии для отмены режима изоляции в отношении пациентов с COVID-19. (2020). ВОЗ.
Источник
Научный журнал
Успехи современного естествознания
ISSN 1681-7494
«Перечень» ВАК
ИФ РИНЦ = 0,823
- Авторы
- Файлы
Сологуб Т.В. Ледванов М.Ю. Малый В.П. Стукова Н.Ю. Романцов М.Г. Бизенкова М.Н. Полякова Т.Д.
Взаимоотношения иммунитета и инфекции определяют развитие очень многих заболеваний. В полной мере сила и «разумность» инфекции проявляются в примере динамического противостояния живых систем — вирусной инфекции и иммунитета. Если вирус «спрятался» в клетках организма человека и заблокировал их апоптоз, то найти такую инфекцию и избавить организм от нее иммунная система может с помощью Т-клеток -киллеров. Они обнаруживают небольшие фрагменты вирусных белков, встроенных на поверхность инфицированной клетки. Задача Т-киллеров — выявить все инфицированные клетки и убить их путем апоптоза, чтобы не навредить соседним неинфицированным клеткам. Так и происходит в большинстве случаев, но когда Т-клетки-киллеры не обнаруживают признаков инфекции на поверхности инфицированных клеток и превращаются в бесполезное оружие иммунитета, на помощь приходят NK-клетки, имеющие точно такой же аппарат убийства других клеток, как и Т-киллеры. Такой иммунный контроль вирусной инфекции высокоэффективен.
Экспрессия генов ДНК-содержащих вирусов происходит в соответствии с центральной догмой молекулярной биологии: «ДНК — мРНК — белок». В процессе транскрипции участвуют вирусные и клеточные ферменты, как правило, неструктурные белки. По локализации ДНК-вирусы разделяются на ядерные (герпесвирусы, аденовирусы, паповавирусы) и цитоплазматические (вирус оспы). У некоторых из ядерных ДНК-вирусов (паповавирусы, герпесвирусы) возможна интеграция генома в клеточные хромосомы. У крупных ДНК-вирусов сначала синтезируется полицистронная РНК, которая затем нарезается и процессируется. У цитоплазматических ДНК-вирусов транскрипция осуществляется вирусными РНК-полимеразами.
У РНК-содержащих ретровирусов сначала происходит обратная транскрипция генома в ДНК, затем ее интеграция в клеточные хромосомы и лишь после этого транскрипция генов.
Цитопатические эффекты при вирусных инфекциях разнообразны, они определяются как вирусом, так и клеткой и сводятся к разрушению клетки (цитолитический эффект), сосуществованию вируса и клетки без гибели последней (латентная и персистирующая инфекция) и трансформации клетки.
Вовлеченность организма в инфекционный процесс зависит от ряда обстоятельств — количества погибших клеток, токсичности вирусов и продуктов распада клеток, от реакций организма, начиная от рефлекторных и заканчивая иммунными. Количество погибших клеток влияет на тяжесть инфекционного процесса. Например, будут ли поражены при гриппе только клетки носа и трахеи или вирус поразит клетки эпителия альвеол, зависит тяжесть и исход болезни.
Хотя вирусы и не образуют типичных токсинов, однако и вирионы, и вирусные компоненты, накапливающиеся в пораженных тканях, выходя в кровоток, оказывают токсическое действие. Неменьшее токсическое действие оказывают и продукты распада клеток. В этом случае действие вирусной инфекции столь же неспецифично, как и действие патогенных организмов, убивающих клетки и вызывающих их аутолиз. Поступление токсинов в кровь вызывает ответную реакцию — лихорадку, воспаление, иммунный ответ. Лихорадка является преимущественно рефлекторным ответом на поступление в кровь и воздействие на ЦНС токсичных веществ.
Если лихорадка — общий ответ организма на вирусную инфекцию, то воспаление — это местная многокомпонентная реакция. При воспалении происходят инфильтрация пораженных тканей макрофагами, утилизация продуктов распада, репарация и регенерация. Одновременно развиваются реакции клеточного и гуморального иммунитета. На ранних стадиях инфекции действуют неспецифические киллеры и антитела класса IgM. Затем вступают в действие основные факторы гуморального и клеточного иммунитета. Однако гораздо раньше, уже в первые часы после заражения, начинает действовать система интерферона, представляющая семейство секреторных белков, вырабатываемых клетками организма в ответ на вирусы и другие стимулы. Описанные явления относятся к так называемой острой репродуктивной вирусной инфекции. Взаимодействие вируса и клеток может происходить, как отмечалось выше, без гибели последних. В этом случае говорят о латентной, т.е. бессимптомной или персистирующей хронической вирусной инфекции. Дальнейшая экспрессия вируса, образование вирусспецифических белков и вирионов вызывает синтез антител, на этой стадии латентная инфекция переходит в персистирующую и появляются первые признаки болезни.
Репродукция вируса в клетках сопровождается развитием цитопатических процессов, специфичных для разных вирусов и для разных типов инфекционных процессов. Цитопатические процессы при вирусных инфекциях разнообразны, они определяются как вирусом, так и клетками, причем специфика их больше «задается» клеткой, нежели вирусом, и сводится в основном к разрушению клеток, сосуществованию вируса и клеток без гибели последних и трансформация клеток. Несмотря на значительные различия цитоцидного действия разных вирусов, в общем, они сходны. Подавление синтеза клеточных макромолекул — нуклеиновых кислот и белков, а также истощение энергетических ресурсов клетки ведут к необратимым процессам, заканчивающимся гибелью пораженной клетки. Повреждение клеток вирусами, их отмирание и распад переносят вирусную инфекцию с клеточного уровня на уровень организма в целом.
При встрече организма с вирусной инфекцией продукция интерферона (растворимого фактора, вырабатываемого вирус-инфицированными клетками, способного индуцировать антивирусный статус в неинфицированных клетках) становится наиболее быстрой реакцией на заражение, формируя защитный барьер на пути вирусов намного раньше специфических защитных реакций иммунитета, стимулируя клеточную резистентность, — делая клетки непригодными для размножения вирусов.
Продукция и секреция цитокинов относятся к самым ранним событиям, сопутствующим взаимодействию микроорганизмов с макрофагами. Этот ранний неспецифический ответ на инфекцию важен по нескольким причинам: он развивается очень быстро, поскольку не связан с необходимостью накопления клона клеток, отвечающих на конкретный антиген; ранний цитокиновый ответ влияет на последующий специфический иммунный ответ.
Интерферон активирует макрофаги, которые затем синтезируют интерферон-гамма, ИЛ-1, 2, 4, 6, ФНО, в результате макрофаги приобретают способность лизировать вирус-инфицированные клетки.
Интерферон-гамма является специализированным индуктором активации макрофагов, который способен индуцировать экспрессию более 100 разных генов в геноме макрофага.
Продуцентами этой молекулы являются активированные Т-лимфоциты (Тh2-тип) и естественные киллеры (NK-клетки). Интерферон-гамма индуцирует и стимулирует продукцию провоспалительных цитокинов (ФНО, ИЛ-1, 6), экспрессию на мембранах макрофагов, антигенов МНС II; гамма-интерферон резко усиливает антимикробную и противовоспалительную активность путем повышения продукции клетками супероксидных радикалов, а усиление иммунного фагоцитоза и антителоопосредованной цитотоксичности макрофагов под влиянием гамма-интерферона связано с усилением экспрессии Fc-рецепторов для JgG. Активирующее действие интерферона-гамма на макрофаги опосредовано индукцией секреции этими клетками ФНО -альфа. Этот пик наблюдается совместно с ФНО-альфа. Максимум продукции ИЛ-4 наступает через 24-48 ч с момента активации клеток. При этом ИЛ-4 рассматривается как цитокин, ограничивающий иммуновоспалительные реакции и снижающий ответ организма на инфекцию, угнетая при этом экспрессию гамма-интерферона. Интерферон-гамма ин витро усиливает фагоцитарную активность нейтрофилов, что обусловлено усилением экспрессии Fc-рецепторов и поверхностных белков семейства интегринов на нейтрофилы. Это позволяет нейтрофилам осуществлять цитотоксические функции и фагоцитоз. В качестве основных эффекторных клеток воспалительного процесса, они обеспечивают элиминацию инфекта из организма.
Взаимодействие цитокина с клеткой определяется универсальной биологической системой, специфическим механизмом которой является рецепторный аппарат, связанный с восприятием метаболического кода. Для проявления биологической активности цитокина необходимо присутствие на поверхности чувствительных клеток специфических рецепторов, которые могут экспрессироваться параллельно с синтезом цитокина. Рецепторы цитокинов представляют собой комплексы, состоящие из двух и более рецепторных молекул, которые объединяются на мембране клетки-мишени и образуют высокоаффинный рецепторный комплекс. Большинство рецепторов состоит из отдельных молекул, связывающих цитокины, которые ассоциируются после связывания лиганда с сигналпередающим рецепторным компонентом; часть рецепторов существует как растворимые изоформы, способные связывать и растворять цитокины, а часть функционирует как многокомпонентные блоки; механизм комплексирования субъединиц рецепторов объясняет плейотропные и дублирующие эффекты цитокинов, имеющих большое структурное сходство. Рецепторы ИЛ-10 имеют гомологию рецепторов интерферона, и подобно ИЛ-10 индуцирует экспрессию в моноцитах гена Fc- рецептора. Для полного функционирования цитокиновой системы необходимы повышение уровня цитокина в ответ на инфект и экспрессия нормального количества рецепторов к ним на клетках. Изменение рецепторов после их связывания с цитокином заключается в интернализации комплексов цитокин — рецептор внутрь клетки. На поверхности клеток рецептор появляется заново, постепенно синтезируясь в течение 24-36 ч (время появления рецепторов интерферон-альфа). В этот период клетки остаются чувствительными к последующим дозам цитокина, чем объясняется эффективность введения препаратов интерферона и их индукторов три раза в неделю.
Пик продукции цитокинов после стимуляции макрофагов наблюдается через 1-2,6,18-48 ч, а пик продукции интерферон-гамма наступает через 20 ч после первого выхода цитокина из клетки. Поскольку интерферон-гамма ингибирует миелопоэз, то нормализация числа нейтрофилов после элиминации инфекта связана с системой регуляции нейтропоэза. Через 6 ч после стимуляции интерферон-альфа для выполнения своих функций NK-rклетки (активность которых регулируется ИЛ-1, 4, 2) продуцируют гамма-интерферон, в результате чего происходит лизис инфицированных клеток.
При антигенной стимуляции клеток трансдукция сигнала с активированного рецептора на генетический аппарат осуществляется с помощью внутриклеточных регуляторных систем, компоненты которых (белки мембран, ферментов, хроматина) связываются с чувствительными к ним последовательностями ДНК. После связывания цитокина (интерферон) с поверхностными клеточными мембранными рецепторами происходит активация ферментов протеинкиназы-С (ПКС), тирозинкиназы, ц-АМФзависимой протеинкиназы, серин-треонинкиназы. Интерферон-альфа активирует tyk 2 и jak 1-киназы, а интерферон-гамма активирует jak 1 и 2-киназы. Далее факторы транскрипции перемещаются в ядро клетки и связывают гены раннего ответа.
Первый ответ клеток на цитокин — это быстрая индукция генов раннего ответа («imte early» генов), в число которых и входит ген интерферон-гамма. Стимуляция экспрессии этих генов важна для выхода клеток из Go-стадии и перехода в Gi-стадию и дальнейшей прогрессии клеточного цикла. Их индукция происходит после активации рецепторов роста на клеточной мембране и активации протеин-киназной системы. Гены раннего ответа являются ключевыми регуляторами клеточной пролиферации и дифференцировки, кодируют белки, регулирующие репликацию ДНК.
Таким образом, при активации клеток происходит стимуляция генов раннего ответа, что ассоциируется с изменением фаз клеточного цикла. Основная протективная роль в иммунном ответе, направленном против внутриклеточных паразитов (грибы, простейшие, вирусы, микобактерии туберкулеза), принадлежит клеточным механизмам. Способность перечисленных возбудителей переживать и размножаться внутри клеток делает их защищенными от действия антител и системы комплемента. Резистентность к антимикробным факторам макрофагов позволяет им длительно переживать внутри этих клеток. Для элиминации возбудителя необходим специфический клеточно-опосредованный ответ. Его специфичность определяется антигенраспознающими СД8+-Т-лимфоцитами, которые пролиферируют, активируются и формируют клон эффекторных цитотоксических лимфоцитов. Решающий момент специфического иммунного ответа — это ответ СД4+Т-лимфоцитов с хелперной направленностью на распознавание антигена. На этом этапе определяется форма иммунного ответа: либо с преобладанием гуморального иммунитета, либо с преобладанием клеточных реакций (ГЗТ). Направление дифференцировки СД4+-лимфоцитов, от которого зависит форма специфического иммунного ответа, контролируется цитокинами, образующимися в ходе воспалительной реакции. Так, в присутствии ИЛ-12 и интерферон-гамма СД4+-лимфоциты дифференцируются в воспалительные Тh2-клетки, начинают продуцировать и секретировать интерлейкин-2, интерферон-гамма, ФНО и определяют клеточный характер специфического иммунного ответа. Присутствие ИЛ-12 обеспечивается его продукцией макрофагами, а интерферон-гамма — естественными киллерами, активированными в раннюю фазу ответа на внутриклеточно паразитирующие бактерии и вирусы. В отличие от этого, в присутствии ИЛ-4 СД4+-лимфоциты дифференцируются в хелперы Тh 2, которые начинают продуцировать и секретировать ИЛ-4, ИЛ-5, ИЛ-6 и запускают гуморальный иммунный ответ, т.е. синтез специфических антител — иммуноглобулинов. Воспалительные Тh 1-лимфоциты нужны для борьбы с внутриклеточными паразитами, а Тh 2 хелперы нужны для элективной защиты от внеклеточных паразитов.
Вирусная инфекция может вызывать быстрое подавление экспрессии ряда клеточных генов (из которых наиболее изучены интерфероновые гены и гены, кодирующие дс-РНК-зависимые ферменты -2,5-ОАС и ПК-дс), принимающих участие в антивирусном действии. Специальные исследования механизма антивирусного действия интерферонов и дс-РНК в клеточных и бесклеточных системах показали ключевую роль в этом процессе вышеуказанных ферментов. ПК-дс, взаимодействуя с дс-РНК, фосфорилируется и в активной форме фосфорилирует регуляторные факторы транскрипции и трансляции, из которых наиболее изучен инициирующий фактор трансляции (eIF2).
ПК-дс выполняет регуляторную роль в системе клеточной пролиферации на уровне факторов трансляции и активации ряда генов цитокинов. Вероятно, существует связь между подавлением транскрипции мРНК и ПК-дс, угнетением общего синтеза клеточного белка при вирусных инфекциях и накоплением в ядрах клеток белка нуклеокапсида и белка NSP2. Фрагментация клеточных хромосом, наблюдающаяся на ранних сроках вирусной инфекции, может быть одной из причин подавления экспрессии генов, участвующих в противовирусном ответе.
Есть основания предполагать участие белков NSP2 в регуляции активности генов цитокинов — низкомолекулярных белковых регуляторных веществ, продуцируемых клетками и способных модулировать их функциональную активность. Нарушения в системе цитокинов приводят к нарушению кооперативных взаимодействий иммунокомпетентных клеток и нарушению иммунного гомеостаза.
В последние годы показано, что ИЛ- 12, относящийся к провоспалительным цитокинам, является ключевым для усиления клеточно-опосредованного иммунного ответа и инициации эффективной защиты против вирусов.
Средства терапии гриппа и ОРЗ можно разделить на этиотропные, иммунокорригирующие, патогенетические и симптоматические. Приоритет принадлежит этиотропным препаратам, действие которых направлено непосредственно на возбудитель инфекции. Все препараты этиотропного действия целесообразно рассматривать с учетом их точек приложения в цикле репродукции вирусов гриппа и других ОРЗ.
Применение химиопрепаратов для профилактики и лечения гриппа и ОРЗ относится к базовой терапии и является общепризнанным мировым стандартом. Многолетние клинические исследования достоверно выявили их высокую лечебно-профилактическую значимость. Химиотерапевтические средства представлены тремя основными группами: это блокаторы М2-каналов (амантадин, ремантадин); ингибиторы нейраминидазы (занамивир, озельтамивир) и ингибиторы протеаз (амбен, аминокапроновая кислота, трасилол). Препараты оказывают прямое антивирусное действие, нарушая различные фазы репликативного цикла вирусов. Несколько особняком стоит группа вирулицидных препаратов, применяемых местно для предотвращения адсорбции и проникновения вирионов в клетки.
СПИСОК ЛИТЕРАТУРЫ
- Грипп и другие респираторные вирусные инфекции / под ред. О.И. Киселева, И.Г. Мариничева, А.А. Сомининой. — СПб, 2003.
- Дриневский В.П., Осидак Л.В., Цыбалова Л.М. Острые респираторные инфекции у детей и подростков // Практическое руководство под редакцией О.И. Киселева. — СПб, 2003.
- Железникова Г.Ф., Иванова В.В., Монахова Н.Е. Варианты иммунопатогенеза острых инфекций у детей. СПб, 2007. — 254 с.
- Ершов Ф.И. Грипп и другие ОРВИ // Антивирусные препараты. Справочник. — М., 2006. — С.226-247.
- Ершов Ф.И., Романцов М.Г. Антивирусные средства в педиатрии. — М., 2005. — С.159-175.
- Ершов Ф.И., Киселев О.И. Интерфероны и их индукторы (от молекул до лекарств). М., 2005. — С.287-292.
- Иванова В.В. Острые респираторно-вирусные заболевания // Инфекционные болезни у детей. — М., 2002.
- Онищенко Г.Г., Киселев О.И., Соминина А.А. Усиление надзора и контроля за гриппом как важнейший элемент подготовки к сезонным эпидемиям и очередной пандемии. — М., 2004. — С.5-9.
- Об утверждении стандарта медицинской помощи больным гриппом, вызванным идентифицированным вирусом гриппа (грипп птиц) // Приказ Минздравсоцразвития №460 от 07.06.2006 г.
- Романцов М.Г., Ершов Ф.И.Часто болеющие дети: Современная фармакотерапия. — М., 2006. — 192 с.
- Стандартизированные принципы диагностики, лечения и экстренной профилактики гриппа и других острых респираторных инфекций у детей / под ред. О.И. Киселева. — Санкт-Петербург. — 2004. — С.82-95.
- Лекарственные средства в фармакотерапии патологии клетки / под ред. Т.Г.Кожока. — М., 2007.
Библиографическая ссылка
Сологуб Т.В., Ледванов М.Ю., Малый В.П., Стукова Н.Ю., Романцов М.Г., Бизенкова М.Н., Полякова Т.Д. ИММУННЫЙ ОТВЕТ ПРИ ВИРУСНЫХ ИНФЕКЦИЯХ // Успехи современного естествознания. — 2009. — № 12. — С. 29-33;
URL: https://natural-sciences.ru/ru/article/view?id=14061 (дата обращения: 01.07.2021).
Предлагаем вашему вниманию журналы, издающиеся в издательстве «Академия Естествознания»
(Высокий импакт-фактор РИНЦ, тематика журналов охватывает все научные направления)
Источник