Менингит у новорожденного недоношенного ребенка прогноз
Содержание статьи
сложнения острого бактериального менингита у новорожденного и детей
Осложнения острого бактериального менингита у новорожденного и детейа) Васкулит представляет собой компонент патологического комплекса гнойного менингита. Он может привести к тромбозу вен или мелких и изредка крупных артерий с вторичными некрозами (Taft et al., 1986). Локализация ишемических очагов непостоянная, от четко отграниченных участков до диффузных некротических поражений, способных вызывать мультикистозную энцефаломаляцию. Ишемические повреждения встречаются и без тромбозов сосудов. Воспаление сосудистых стенок капилляров ЦНС может позволить микроорганизмам проникнуть в паренхиму мозга с появлением небольших очагов септических некрозов. Вероятно, такие некрозы дают начало абсцессам мозга, которые в редких случаях осложняют бактериальный менингит. Васкулит шунтирующих вен также играет важную роль в генезе субдуральных кровоизлияний. Очаговая мозговая симптоматика, такая как гемиплегия или моноплегия, также являются следствием васкулита. Инфаркт в спинном мозге является необычным осложнением, связанным с вовлечением сосудов. Это было отмечено только в одном случае (Boothman et al., 1988). В случае появления двустороннего сенсорного или моторного дефицита в ходе течения бактериального менингита следует предположить инфаркт спинного мозга (Glista et al., 1980). Другие необычные неврологические симптомы включают в себя двигательные расстройства (Burstein и Breningstall, 1986), дисфункцию гипоталамуса и центральный несахарный диабет (Greger et al., 1986). Нейровизуализация позволяет тонкую оценку типа и локализации соответствующих поражений. Они обычно представлены участками пониженной плотности с периартериальной или более широкой локализацией. Некоторые поражения могут содержать геморрагический компонент. Очаговая мозговая симптоматика, такая как паралич III, VI или реже VII черепных нервов, встречается при пересечении воспаленных лептоменингеальных пространств. Такие параличи обычно возникают как следствие перенесенного менингита. Ранее сообщалось об опсоклонусе (Rivner et al., 1982). Припадки, которые встречаются у 30-40% детей, страдающих острым бактериальным менингитом, могут быть вторичными в связи с лихорадкой или возбуждением мозга при их генерализации и развитии на ранних стадиях заболевания. Парциальные припадки из-за локализованного поражения полушарий, как правило, развиваются в результате васкулита. В некоторых случаях развивается эпилептический статус, требующий незамедлительного лечения для предотвращения стойких повреждений.
небольшая левосторонняя субдуральная эмпиема и тромбоз заднего саггитального синуса. б) Субдуральные кровоизлияния все больше признаются в качестве осложнений острого бактериального менингита и встречаются у 20-50% больных детей, но обычно в виде ограниченного слоя и объема клинически они малозначимы (Syrogiannopoulos et al., 1986, Cabral et al., 1987). Большинство кровоизлияний локализуются с обеих сторон над лобно-теменными областями. Субдуральная жидкость редко содержит кровь, но имеет непропорционально высокое соотношение альбумина с глобулином (Rabe et al., 1968). Постоянная или рецидивирующая лихорадка, очаговая неврологическая симптоматика и устойчиво положительные культуры СМЖ, вероятно, более тесно связаны с повреждениями коры, чем с наличием кровоизлияний (Syrogiannopoulos et al., 1986; Snedeker et al., 1990). Массивные кровоизлияния, сопровождающиеся увеличением окружности головы или повышением ВЧД, встречаются редко, но требуют выполнения дренирования. Большинство субдуральных скоплений разрешается самостоятельно. Snedeker et al. (1990) обнаружили, что пациенты с кровоизлияниями более склонны к неврологическим расстройствам и судорогам на протяжении острого периода заболевания, но потеря слуха, приступы и задержка развития не встречались с большей частотой при последующем наблюдении. Субдуральная эмпиема является редкой (Jacobson и Farmer, 1981). Эмпиема часто характеризуется сохранением лихорадки и симптомов инфекции и признаков, связанных с очаговой симптоматикой, такой как судороги и гемиплегии. Диагноз устанавливается на основании методов нейровизуализации, которые показывают скопления вне ткани мозга с периферическим усилением сигнала. Диффузионно-взвешенные изображения (ДВИ) оказались эффективными для дифференциальной диагностики кровоизлияний и эмпиемы (Hunter и Morriss, 2003). в) Повышенное внутричерепное давление (ВЧД) тяжелой степени является серьезным осложнением бактериального менингита и может возникнуть в результате разных механизмов: гидроцефалия из-за измененной абсорбции СМЖ или нарушенного тока, или в связи с отеком ткани мозга. Острая гидроцефалия вызвана повышенной резистентностью к циркуляции и резорбции ликвора из-за наличия тонкого лептоменингеального экссудата в базальных цистернах или по конвекситальной поверхности мозга вблизи пахионовых грануляций, или вследствие вентрикулита с обструкцией водопровода. Это обычно преходящее явление, но может привести к возникновению поздней гидроцефалии, если разовьется обширный менингеальный фиброз. Отек мозга., очевидно, происходит в результате нескольких механизмов. Они включают в себя цитотоксический отек, ускоренный гибелью клеток из-за инфекции, вазогенный отек из-за увеличенной капиллярной проницаемости, связанной с воспалительным ответом на инфекционный процесс, и интерстициальный отек при нарушении обычной резорбции СМЖ. SIADH может встречаться с острым бактериальным менингитом (Kaplan и Feigin, 1978) и приводить к гипонатриемии и гипотонии внеклеточной жидкости, усугубляя отек мозга. Клинические проявления высокого ВЧД не всегда могут быть очевидны. Они включают снижение уровня сознания, головную боль и рвоту, напряжение родничка и расхождение швов, патологический зрачковый ответ и гипертензию с брадикардией (рефлекс Кушинга). Отек сосочка зрительного нерва встречается редко, особенно на ранних стадиях. Компьютерная томография может выявить исчезновение дифференцировки на серое и белое вещество, сдавление желудочков и борозд и уменьшенные базальные цистерны. МРТ может показать набухание извилин, а ДВИ поможет при различении цитотоксического отека (ограниченное распространение) от вазогенного отека. Мониторинг ВЧД может быть неотъемлемой частью лечения в случаях выраженной или устойчивой внутричерепной гипертензии (Goitein et al., 1983; Minns et al., 1989). Лечение заключается в фиксации головного конца кровати с подъемом, примерно на 30° и назначении маннитола или других гиперосмолярных веществ (для уменьшения цитотоксического отека). Более активные меры описаны в отдельной статье на сайте. Внутричерепная гипертензия связана с уменьшением мозговой перфузии и сниженной скоростью кровотока в мозге (McMenamin и Volpe, 1984), так что необходимо избегать даже незначительных эпизодов системной гипотонии, способных приводить к серьезным последствиям (Kaplan и Fishman, 1988). в) Вентрикулиты почти постоянно встречаются у новорожденных детей с менингитом, но сравнительно редки у детей старшего возраста. Когда вентрикулит сопровождается стенозом сильвиева водопровода, инфекция становится ограниченной (пиоцефалия) и может проявляться как абсцесс мозга. В большинстве случаев диагноз вентрикулита ставится по устойчиво положительным культурам ликвора с наличием или без клинических проявлений. Сканирование мозга может позволить определить вентрикулит с аномальным расширением желудочков мозга и отеком прилежащих перивентрикулярных областей белого вещества. В полостях желудочков может появляться взвесь (Fukui et al., 2001). Вентрикулит может отреагировать на высокие дозы парентеральных антибиотиков, но может потребоваться местное лечение и дренирование. При отсроченном лечении у выживших развивается склонность к гидроцефалии. Устойчивая лихорадка и другие септические осложнения являются результатом одновременной бактериемии. Они включают септический артрит, перикардит, пневмонию, эндофтальмит и гипопион (Kaplan и Fishman, 1988). Артрит, появляющийся через 5-7 дней антибиотикотерапии, вероятно, опосредован иммунными механизмами и часто реагирует на противовоспалительные средства (Rush et al., 1986). В тяжелых случаях могут наблюдаться гастроинтестинальное кровотечение, анемия и диссеминированное внутрисосудистое свертывание, особенно, но не исключительно при менингококковом менингите. В 13% случаев лихорадка продолжается 10 дней и более, особенно при пневмококковом менингите, и вторично рецидивирует у 16% пациентов (Lin et ah, 1984). Лихорадка может быть связана с сохранением очагов воспаления, поверхностным тромбофлебитом из-за внутривенных инфузий, нозокомиальных инфекций или септических или асептических абсцессов. Чаще всего причина не выявляется. В таких случаях показана люмбальная пункция. Если ребенок на вид здоров и показатели СМЖ приближаются к нормальным, антимикробная терапия может быть прекращена в обычные сроки.
преимущественно в субдуральном пространстве, у ребенка с пневмококковым менингитом. вентрикулит и вторичная гидроцефалия как осложнение двустороннего менингоэнцефалита. г) Неврологические осложнения. Неврологические осложнения затрагивают почти половину пациентов, перенесших менингит, и даже у лиц с нормальными познавательными способностями в сравнении с бывшим ранее качество жизни значительно снижается. Наиболее распространенными проблемами, наблюдающимися после менингита, являются трудности с обучением и нейромоторные расстройства, потеря слуха, эпилепсия, речевые и языковые проблемы, рубцы (особенно после менингококковой инфекции), нарушения зрения и заболевания глаз, и нарушения поведения. Результаты исследований сильно варьируют, также зависящие от этиологии микроорганизмов. Тяжелый дефицит обучения и нейромоторный дефицит обнаружены у 5-10% детей (Grimwood et ah, 1995, 2000; Bedford et ah, 2001), перенесших бактериальный менингит, немного хуже последствия среди новорожденных (11%) (Stevens et ah, 2003) и в развивающихся странах. Подавляющее большинство этих детей обучаются по специальным программам или посещают специальные школы. Эти дети с более высокой частотой осложнений имеют худший исход. Существуют некоторые расхождения между результатами различных исследований. Feldman и Michaels (1988) сообщили, что успехи в школьном обучении 10-12-летних детей после гемофильного менингита (Н. influenzae) не имели значимых отличий от их сибсов, не отмечено неспособности к обучению, дефицита внимания или поведенческих отклонений. Pomeroy et ah (1990) и Taylor et ah (1990) также обнаружили более низкий уровень стойких осложнений (всего примерно 14%) и лишь 1% и 4% пациентов соответственно стали тяжелыми инвалидами. Baraffet ah, (1993) проанализировали исходы у 4920 детей, перенесших менингит, в 45 опубликованных работах после 1955 г. Из этих детей 1602 ребенка были включены в 19 проспективных исследований, проведенных в развитых странах, у 4,2% были выявлены расстройства обучения или умственная отсталость; у 3,5% наблюдались мышечные спазмы или парезы; у 4,2% судороги; у 16,4% отмечался минимум один основной неблагоприятный исход, включая интеллектуальные осложнения, неврологический дефицит, судороги или глухоту. Различные возбудители были связаны с разными исходами; худшие исходы наблюдались у перенесших пневмококковый менингит, 15,3% развившихся осложнений по сравнению с 7,5% у детей с менингитами, вызванными N. meningitidis и 3,8% с H. influenzae. Grimwood et ah (1995) исследовали 158 детей, выживших после менингита в период между 1983 и 1986 годами (74% с H. influenzae тип В): в 8,5% случаев дефицит был значительным (IQ<70, судороги, гидроцефалия, спазмы, слепота или глубокая глухота), тогда как в 18,5% были незначительные изменения (трудности в школе, проблемы в поведении или снижение слуха) в сравнении с 10,8% в контрольной группе. Правда, течение заболевания в необычно высоком проценте случаев было осложнено (кома у 18,2%, судороги в 32% случаев, парез или гипотония отмечена у 10,7%). Нейросенсорная тугоухость среднетяжелой и тяжелой степени встречается у 10% детей с менингитом (Pomeroy et ah, 1990; Taylor et ah, 1990; BarafF et ah, 1993) и является двусторонней в 4-5% случаев. Потеря слуха, как полагают, развивается в результате лабиринтита, предположительно, в связи с распространением воспаления из субарахноидального пространства через водопровод улитки (Kaplan et ah, 1981;Eaveyetah, 1985).Риск развития глухоты повышается, если концентрация глюкозы в ликворе при госпитализации менее 1,1 ммоль/л (Dodge et ah, 1984), при судорогах наблюдавшихся до поступления и если стерилизация СМЖ запаздывает. Лечение цефуроксимом связано с задержкой стерилизации ликвора по сравнению с цефтриаксоном, и это могло повлиять на ранние испытания дексаметазона (Schaad et ah, 1990; van de Beek et ah, 2007). Глухота, видимо, появляется рано при менингите. Это трудно обнаружить клинически, поэтому систематическая оценка слуха должна проводиться до выписки из стационара по вызванной при аудиометрии реакции (Vienny et ah, 1984; Cohen et ah, 1988). Повторное обследование рекомендовано после выписки, если отклонения выявлялись при первоначальной оценке. Ранние вызванные реакции могут быть с временными изменениями примерно в 20% случаев, с восстановлением за 1-2 месяца (Vienny et al., 1984). Тугоухость не связана с возрастом пациентов и продолжительностью заболевания до госпитализации, таким образом, маловероятно ее предотвращение при постановке раннего диагноза. Использование дексаметазона в лечении уменьшает частоту нарушения слуха. Глухота чаще отмечается у детей с атаксией, но встречается и при ее отсутствии у большинства пациентов. Атаксия, по всей вероятности, имеет вестибулярное происхождение, хотя в некоторых случаях возможны дисфункции мозжечка (Kaplan et al., 1981). Практически все пациенты в состоянии компенсировать дефицит баланса за несколько недель и месяцев. Стойкая эпилепсия встречается у 2-5% пациентов (Pomeroy et al., 1990; Taylor et al., 1990; Baraff et al., 1993). Она может быть изолированной, но часто связана с трудностями в обучении и другими неврологическими осложнениями разной степени тяжести. Такие осложнения являются следствием паренхиматозных изменений в результате прямого или токсического воздействия патогенных микроорганизмов, васкулитов, и возможно, гипоксии и повышенного ВЧД. Хроническая гидроцефалия — нетипичное последствие острого детского бактериального менингита. Она вызывается менингеальным фиброзом базальных цистерн или конвекситальной поверхности мозга, или стенозом сильвиева водопровода в результате гранулематозного эпендиматита. Хроническая гидроцефалия может быть следствием ранней обструктивной гидроцефалии. Чаще всего она развивается незаметно, оставаясь нераспознанной в течение недель и месяцев. Поэтому после перенесенного менингита у новорожденных показано систематическое ультразвуковое обследование ЦНС, так как расширение желудочков может развиться задолго до увеличения окружности головы. Ведение на ранних стадиях осуществляется путем внешнего дренажа с последующим шунтированием. Другие неврологические осложнения включают гемиплегию, тетраплегию и слабость в конечностях, которые встречаются у 1 -4% пациентов. Слепота вследствие гнойного менингита развивается редко. Это может быть связано с внутриглазной патологией, с невритом глазного нерва или иметь кортикальное происхождение. — Также рекомендуем «Особенности менингита Neisseria meningitidis (менингококковый менингит) у новорожденного и детей» Редактор: Искандер Милевски. Дата публикации: 20.12.2018 |
Источник
собенности бактериального менингита у новорожденного ребенка
Особенности бактериального менингита у новорожденного ребенкаМенингит в первые 28 дней жизни во многом отличается от такового у старших детей; различаются не только микроорганизмы, но и характеристика головного мозга так же, как незрелость механизмов защиты против инфекции, что приводит к различной картине и исходам. В первую неделю жизни большинство случаев происходит при вертикальной передаче в первую очередь стрептококка группы В (42%), затем Е. coli (16%) (особенно К1 штаммы), энторовирусов (7%) и L. monocytogenes (3%). Менингит с более поздним началом может быть нозокомиальным или внебольничным, причиной которого могут быть другие грамотрицательные бактерии, такие как S. pneumoniae и Staphylococcus. Частота неонатального менингита в Великобритании около 0,21 на 1000 новорожденных, возрастающая среди недоношенных и детей с низкой массой при рождении и среди тех, у кого в анамнезе имеется длительный безводный период и пирексия у матери. Мальчики больше подвержены заболеванию, чем девочки, особенно при грамотрицительных инфекциях (Holt et al., 2001). У новорожденных диагностика не всегда проста и менингит должен быть заподозрен у любых детей грудного возраста с сонливостью и раздражительностью. Приступы апноэ, тошнота, небольшое повышение температуры тела и другие системные проявления, такие как желтуха и дыхательная недостаточность являются обычными, но неспецифичными. Судороги, обычно очагового типа, являются четким показанием для выполнения люмбальной пункции. Менингеальные признаки редки, а напряжение или выбухание родничка встречается менее, чем у трети пациентов. С учетом неспецифических особенностей, исследование СМЖ обязательно в каждом случае подозрения неонатальной инфекции. У новорожденных интерпретация результатов люмбальной пункции может быть сложной из-за характеристик ликвора в этом возрасте (Rodriguez et al., 1990). В одном исследовании (Bonadio et al, 1992) обнаружили, что у 31% младенцев в возрасте до 8 недель в ликворе больше 10 лейкоцитов/мм3 и только у 10% они отсутствуют. Большинство белых клеток были полиморфными. Уровень белка был в среднем 0,44 г/л у недоношенных новорожденных и известны случаи достижения уровня 1,5 г/л и выше. Низкий уровень глюкозы часто бывает у новорожденных, особенно в возрасте 4-8 недель. Кроме того, люмбальная пункция в этом возрасте травматична, и более чем у 4% новорожденных детей с менингитом, особенно у недоношенных, СМЖ при первом исследовании не изменена. Это подчеркивает необходимость проведения в сомнительных случаях повторной поясничной пункции через 6-12 часов после первой. Более 30% новорожденных со стрептококковым менингитом группы В в СМЖ имеют менее 30 белых кровяных клеток/мм3, что редко имеет место при эшерихиозном менингите. Однако Klein et al. (1986) сообщили, что менее, чем 1% пациентов имеют совершенно нормальный ликвор (включая количество клеток, белка и сахара). Существует несколько противопоказаний к спинномозговой пункции, даже у больных детей, у которых может использоваться изменение левой латеральной позиции со сгибанием бедер, но без сгибания шеи, что лучше переносится.
Кроме этого, присутствует небольшое скопление субдуральной жидкости с левой стороны и небольшое отклонение срединной линии. Начальное применение антибиотиков основывается на опыте, для большинства новорожденных используется комбинация третьего поколения цефалоспоринов, ампициллина (против листерий) и аминогликозидов. При подозрении на герпесный энцефалит добавляется ацикловир. После идентификации возбудителей и определения чувствительности к антибиотикам лечение может быть рационализировано. Стрептококковый менингит группы В эффективно лечится цефтриаксоном. Листериозный менингит реагирует на ампициллин отдельно или в сочетании с аминогликозидами, но не с цефалоспоринами (Kessler и Dajani, 1990), а грамотрицательные кишечные бактерии лучше лечить комбинацией цефалоспоринов и аминогликозидов. Интратекальное или внутрижелудочковое назначение антибиотиков уже давно не рекомендуется. Изучения длительности лечения не проводилось, но в настоящее время в Великобритании практикуется 2-3 недели; обычно две недели для стрептококкового менингита и три недели для Е. coli. Люмбальная пункция для подтверждения стерильности СМЖ рекомендована через 24-48 часов (Heath et al., 2003), а не в конце лечения (Schaad et al., 1981). Дополнительная терапия дексаметазоном не принесла дополнительного эффекта и в настоящее время не рекомендуется. Испытания с другими дополнительными препаратами (колониестимулирующий фактор гранулоцитов, эритропоэтин, IgG) пока еще не не выявили однозначных преимуществ. Нейровизуализация используется для определения осложнений менингита, таких как гидроцефалия, эмпиема, и мозговой абсцесс (сочетающихся, в частности, с Enterobacter sakazaki, Morganella morganii или Citrobacter koseri) (рис. 10.4). Ультразвук, КТ и MPT играют немаловажную роль в обследовании. Разделение мозговых желудочков, особенно на уровне отверстия Монро, может привести к ограниченной гидроцефалии (Kalsbeck et al., 1980), хотя более характерно развитие диффузной гидроцефалии из-за блокады цистерны. Для новорожденных с абсцессом мозга, особенно из-за Proteus или Citrobacter spp., обычно достаточно провести медикаментозное лечение. Дренирование больших полостей показано в случаях их увеличения и/или повышения ВЧД. Исход при неонатальном менингите гораздо хуже, чем при менингите у старших детей. Хотя смертность существенно снизилась за последние десять лет с примерно 24% до 6,6% (Holt et al., 2001), заболеваемость остается удручающе высокой с 10-кратным увеличением риска развития умеренной или тяжелой инвалидности вследствие неонатального менингита (Bedford et al., 2001). У более половины пострадавших новорожденных имеются некоторые расстройства, или интеллектуальные, или двигательные, нейросенсорная тугоухость или припадки. ЭЭГ может иметь прогностическую ценность, как медленные кривые имеют неблагоприятное значение (Chequer et al., 1992). Основой улучшения ситуации с неонатальным менингитом является профилактика с вакцинацией матери от стрептококка группы В и Е. coli, потенциально предупреждающей большинство случаев менингита новорожденных. У младенцев в возрасте от 28 дней до трех месяцев отмечается частичное «наложение» микроорганизмов, вызывающих неонатальный и детский менингит (Baumgartner et al., 1983). Тем не менее, возбудители детского менингита иногда являются причиной неонатального заболевания. — Также рекомендуем «Туберкулезный менингит у ребенка — клиника, диагностика. Эффективность БЦЖ» Редактор: Искандер Милевски. Дата публикации: 21.12.2018 |
Источник
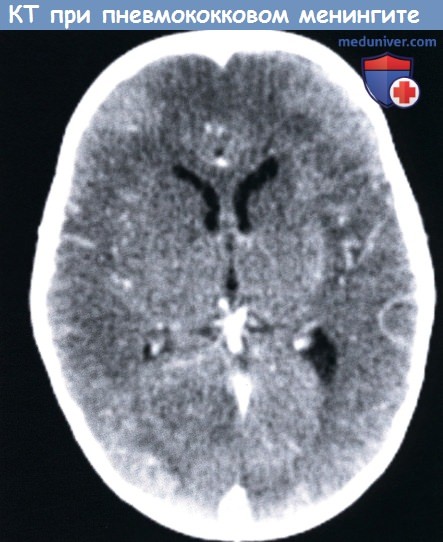 КТ с контрастным усилением у десятимесячного мальчика с пневмококковым менингитом: мозговой инфаркт вызванный васкулопатией,
КТ с контрастным усилением у десятимесячного мальчика с пневмококковым менингитом: мозговой инфаркт вызванный васкулопатией,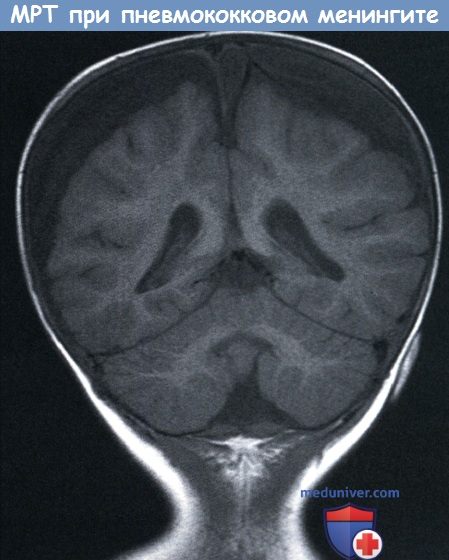 МРТ в Т1 -режиме: билатеральные значительные экстрааксиальные скопления,
МРТ в Т1 -режиме: билатеральные значительные экстрааксиальные скопления,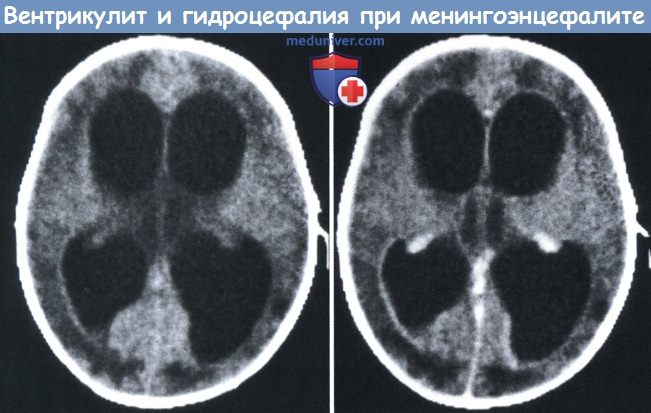 MPT до контрастирования (слева) и после контрастирования (справа):
MPT до контрастирования (слева) и после контрастирования (справа):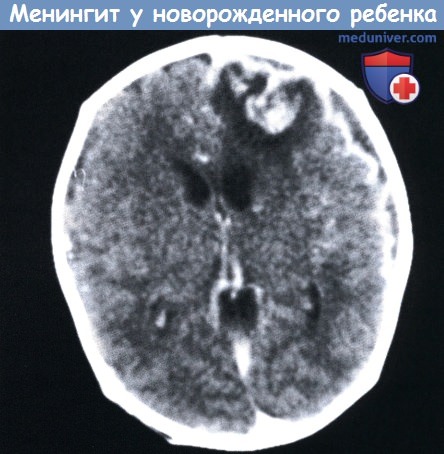 КТ с контрастным усилением четырехнедельного новорожденного с Salmonella менингитом: левостороннее усиление и лобно-париетальный инфаркт слева.
КТ с контрастным усилением четырехнедельного новорожденного с Salmonella менингитом: левостороннее усиление и лобно-париетальный инфаркт слева.