Эпидемиологический надзор за врожденной краснухой
Содержание статьи
МУ 3.1.2.2356-08 Эпидемиологический надзор за врожденной краснухой
МУ 3.1.2.2356-08
3.1.2. ПРОФИЛАКТИКА ИНФЕКЦИОННЫХ БОЛЕЗНЕЙ. ИНФЕКЦИИ ДЫХАТЕЛЬНЫХ ПУТЕЙ
Эпидемиологический надзор за врожденной краснухой
1. РАЗРАБОТАНЫ: Федеральной службой в сфере защиты прав потребителей и благополучия человека (Г.Ф.Лазикова, Е.Б.Ежлова); ФГУН «Московский научно-исследовательский институт эпидемиологии и микробиологии им. Г.Н.Габричевского» (Н.Т.Тихонова, А.Г.Герасимова, Т.А.Мамаева, О.В.Цвиркун, С.В.Шульга, О.О.Чава, Т.Н.Москалева, М.А.Наумова); Управлением Роспотребнадзора по г.Москве (И.Н.Лыткина, В.С.Петина).
2. РЕКОМЕНДОВАНЫ к утверждению Комиссией по государственному санитарно-эпидемиологическому нормированию при Федеральной службе по надзору в сфере защиты прав потребителей и благополучия человека (протокол от 3 апреля 2008 г. N 1).
3. УТВЕРЖДЕНЫ Руководителем Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека, Главным государственным санитарным врачом Российской Федерации Г.Г.Онищенко 25 апреля 2008 г. Введены в действие с 1 июля 2008 г.
1. Область применения
1.1. Настоящие методические указания (МУ) предназначены для специалистов органов и учреждений Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека, осуществляющих надзор за инфекционными заболеваниями, проведением иммунопрофилактики, соблюдением санитарно-противоэпидемического режима в лечебно-профилактических учреждениях, и могут быть использованы учреждениями здравоохранения, а также лечебно-профилактическими учреждениями независимо от организационно-правовой формы.
1.2. В методических указаниях изложены основные принципы организации и осуществления эпидемиологического надзора за врожденной краснухой (ВКИ — врожденной краснушной инфекцией и СВК — синдромом врожденной краснухи) с целью предупреждения рождения детей с врожденными аномалиями, обусловленными вирусом краснухи.
2. Нормативные и методические ссылки
2.3. Основы законодательства Российской Федерации об охране здоровья граждан от 22.07.93 N 5487-1 (в ред. Федеральных законов от 02.03.98 N 30-ФЗ, от 20.12.99 N 214-ФЗ, от 02.12.00 N 139-ФЗ, от 10.01.03 N 15-ФЗ, от 27.02.03 N 29-ФЗ, от 30.06.03 N 86-ФЗ, от 29.06.04 N 58-ФЗ, от 22.08.04 N 122-ФЗ (ред. 29.12.04), от 01.12.04 N 151-ФЗ, от 07.03.05 N 15-ФЗ, от 21.12.05 N 170-ФЗ, от 31.12.05 N 199-ФЗ, от 02.02.06 N 23-ФЗ, от 29.12.06 N 258-ФЗ, с изм., внесенными Указом Президента РФ от 24.12.93 N 2288).
2.5. СП 1.1.1058-01 «Организация и проведение производственного контроля за соблюдением санитарных правил и выполнением санитарно-противоэпидемических (профилактических) мероприятий».
2.6. СП 3.1.2.1176-02 «Профилактика кори, краснухи и эпидемического паротита».
2.7. СП 3.1/3.2.1379-03 «Общие требования по профилактике инфекционных и паразитарных болезней».
2.11. МУ 3.1.2.1177-02 «Эпидемиологический надзор за корью, краснухой и эпидемическим паротитом».
3. Общие положения
Краснуха — повсеместно распространенное вирусное инфекционное заболевание, передающееся воздушно-капельным путем, протекающее, как правило, в легкой, иногда бессимптомной форме. Возбудителем краснухи является РНК-вирус — единственный представитель рода Rubovirus семейства Togaviridae.
Медицинская и социальная значимость краснухи обусловлена, прежде всего, тератогенным действием вируса краснухи. Благодаря небольшим размерам вирус способен проникать через плаценту, что приводит к инфицированию плода и, в зависимости от срока беременности, может привести к прерыванию беременности, смерти плода или к рождению детей с ВКИ или с СВК.
В настоящее время по многочисленным данным известно, что риск развития врожденных дефектов составляет 80-90% при заболевании краснухой беременной женщины в первые 12 недель беременности. Наиболее тяжелые, но крайне редко встречающиеся, поражения плода возникают, когда вирус краснухи проникает в плод до формирования плаценты, в момент закладки органов. Данные по числу случаев СВК весьма ограничены, однако, по оценкам специалистов ВОЗ, при существующей заболеваемости, показателе рождаемости и популяционном иммунитете в группе женщин детородного возраста только в развивающихся странах ежегодно должно регистрироваться более 100000 случаев СВК.
Единственным научно обоснованным методом профилактики ВКИ и СВК является вакцинация. Вакцинация против краснухи в Российской Федерации введена в национальный календарь профилактических прививок в 1997 г. (приказ Минздрава России от 18.12.97 N 375). С 2002 г. в соответствии с приказом Минздрава России от 27.06.01 N 229 прививки против краснухи проводят в возрасте 12 месяцев, а также в 13 лет девочкам, ранее не привитым. Ревакцинация — в 6 лет и девочкам в 13 лет, ранее (не менее 6 месяцев назад) получившим лишь одну дозу вакцины.
Регламентированный охват населения, по данным ВОЗ, позволяющий ставить вопрос об элиминации краснухи и предупреждении возникновения случаев СВК, должен превышать 80% в возрасте 1 года и старше. В настоящее время в Российской Федерации вакцинированы против краснухи более 95% детей в возрасте до 2 лет, а ревакцинированы в возрасте 6 лет 87,2% детей.
Тем не менее, пока охват прививками против краснухи имеет ограниченное влияние на эпидемический процесс, и краснуха в России до сих пор сохранила черты неуправляемой инфекции (периодичность, сезонность, очаговость, преимущественное поражение детей). Более того, в последние годы среди заболевших краснухой наметилась тенденция к увеличению доли взрослого населения, в том числе женщин детородного возраста.
В целом по Российской Федерации показатель заболеваемости колеблется от 399,3 в 1999 г. до 93,1 на 100 тыс. населения в 2006 г. В 2007 г. (10 мес.) показатель заболеваемости краснухой впервые заметно снизился и составил 20,28 на 100 тыс. населения. Выраженное снижение заболеваемости краснухой связано с реализацией приоритетного Национального проекта в сфере здравоохранения в 2006-2007 гг., в рамках которого проводится интенсивная дополнительная вакцинация против краснухи детского и взрослого населения в возрасте до 25 лет, ранее не болевшего и не вакцинированного против этого инфекционного заболевания.
В условиях относительно высокой заболеваемости краснухой основной задачей ближайшего будущего для Российского здравоохранения является не только продолжающееся увеличение охвата прививками детского населения и женщин детородного возраста, не болевших краснухой и не привитых против этой инфекции, но и усиление эпидемиологического надзора за краснухой, направленного на предупреждение случаев заболевания краснухой беременных женщин и профилактику СВК.
4. Стандартное определение случая краснухи, врожденной краснушной инфекции и синдрома врожденной краснухи*
________________
* Данные стандартные определения рекомендованы ВОЗ.
Случай заболевания, подозрительный на краснуху — больной любого возраста с клиническим подозрением на краснушную инфекцию, у которого имеются следующие симптомы: лихорадка; пятнисто-папулезная сыпь; увеличение шейных, затылочных и (или) заушных лимфатических желез; или артралгии (артриты).
Лабораторно подтвержденный случай краснухи — случай заболевания, подозрительный на краснуху, который подтвержден лабораторно.
Эпидемиологически подтвержденный случай краснухи — случай заболевания, подозрительный на краснуху, который лабораторно не обследован, но эпидемиологически связан с лабораторно подтвержденным случаем краснухи.
Врожденная краснушная инфекция — заболевание ребенка (новорожденного), у которого обнаружены IgM к вирусу краснухи, но отсутствуют клинические симптомы, характерные для СВК, мать ребенка в период беременности перенесла краснуху или заболевание, подозрительное на нее.
Случай, подозрительный на синдром врожденной краснухи — любой младенец в возрасте до одного года, у которого медицинский работник заподозрил СВК, при этом:
у ребенка до одного года имеется заболевание сердца и (или) подозрение на наличие глухоты, и (или) один или несколько симптомов поражения глаз (катаракта, снижение остроты зрения, нистагм, косоглазие, микрофтальмия или врожденная глаукома);
мать ребенка имеет в анамнезе в период беременности подтвержденную краснуху или подозрение на нее.
Клинический случай СВК — случай заболевания, при котором имеются два и более осложнений из группы А или одно из А и одно и более из группы Б:
А) катаракта, врожденная глаукома, врожденное заболевание сердца, дефект слуха, пигментная ретинопатия;
Б) пурпура, спленомегалия, микроцефалия, отставание в развитии, менингоэнцефалит, желтуха в течение 24 ч после рождения.
Лабораторно подтвержденный случай СВК — ребенок с клиническими проявлениями СВК, в сыворотке которого обнаружены IgM к вирусу краснухи.
5. Патогенез краснухи, ВКИ/СВК. Диагностическая значимость маркеров инфекции
Вирион вируса краснухи диаметром около 70 нм представляет собой нуклеокапсид, окруженный липопротеидной оболочкой. Геном вируса представлен одноцепочечной позитивной РНК. В состав вириона входят три структурных белка: капсидный (белок С) и белки липопротеидной оболочки (Е1 и Е2). Структурные протеины Е1 и Е2 ответственны за индукцию гуморального (гемагглютинирующие, гемолизирующие и нейтрализующие антитела) иммунитета, в то время как С-протеин содержит эпитоп, индуцирующий клеточный иммунный ответ.
Хотя не существует значительных антигенных различий между изолятами вируса краснухи в соответствии с номенклатурой ВОЗ, принятой в 2005 г., идентифицировано 10 различных генотипов вируса. Идентификация генотипов используется для мониторинга циркуляции вируса и является важным источником информации при расследовании вспышек заболевания.
Возбудитель краснухи малоустойчив во внешней среде, легко разрушается детергентами, нагреванием или предельными значениями рН. По сравнению с другими распространенными воздушно-капельными инфекциями (корь, грипп) краснуха менее заразна, и обычно для передачи инфекции необходим тесный контакт. Продолжительность инкубационного периода варьирует от 9 до 23 дней, составляя в среднем 21 день. После попадания в дыхательные пути вирус размножается в клетках респираторного тракта и периферических лимфатических узлов, а затем проникает в кровоток. Вирус может быть выделен из носоглоточных секретов в период за 1 неделю до и в течение 2 недель после появления сыпи. В течение этого периода больной является потенциальным источником инфекции.
Клинически в продромальном периоде заболевания наблюдается повышение температуры до субфебрильных цифр, головная боль, слабость, легкий конъюнктивит, насморк, боль в горле и кашель, характерно увеличение затылочных, шейных и суставных лимфатических узлов. Мелкая, не сливная пятнисто-папулезная сыпь появляется сначала на лице и шее, затем быстро распространяется на туловище и конечности. Преимущественная локализация сыпи на 2-й день высыпания — разгибательные поверхности конечностей. Заболевание может сопровождаться артралгиями и артритами, что нехарактерно для детей, но часто встречается у взрослых, особенно у женщин. Изменения суставов, как правило, нестойкие и исчезают в течение 1-2 недель без остаточных явлений.
Сходство клинической симптоматики краснухи и других заболеваний, сопровождающихся экзантемой, требует проведения дифференциального диагноза с корью, внезапной экзантемой (вирус герпеса 6 типа), инфекционной эритемой (парвовирус В19), скарлатиной и рядом других. Следует учитывать, что до 50% случаев краснухи протекают бессимптомно.
При формировании иммунитета к вирусу краснухи IgM-специфические антитела появляются в крови в период высыпания и в первые 48 ч после появления сыпи выявляются в 50-70% случаев подтвержденной краснухи. В 100% случаев вирусспецифические IgM-антитела выявляются в период с 3-го дня до 8 недель и в 35% образцов — в сроки с 8-й по 18-ю неделю от начала клинических проявлений краснухи, затем уровень IgM-специфических антител постепенно снижается до неопределяемого. IgG-антитела к вирусу краснухи появляются в те же сроки, что и IgM, достигают «пика» через 3-4 недели и циркулируют в крови в течение всей жизни. Специфический клеточный иммунитет формируется через неделю после гуморального и также сохраняется в течение всей жизни переболевшего краснухой.
Заболевание краснухой формирует пожизненный иммунитет, однако случаи реинфекции, хоть и крайне редкие, возможны. Реинфекция характеризуется бессимптомным течением или слабовыраженной симптоматикой, и диагноз подтверждается с помощью серологического обследования, когда наблюдается кратковременный подъем уровня специфических IgM- и IgG-антител к вирусу краснухи. Вероятность реинфекции выше у ранее привитых, по сравнению с лицами, имеющими постинфекционный иммунитет.
Краснуха у плода протекает как генерализованный системный процесс с выраженной вирусемией и полиорганными поражениями. Формирование врожденных дефектов обусловлено тяжелым нарушением органогенеза в ранние сроки гестации вследствие активной репликации вируса в пораженных органах и тканях.
Последствия внутриутробного инфицирования зависят в первую очередь от срока беременности, при котором оно произошло. Так, при тяжелом течении инфекции, несовместимой с жизнью плода, до 20% случаев краснухи в первые 8 недель беременности приводят к самопроизвольным абортам. По данным Е.Miller с соав., при инфицировании в первые 12 недель беременности риск развития СВК достигает 80-90%, существенно снижается в период до 20-й недели и при инфицировании после 20-й недели беременности у новорожденных, как правило, выявляется ВКИ (табл.1).
Таблица 1
Риск врожденной инфекции и врожденных дефектов при краснухе беременных в зависимости от срока беременности
Срок беременности (недель) | Число случаев врожденной инфекции/Общее число случаев | Число случаев с врожденными дефектами/Общее число случаев |
1-12 | 13/16 (81%) | 11/13 (85%) |
13-16 | 29/54 (54%) | 9/26 (35%) |
17-22 | 33/92 (36%) | /* |
23-30 | 19/63 (30%) | |
31-36 | 15/25 (60%) | |
>36 | 8/8 (100%) | |
/* по данным Эндерс (1988) процент эмбриопатий при инфицировании плода на 18-38-й неделе беременности не превышает 3,5. | ||
Такая зависимость связана со сроками наиболее интенсивного органогенеза у плода, в том числе со сроками формирования иммунной системы. К 20-й неделе беременности иммунная система плода практически полностью сформирована, и благодаря эффективному иммунному ответу вирус краснухи нейтрализуется на ранних стадиях инфекции, и органная патология не развивается.
Следует отметить, что множественные врожденные дефекты чаще выявляются при инфицировании плода в первые 8 недель беременности.
Риск развития внутриутробной инфекции с проявлением тератогенного действия вируса очень высок при первичной инфекции. В то же время, врожденных дефектов развития не наблюдалось ни в случае ошибочной вакцинации беременных женщин вакцинами на основе аттенуированного штамма вируса, ни в редких случаях реинфекции в первом триместре беременности.
Эпидемиологическая значимость СВК обусловлена длительным персистированием вируса краснухи в организме таких пациентов и его выделением в окружающую среду (до 12 месяцев после рождения), что может способствовать распространению инфекции.
Источник
3.1.2. .
3.1.2.2356-08
(.
,
.. 25 2008 .)
: 1 2008 .
1. . 2
2. . 2
3. . 3
4. , . 4
5. , /. . 5
6. , . 7
6.1. . 8
6.2. . 11
6.3. , , /.. 12
6.4. .. 14
7. . 14
. 15
1. , . 16
2. .. 18
3. . 18
4. (- ) 20
5. () 20
6. .. 21
7. . 23
8. . 24
9. . 24
10. .. 24
11. . 25
12. , , , -, . 26
13. . 29
. 31
1.1. () , , , — — , , — — .
1.2. ( — — ) , .
2.1. 30.03.99 52- — .
2.2. 17.09.98 157- .
2.3. 22.07.93 5487-I ( . 02.03.98 30-, 20.12.99 214-, 02.12.00 139-, 10.01.03 15-, 27.02.03 29-, 30.06.03 86-, 29.06.04 58-, 22.08.04 122- (. 29.12.04), 01.12.04 151-, 07.03.05 15-, 21.12.05 170-, 31.12.05 199-, 02.02.06 23-, 29.12.06 258-, ., 24.12.93 2288).
2.4. 08.08.01 128- .
2.5. 1.1.1058-01 — () .
2.6. 3.1.2.1176-02 , .
2.7. 3.1/3.2.1379-03 .
2.8. 27.06.01 229 .
2.9. 17.06.06 27 1 27.06.01 229 .
2.10. 11.01.07 14 27 2001 . 229 68 , , , , , .
2.11. 3.1.2.1177-02 , .
2.12. 07.04.06 0100/3978-06-32 .
— , — , , , , . — — Rubovirus Togaviridae.
, , . , , , , .
, 80 — 90 % 12 . , , , , . , , , , 100000 .
. 1997 . ( 18.12.97 375). 2002 . 27.06.01 229 12 , 13 , . — 6 13 , ( 6 ) .
, , , 80 % 1 . 95 % 2 , 6 87,2 % .
, , (, , , ). , , .
399,3 1999 . 93,1 100 . 2006 . 2007 . (10 .) 20,28 100 . . 2006 — 2007 ., 25 , .
, , , .
________
*(1) .
, — , : ; — ; , () ; ().
— , , .
— , , , .
— (), IgM , , , , .
, — , , :
— () , () (, , , , );
— .
— , :
) , , , , ;
) , , , , , 24 .
— , IgM .
70 , . . : ( ) (1 2). 1 2 (, ) , — , .
, 2005 ., 10 . .
, , . — (, ) , . 9 23 , 21 . , . 1 2 . .
, , , , , , , . , — , . 2- — . , , , . , , 1 — 2 .
, , , ( 6 ), ( 19), . , 50 % .
IgM- 48 50 — 70 % . 100 % IgM- 3- 8 35 % — 8- 18- , IgM- . IgG- , IgM, 3 — 4 . .
, , , . , , IgM- IgG- . , , .
. .
, . , , , 20 % 8 . . Miller ., 12 80 — 90 %, 20- 20- , , (. 1).
1
() | / | / |
1 — 12 | 13/16 (81 %) | 11/13 (85 %) |
13 — 16 | 29/54 (54 %) | 9/26 (35 %) |
17 — 22 | 33/92 (36 %) | /* |
23 — 30 | 19/63 (30 %) | |
31 — 36 | 15/25 (60 %) | |
> 36 | 8/8 (100 %) | |
/* (1988) 18 — 38- 3,5. | ||
, . 20- , , .
, 8 .
. , , .
( 12 ), .
, .
, , . 2 3 .
2
,
, ≥ 50 % | , ≥ 90 % | , 50 % | |
IgM () | 1 (50 %) | 5 | 6 |
IgG () | 3 (50 %) | 8 | |
1 (90 %) | 2 | 4 | |
1 (50 %) | 5 | 1 |
. , . , .
3
,
, ≥50 % | , ≥ 90 % | , 50 % | |
IgM () | (80 %) | 1 | 3 |
IgG () | 100 % , | ||
( 100 %) | 2 | 3 | |
, / — , .
, /:
— ;
— / ;
— ;
— /.
, / :
1. , .
2. , .
3. .
4. .
5. , .
6.1.
( ) () .
( ) , . , , ( ), . 3.1.2.1177-02 , 3.1.2.1176-02 , .
— 24 , .
24 (. 1). , , .
( 15 , ) (. 8).
.
IgM- IgG- , IgG- (. 2).
, , 4 28 , 4 — 7 . , , . ( 21 ).
— .
, , , (. 3).
IgM- IgG- (), . , .
( ) . , , , .
, , , .
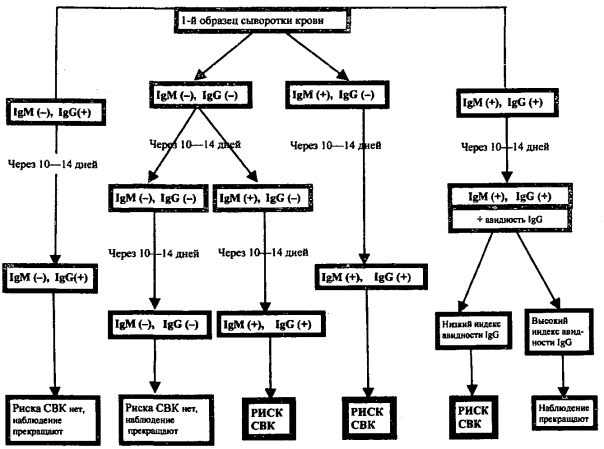
( IgG, IgM), , 10 — 14 . . 10 — 14 . , . .
IgM IgG , , , .
IgM- , 10 — 14 . IgM- ( IgG-) .
IgG- ( IgM-) , .
IgM- IgG- 10 — 14 . , IgG.
IgG- , .. IgG, , (), IgG, , (). 2 — 3 , IgM, .
IgG , . IgG, IgG, .
, IgM , 19 , , . IgG .
— .
, , ( ), — ( .. ) . , (5, 10), — , .
— , (5 5 ), IgM IgG.
, , . IgM .
, , .
, !
( 15 ) — ( . .. ) , (. 11).
6.2.
:
— ();
— ();
— .
, , , , . 12 , 80 — 90 % (). , , , . ; — 18 . , . . .
1991 . 1991 — 2006 . 0 1996 . 11 — 2000 ., . , 0,13 % , , 300 — 400 .
, / , IgM-. , , , ( ) (. 3). Ig- . IgM- . () ().
— . .
, .
, , , — , (. 5).
: IgM IgG , IgG, — — (. 3, 4).
, IgM- 100 % 3 , , 3- IgM , 18 .
IgG- , 100 % 1 , 6 — 10 () , () . , IgG .
— , 3 . , . , (), , .
— .
, , , — ( , ), .
.
6.3. , ,
/
, , .
/ , , , -, , — .
/ — 24 , , .
/ . , /. ( .)
2- ݻ (. 3). 48 . ݻ , . .
ݻ / 72 . / .
.
, , .
/ 72 , .
24 (. 5). , .
ʻ (. 6), .
( ), 24 , .
/ ,
. (. 7), (. 8) (. 9). ( 15 , ) (. 7 — 9).
, , .
6.4.
, , 12 , . () , .
— 24 , , .. , () , .
, , , , . ( ) () — 72 , 25 :
— ;
— ;
— 6 , ;
— ;
— , .
, , , , .
, () 12 . (, ) — ( . .. ) (. 4) , (. 12).
, 24 .
(. 10).
, . . .
/ ( ) , , . / , , . , , 2005 — 2010 , .
/ .
(, , -, , , ), , , , . , , — .
1. .. . ., 1987.
2. .. .// . . : . . 1997. . 17 — 24.
3. .., .. — // . 2004. — .
4. .., .. , // . 2004. 5, . 8 — 11.
5. . , 2003.
6. , , : 0100/5751-05-32 08.07.05.
7. 2005 — 2010 . , 2005.
8. : . -, 2002.
9. Cutts FT, Robertson SE, Diaz-Ortega J-L, Samuel R. Control of Rubella and congenital rubella syndrome (CRS) in developing countries. Part 1: burden of disease from CRS. Bull World Health Organ 1997; 75:55 — 68.
10. Manual for the laboratory diagnosis of measles and rubella virus infection, WHO, 2006.
11. Measles and Rubella surveillance and monitoring vaccination cover age in countries with complex health care systems-Report of WHO European meeting, Paris, France, 20 — 21 September, 2004.
12. Measles and Rubella viruses. William J. Bellini, Joseph . Icenogle/Manul of Clinical Microbiology, 8-th Ed.//ASM Press, Washington, P.C., p. 1389 — 1403.
13. Miller E, Cradock-Watson JE, Pollock TM. Consequences of confirming maternal rubella at successive stages of pregnancy. Lancet 1982; 2: 781 — 784.
14. Munro N.D. Sheppard S, Smithells RW, Holcel H, Jones G. Temporal relations between maternal rubella and congenital defects. Lancet 1987; 2: 201 — 204.
15. Rubella. Jennifer . Best. Seminars in Fetal and Neonatal Medicine, 2007; 12: 182 — 192.
16. Standardization of the nomenclature for genetic characteristics of wild-type rubella viruses. Wkly Epidemiol Rec, 2005. 80 (14): p. 126 — 132.
17. Third WHO Global Measles and Rubella Laboratory Network Meet ing, Geneva, 2526 August 2005, Summary and ation.
18. Ueda K, Nishida Y, Oshima K, Shepard TN. Congenital rubella syndrome: correlation of geional age at of maternal rubella with type of defect. J Pediatr 1979; 94:763 — 765.
19. World Health Organization. Guidelines for surveillance of congenital rubella syndrome and rubella — field test version, May 1999 (WHO/V&B/99.22).
20. World Health Organization. Progress towards elimination of measles and prevention of congenital rubella infection in the WHO Europian Region, 1990 — 2004. Wkly Epidemiol Rec 2005; 80 (8); 66 — 71.
21. World Health Organization. Surveillance guidelines for measles and congenital rubella infection in the WHO Europian Region. Copenhagen: World Health Organization; 2003.
,
A.
., ., . ___________________________________________________________________
□ □ . * ___________________________________________
________
, ,
: _____________________________________________________________________
, ( )
__________ ,
___________________________________________________________________________
, _____________________________________________________
___________________________________________________ □
() ____________________________________________
() __________________________________________
() ____________ ____________
: □ □ □, _____________________
: □ □ □, ________________
, _______________________________
___________________ _________________________
_____________________
___________________________
__________________________________________________
(, 1 2 , (), __________________ ()
_________________________________________________________
: □ □ □
____________ ____________ ___________
B. . ().
1. _________________________________________________
. ݻ _________________________
___________________________________________
____________________ _____________________
2. _________________________________________________________
. ݻ _________________________
___________________________________________
__________________ _______________________
. :
: ( )
., ., . ____________________________________ □
/ _________________________________________________________
________________________________________ (, , )
_______________ (, ) _______________
______________________________________________
____________________________________________
— □ _____________________ □
. ( )
_________________ ______________
: ______________ () _____________
(): □ □ □ □ □
: □ □
: — □ □
: □ □ □ _________________________
: □ □ □
: □ □ □
: □ □ □
: □ □ □ □ □ □
: □ □
: □ □ □ : □ □ □
□ □ ( ) ________________________________________
: □ □ _______________________________________
___________________________________________________________________________
: □ □ ______________________________
_______________________________________________________
. ( ) __________________________
□ □ □ □ □
_____________________________________________________________
: □ □ □
: □ □ □ __________________________________
_________________________________________________
___________________________________________________________________________
_______________________________________________
__________________ — _____________
( , ,
; ,
; , ,
/; , )
I. ,
, : — _______________ — ______________
., ., . __________________________________________________________
* _____________________________________________________________
________
* , , .
_____________________________________________________________________
_____________________ ___________________
: ___________________________________________________
_______________________________________________________
________ □ □ □ □
_______________ _________________
: IgM □ □
IgG □ □
_______________________________________
II. , /
, : — __________ — ___________________
., ., . __________________________________________________________
* _____________________________________________________________
________
* , , .
_____________________________________________________________________
_____________________________________
_________________________________________________
________________________ _______________________
_____________________ ___________________
: ___________________________________________________
_______________________________________________________
_____ □ □ □ □
_________________ _______________
: IgM □ □
IgG □ □
_______________________________________
III. /
, : — _________ — ________ / _________
., ., . __________________________________________________________
* _____________________________________________________________
________
* , , .
_____________________________________________________________________
__________________ : _________________
_______________________________________________________
_____ □ □ □ □
__________________ ______________
: IgM □ □
IgG □ □
_______________________________________
IV. (, )
, : — _________ — ________ / _________
., ., . ________________________________________ __________
_____________________________________________________________________
__________________________________________________________
____________________________________________
_____________________ ___________________
___________________ _____________________
□ □ ______________________
_____________________________________________
_________________ _______________
: IgM □ □
IgG □ □
_______________________________________
___________________ ____________________________
(- )
_____________________________ ___________________________________
., ., . : __________________________________________________ □ □
______________________________________________________________
_____________________________________________________________________
: ________________________________________________
: ________________________________________________________
: ________________________________________
., ., . , :
___________________________________________________________________________
: _____________________________________________________________________
: ____________ : _______________ : _______________
— ( . .. ):
., ., . , : ________________________
()
, : ____________________
___________________________________________________________________________
(, , .)
1. ___________________________ _____________________
____________________ _________________ / ____________
, , , . ______________________________
( ):
— . — □ □
— (, , , ..) □ □
— , □ □
— . □ □
— (, — ) □ □
— 24 □ □
— □ □
— □ □
— □ □ ()
() _____________________________________________________
____________________ ________________
____________________ ______________________
□ □ ________________________________
2. ., ., . __________________________________________________________
______________ _______________________________________________
() ____________________________________________________
, ___________________________________________________________
( , ) ______________________________________
□ □ _____________________________
_____________________________________________
___________________________________________
_______________ ____________________
/ ( .) ___________________________________
______________________________
_______________________
_____________________________________________
___________________________________________________________________________
□ □ ______________
___________________________________________________________________________
___________________________________________________________________________
___________________________________________________________________________
3.
4. ( ):
___________________________________________ □ □
____________________________ □ □
() _____________________________ □ □
., ., . , __________________________________
_______________________________________________________________________
., ., . , _______________________________
_______________________________________________________________________
________________________________________ 20 __
1. , ____________________
___________________________________________________________________________
2. ., ., . ________________________________________________________
3. (, , ) ___________________________________________
4. ________________________________________________________
5. ____________________________________________________
6. ______________________________________________________________
7. ___________________________________________________________
8. — ____________________________________________
9. :
______________________ _________________________
10. :
— □ □
— □ □
— __________________________
__________________________________________________________
_______________________________________________________________________
Источник