Гнойный менингит при травмах черепа
Содержание статьи
Гнойный менингит (Бактериальный менингит)
Гнойный менингит — воспалительный процесс, возникающий в мягкой оболочке головного мозга при проникновении в нее гноеродных микроорганизмов (пневмококков, менингококков, стрептококков и пр.). Гнойный менингит характеризуется высокой температурой тела, интенсивной головной болью, тошнотой, рвотой, нарушениями со стороны черепно-мозговых нервов, ранним появлением менингеальных симптомов, гиперестезией, расстройством сознания, психомоторным возбуждением. Диагностировать гнойный менингит можно на основании типичной клинической картины и данных анализа цереброспинальной жидкости. Гнойный менингит является показанием к обязательному проведению антибиотикотерапии. Применяются противоотечные препараты, глюкокортикостероиды, транквилизаторы, противосудорожные средства и пр. симптоматическая терапия.
Общие сведения
Гнойный менингит — это воспаление мозговых оболочек (менингит), имеющее бактериальную этиологию. Гнойный менингит встречается с частотой 3,3 случаев на 100 тыс. населения. Заболеванию подвержены все возрастные категории, но наиболее часто гнойный менингит развивается у детей до 5 лет. Отмечено, что гнойный менингит часто возникает на фоне ослабленного состояния иммунной системы. Повышение заболеваемости наблюдается в зимне-весенний период. С начала 90-х годов прошлого века произошло существенное снижение заболеваемости гнойным менингитом, уменьшение числа летальных исходов и случаев развития тяжелых осложнений.
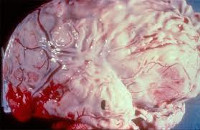
Гнойный менингит
Причины возникновения гнойного менингита
К развитию гнойного менингита может приводить не только менингококковая инфекция, но также пневмококки, гемофильная палочка и другие бактерии. Почти половина случаев гнойного менингита приходится на долю гемофильной палочки. В 20% причиной гнойного менингита является менингококк, в 13% случаев — пневмококк. У новорожденных гнойный менингит зачастую возникает в результате стрептококковой инфекции, сальмонеллеза или инфицирования кишечной палочкой.
В зависимости от механизма проникновения возбудителя в оболочки головного мозга в неврологии выделяют первичный и вторичный гнойный менингит. Первичный гнойный менингит развивается при гематогенном распространении возбудителя из полости носа или глотки, куда он попадает из внешней среды. Заражение происходит от больных лиц и носителей воздушно-капельным и контактным путем. Прямое инфицирование мозговых оболочек возможно при переломе черепа и открытой черепно-мозговой травме, открытых повреждениях сосцевидного отростка и придаточных пазух носа, недостаточно тщательном соблюдении правил асептики в ходе нейрохирургических вмешательств.
Вторичный гнойный менингит возникает на фоне имеющегося в организме первичного септического очага, инфекция из которого проникает в оболочки головного мозга. Контактное распространение гноеродных микроорганизмов может наблюдаться при абсцессе головного мозга, остеомиелите костей черепа, септическом синустромбозе. Гематогенное и лимфогенное распространение возбудителя возможно из инфекционного очага любой локализации, но наиболее часто происходит при длительно протекающих инфекциях лор-органов (остром среднем отите, хроническом гнойном среднем отите, синуситах).
Проникновению возбудителей гнойного менингита через гематоэнцефалический барьер способствует ослабленное состояние иммунной системы организма, которое может быть вызвано частыми ОРВИ, гиповитаминозом, перенесенным стрессом, физическими перегрузками, резкой сменой климата.
Классификация гнойного менингита
В зависимости от тяжести клинических проявлений гнойный менингит классифицируется на легкую, среднетяжелую и тяжелую формы. Тяжелые формы заболевания наблюдаются в основном на фоне резкого снижения иммунитета и у пациентов с удаленной селезенкой.
По особенностям течения выделяют молниеносный, абортивный, острый и рецидивирующий гнойный менингит. Наиболее часто встречается острый гнойный менингит с типичными общемозговыми и оболочечными симптомами. Молниеносное течение гнойного менингита с первых часов заболевания характеризуется быстрым нарастанием отека головного мозга, приводящего к нарушению сознания и витальных функций. Абортивный вариант отличается стертой клинической картиной, в которой на первый план выходят симптомы интоксикации. Рецидивирующий гнойный менингит может наблюдаться при недостаточном или запоздалом лечении острой формы заболевания, а также при наличии в организме хронического очага гнойной инфекции.
Симптомы гнойного менингита
Инкубационный период первичного гнойного менингита в среднем длится от 2 до 5 суток. Типично острое начало с резкого повышения температуры тела до 39-40°С, сильного озноба, интенсивной и нарастающей головной боли, тошноты и многократной рвоты. Могут наблюдаться психомоторное возбуждение, бред, нарушения сознания. В 40% случаев гнойный менингит протекает с судорожным синдромом. Специфичные для менингита оболочечные симптомы (симптом Кернига, Брудзинского, Гийена, ригидность затылочных мышц) выражены с первых часов заболевания и усиливаются на 2-3-й день. Типичны выраженная гиперестезия и снижение брюшных рефлексов на фоне общего повышения глубоких рефлексов. Возможно появление диффузной сыпи геморрагического характера.
Очаговая симптоматика, сопровождающая гнойный менингит, чаще всего заключается в нарушении функций различных черепно-мозговых нервов. Наиболее часто наблюдается поражение глазодвигательных нервов, приводящее к двоению, развитию косоглазия, опущению верхнего века и появлению разницы в размере зрачков (анизокории). Реже отмечается неврит лицевого нерва, поражение тройничного нерва, расстройство функции зрительного нерва (выпадение полей зрения, снижение остроты зрения) и преддверно-улиткового нерва (прогрессирующая тугоухость). Более тяжелая очаговая симптоматика свидетельствует о распространении воспалительных изменений на вещество головного мозга или о развитии сосудистых нарушений по типу ишемического инсульта, обусловленных васкулитом, рефлекторным спазмом или тромбозом сосудов головного мозга.
При переходе воспалительного процесса на вещество мозга говорят о развитии менингоэнцефалита. При этом гнойный менингит протекает с присоединением характерной для энцефалита очаговой симптоматики в виде парезов и параличей, нарушений речи, изменений чувствительности, появления патологических рефлексов, повышения мышечного тонуса. Возможны гиперкинезы, галлюцинаторный синдром, нарушения сна, вестибулярная атаксия, расстройства поведенческих реакций и памяти. Распространение гнойного процесса на желудочки мозга с развитием вентрикулита проявляется спастическими приступами по типу горметонии, сгибательными контрактурами рук и разгибательными ног.
Осложнения гнойного менингита
Ранним и грозным осложнением, которым может сопровождаться гнойный менингит, является отек головного мозга, приводящий к сдавлению мозгового ствола с расположенными в нем жизненно важными центрами. Острый отек головного мозга, как правило, возникает на 2-3-й день заболевания, при молниеносной форме — в первые часы. Клинически он проявляется двигательным беспокойством, нарушением сознания, расстройством дыхания и нарушениями со стороны сердечно-сосудистой системы (тахикардия и артериальная гипертензия, в терминальной стадии сменяющиеся брадикардией и артериальной гипотонией).
Среди прочих осложнений гнойного менингита могут наблюдаться: септический шок, надпочечниковая недостаточность, субдуральная эмпиема, пневмония, инфекционный эндокардит, пиелонефрит, цистит, септический панофтальмит и др.
Диагностика гнойного менингита
Типичные клинические признаки, наличие менингеальных симптомов и очаговой неврологической симптоматики в виде поражения черепно-мозговых нервов, как правило, позволяют неврологу предположить у пациента гнойный менингит. Более затруднительна диагностика в случаях, когда гнойный менингит имеет абортивное течение или возникает вторично на фоне симптомов существующего септического очага другой локализации. Чтобы подтвердить гнойный менингит необходимо произвести люмбальную пункцию, в ходе которой выявляется повышенное давление ликвора, его помутнение или опалесцирующая окраска. Последующее исследование цереброспинальной жидкости определяет увеличенное содержание белка и клеточных элементов (в основном за счет нейтрофилов). Выявление возбудителя производится в ходе микроскопии мазков цереброспинальной жидкости и при ее посеве на питательные среды.
С диагностической целью производят также анализ крови и отделяемого элементов кожной сыпи. При предположении о вторичном характере гнойного менингита проводятся дополнительные обследования, направленные на поиск первичного инфекционного очага: консультация отоларинголога, пульмонолога, терапевта; рентгенография околоносовых пазух, отоскопия, рентгенография легких.
Дифференцировать гнойный менингит необходимо от вирусного менингита, субарахноидального кровоизлияния, явлений менингизма при других инфекционных заболеваниях (сыпном тифе, лептоспирозе, тяжелых формах гриппа и др.).
Лечение гнойного менингита
Все имеющие гнойный менингит пациенты подлежат лечению в условиях стационара. Таким больным должна быть неотложно проведена люмбальная пункция и бактериоскопическое исследование ликвора. Сразу же после установления этиологии менингита пациенту назначается антибиотикотерапия. В большинстве случаев она представляет собой сочетание ампициллина с препаратами цефалоспоринового ряда (цефтриаксоном, цефотаксимом, цефтазидимом). При гнойном менингите неустановленной этиологии стартовая терапия заключается во внутримышечном введении аминогликозидов (канамицина, гентамицина) или их комбинации с ампициллином. Тяжело протекающий гнойный менингит может потребовать внутривенного или интратекального введения антибиотиков.
С целью уменьшения гидроцефалии и отека мозга при гнойном менингите назначают дегидратационную терапию (фуросемид, маннитол). Патогенетическое лечение гнойного менингита также включает применение глюкокортикостероидных препаратов (дексаметазона, преднизолона), дозы которых зависят от тяжести заболевания. Наряду с этим производится необходимая симптоматическая терапия. При нарушениях сна назначаются транквилизаторы; для купирования психомоторного возбуждения и судорог — литические смеси (хлорпромазин, дифенгидрамин, тримеперидина), диазепам, вальпроевая кислота; при гиповолемии и развитии инфекционно-токсического шока проводится инфузионная терапия.
В восстановительном периоде после перенесенной острой фазы гнойного менингита рекомендован прием ноотропных и нейропротекторных препаратов, витаминотерапия и общеукрепляющее лечение. Лечение пациентов, имеющих вторичный гнойный менингит, должно включать ликвидацию первичного септического очага, в том числе и путем хирургического вмешательства (санирующая операция при среднем отите, фронтотомия, этмоидотомия, сфенотомия, удаление внутримозгового абсцесса и т. п.).
Прогноз гнойного менингита
По некоторым данным в 14% случаев гнойный менингит приводит к летальному исходу. Однако при своевременно начатом и корректно проведенном лечении гнойный менингит имеет в основном благоприятный прогноз. После перенесенного менингита может наблюдаться астения, ликворно-динамические нарушения, нейросенсорная тугоухость, отдельные слабо выраженные очаговые симптомы. Тяжелые последствия гнойного менингита (гидроцефалия, амавроз, глухота, деменция, эпилепсия) в наше время являются редкостью.
Профилактика гнойного менингита
На сегодняшний день наиболее эффективным способом, позволяющим предупредить гнойный менингит, является вакцинация. Прививки проводится против основных возбудителей гнойного менингита: гемофильной палочки, менинго- и пневмококков. В России эти вакцины не считаются обязательными и вводятся по показаниям или по желанию пациентов.
Вакцинация против гемофильной инфекции проводится в основном детям в возрасте от 3 месяцев до 5 лет и людям, страдающим иммунодефицитными состояниями в результате ВИЧ-инфекции, проведения иммуносупрессивной терапии онкозаболеваний, удаления тимуса или селезенки и т. п. Вакцинация против менингококковой инфекции рекомендована детям после 18 месяцев и взрослым. Детям до 18 месяцев вакцинация проводится по эпидемическим показаниям (например, если менингококковый гнойный менингит диагностирован у одного из членов семьи). В регионах, опасных по менингококковому гнойному менингиту, вакцинация должна проводиться пациентам с иммунодефицитом и людям, имеющим анатомические дефекты черепа. Вакцинация против пневмококковой инфекции показана часто болеющим детям, пациентам с частыми пневмониями и отитами, в случаях пониженного иммунитета.
Источник
Осложнения черепно-мозговой травмы
К осложнениям ЧМТ относятся:
— ликворея. Посттравматическая ликворея — истечение ликвора из полости наружу, возникающее вследствие проникающего травматического повреждения черепа и оболочек головного мозга (особенно часто при переломах основания черепа). В 97% случаев это назальная ликворея. Ликворея встречается, по разным данным, у 1,5-40% больных. При этом существует риск развития менингита. Лечение сводится к созданию условий для заращения свища;
— пневмоцефалия. Редкое осложнение проникающей ЧМТ, при котором воздух попадает в полость черепа. Может быть бессимптомной или проявляться головной болью, психическими нарушениями. Если развивается менингит, то повышается внутричерепное давление. Обычно воздух в полости черепа рассасывается, но стойкая пневмоцефалия требует хирургического вмешательства;
— гнойный менингит. При закрытой ЧМТ развивается в 3-5%, при открытой и проникающей ЧМТ — в 8-10%. Иногда развивается вентрикулит и/или сопутствующий менингиту энцефалит. Первичный менингит возникает вследствие непосредственного проникновения микрофлоры в полость черепа при его повреждении, вторичный менингит — микрофлора мигрирует из гнойных очагов (абсцессы мозга, легких и т. п.). Решающим в диагностике является исследование ликвора (диагностический критерий гнойного менингита: если на один лейкоцит в ликворе эритроцитов приходится меньше, чем в крови). Лечение комплексное: антибактериальное, иммунокорригирующее, детоксикационное;
— абсцесс мозга. Редкое осложнение при проникающей ЧМТ с повреждением кожных покровов головы и их нагноением. В развитии абсцесса различают 3 стадии: 1) латентную; 2) с симптомами формирования абсцесса; 3) терминальную, с явлениями отека, дислокации мозга и интоксикации. Клиническая картина абсцесса мозга складывается из выраженной общемозговой, менингеальной и очаговой полушарной симптоматики с вегетативными нарушениями, в частности температурой тела до 38-40°C, а далее с утяжелением состояния, вызванным развитием дислокационного синдрома. При небольших абсцессах предпочтение отдается консервативной терапии (антибактериальной, детоксикационной, инфузионной, иммунокорригирующей), при абсцессах с компрессией мозга рекомендуется хирургическое лечение (открытое вмешательство, пункция абсцесса, последующее дренирование мозговой раны);
— посттравматическая эпилепсия. Эпилепсия, развивающаяся на первой неделе после ЧМТ, называется ранней. Факторами риска развития ранней эпилепсии являются:
1) отсутствие сознания при поступлении — вероятность развития эпилепсии при утрате сознания составляет 2-6%, а при выключении сознания более 24 часов — 10-14%;
2) линейный перелом костей свода черепа повышает вероятность эпилепсии до 7%;
3) вдавленный перелом свода черепа повышает риск развития эпилепсии до 10-11%;
4) внутричерепная гематома, очаги ушиба-размозжения сопровождаются развитием ранней эпилепсии в 20-30%. У 60-80% пострадавших ранняя эпилепсия проявляется фокальными, у 30-40% — генерализованными припадками. Ранняя эпилепсия чаще бывает у детей и лиц молодого возраста, редко — у пожилых. Какой-либо зависимости между развитием ранней эпилепсии и отдаленными исходами ЧМТ не отмечается.
Посттравматическая эпилепсия чаще возникает у пострадавших с ранней эпилепсией и наблюдается в 2,4-5% случаев ЧМТ. Наиболее часто посттравматическая эпилепсия развивается при:
— проникающем огнестрельном ранении — 53%;
— внутримозговой гематоме в сочетании с ушибом-размозжением головного мозга — 39%;
— локальном очаге ушиба по данным КТ — 3,2%;
— развитии ранней эпилепсии — 25%;
— вдавленном переломе, сопровождающемся повреждением твердой мозговой оболочки, — 25%;
— эпидуральной или субдуральной гематоме — 20%;
— развитии очаговой неврологической симптоматики — 20%.
У 50% пострадавших посттравматическая эпилепсия развивается в течение одного года после ЧМТ, у 70-80% — в течение двух лет. Генерализованные припадки наблюдаются у 60-70% пациентов, фокальные припадки — у 30-40%;
— хроническая посттравматическая энцефалопатия, или травматическая болезнь. Рассматривается как позднее или отдаленное осложнение выраженной ЧМТ. Может проявляться как в форме резидуального состояния, так и в форме динамического процесса с тенденцией к прогредиентности. Основные клинические характеристики болезни:
1) астеноневротический синдром;
2) вегетососудистая дистония;
3) диффузная головная боль («тяжелая голова»);
4) когнитивный (лат. cognito — знание) дефицит;
5) расстройства сна;
6) очаговая мозговая микросимптоматика;
7) иногда — повышенное содержание белка в ликворе.
Также характерны при этом трудности в сосредоточении внимания и выполнении интеллектуальных задач, эмоциональная лабильность, снижение толерантности к эмоциональным нагрузкам и алкоголю, симптомы вегетативной дисфункции, ликвородинамические расстройства, иногда — эпилептические припадки, ипохондрия, депрессия. Со временем проявления посттравматической энцефалопатии могут возрастать, уменьшаться или оставаться стабильными. Обычно она более выражена у пожилых пациентов, перенесших ЧМТ;
— осложнениями ЧМТ могут быть посттравматический арахноидит, стойкие нарушения ликвородинамики (чаще повышение внутричерепного давления), а также атрофические процессы с заместительной гидроцефалией. После резекционной краниотомии или костно-пластической трепанации с последующим удалением костного лоскута может развиваться стойкий трепанационный синдром. Его характеризуют боль и болезненность в зоне трепанационного отверстия в черепе. Боль может усиливаться при резких колебаниях атмосферного давления;
— хронический посткоммоционный синдром (ХПС). Частое возникновение после легкой ЧМТ относительно стойких посттравматических нарушений, сохраняющихся на протяжении недель, месяцев и даже лет, считают «основным парадоксом» легкой ЧМТ. Распространенность ХПС достигает, по данным специальных исследований, 90%. Развитие ХПС связывают с легкой степенью диффузного аксонального повреждения.
Наиболее заметным признаком ХПС является головная боль. Установлена обратно пропорциональная связь между тяжестью ЧМТ и частотой развития в последующем стойких головных болей. В случаях легкой ЧМТ головная боль в последующем выявляется у 30-90% пациентов. Головная боль может быть локальной или диффузной, эпизодической или ежедневной. Чаще она протекает по типу головной боли напряжения («стягивающая» боль, боль в виде «каски»), но она может быть и мигренозной, причем возникает с аурой приступа мигрени. Реже головная боль бывает кластерной (протекает в виде серий коротких эпизодов головной боли) или ортостатической (возникающей при быстром вставании из положения лежа или сидя), наконец, цефалгия иногда является в виде супра- или инфраорбитальной невралгии.
Это цефалгии, которые, согласно классификации Международного общества головной боли, возникают не позже 14 дней после ЧМТ. Механизмы, запускающие такую боль, не установлены.
Посттравматическая головная боль обычно сопровождается шумом в ушах, раздражительностью, снижением концентрации внимания, плохой переносимостью алкоголя. Реже отмечаются головокружение, акустическая гиперестезия, звон в ушах, бессонница, апатия, утомляемость, снижение либидо, синкопальные состояния преимущественно неврогенного генеза. Нейропсихологические исследования выявляют у пациентов снижение скорости усвоения информации, памяти, временных реакций.
Исследованиями ряда авторов установлено, что развитию посткоммоционного синдрома наряду с ЧМТ способствуют дополнительные или вторичные факторы. Наиболее значительными из них являются возраст, социально-экономический статус, семейное положение, депрессия или тревога, личностные качества, посттравматический стресс, употребление алкоголя или наркотиков. Тем не менее остается неясным, каким образом можно профилактировать развитие ХПС.
ХПС трудно поддается терапии. Большинство его симптомов обусловлено как нейрональной дисфункцией, так и психологическими факторами (какими именно в первую очередь, не уточняется). Проблемы таких пациентов, полагают, следует делить на 3 категории:
1) физические (головная боль, головокружение, нарушение сна);
2) когнитивные (снижение концентрации внимания, памяти);
3) эмоциональные (раздражительность, эмоциональная лабильность).
Каждая из этих проблем требует специального подхода, включая психотерапию и дозированную физическую нагрузку.
При лечении головной боли напряжения используют трициклические антидепрессанты (амитриптилин, нортриптилин, доксепин). При лечении посттравматической мигрени в 70% эффективен амитриптилин или пропранолол, достаточно эффективны надолол, тимодол, нортриптилин, доксепин, верапамил, напроксен и др. Препаратом выбора при лечении посттравматических кластерных болей является верапамил.
Диагностика ЧМТ основана на клинико-неврологическом и клинико-психопатологическом исследовании, к обследованию привлекаются и другие специалисты. Из инструментальных методов используются R-графия черепа, эхоэнцефалоскопия, церебральная эхография, компьютерная рентгеновская томография, транскраниальная допплерография, лабораторные методы (исследование ликвора, крови и др.).
Вернуться к Содержанию
Источник