Белок при гнойном менингите
Содержание статьи
Состав ликвора при различных нозологиях
В обзоре представлены изменения лабораторных показателей ликвора при основных тяжелых заболеваниях цетральной нервной системы.
МЕНИНГИТЫ
Исследование спинномозговой жидкости является единственным методом, позволяющим быстро диагностировать менингит. Отсутствие воспалительных изменений в ликворе всегда позволяет исключить диагноз менингита. Этиологический диагноз менингита устанавливают с помощью бактериоскопических и бактериологических методов, вирусологических и серологических исследований.
Плеоцитоз — характернейшая черта изменений СМЖ. По числу клеток различают серозный и гнойный менингиты. При серозном менингите цитоз составляет 500-600 в 1 мкл, при гнойном — более 600 в 1 мкл. Исследование должно быть проведено не позже чем через 1 час после ее получения.
По этиологической структуре 80-90% бактериологически подтвержденных случаев приходится на Neisseria meningitides, Streptococcus pneumoniae и Haemophilus. Бактериоскопия СМЖ благодаря характерной морфологии менингококков и пневмококков дает при первой люмбальной пункции положительный результат в 1, 5 раза чаще, чем рост культуры.
СМЖ при гнойном менингите от слегка мутноватой, как бы забеленной молоком, до густо зеленой, гнойной, иногда ксантохромной. В начальной стадии развития менингококкового менингита имеет место повышение внутричерепного давления, затем в ликворе отмечается нейтрофильный маловыраженный цитоз, а у 24, 7% больных СМЖ нормальная в первые часы болезни. Затем у многих больных уже в первые сутки заболевания цитоз достигает 12000-30000 в 1 мкл, преобладают нейтрофилы. Благоприятное течение заболевания сопровождается уменьшением относительного числа нейтрофилов и увеличение лимфоцитов. Встречающиеся случаи гнойного менингита с типичной клинической картиной и сравнительно небольшим цитозом могут быть объяснены, вероятно, частичной блокадой субарахноидального пространства. Отчетливой корреляции между выраженностью плеоцитоза и тяжестью заболевания может не наблюдаться.
Содержание белка в СМЖ при гнойном менингите обычно повышено до 0, 6-10 г/л и уменьшается по мере санации ликвора. Количество белка и цитоз обычно параллельны, но в отдельных случаях при высоком цитозе уровень белка остается нормальным. Большое содержание белка в СМЖ чаще встречается при тяжелых формах с синдромом эпендидимита, а наличие его в высоких концентрациях в период выздоровления указывает на внутричерепное осложнение (блок ликворных путей, дуральный выпот, абсцесс мозга). Сочетание низкого плеоцитоза с высоким содержанием белка — особенно неблагоприятный прогностический признак.
У большинства больных гнойным менингитом с первых дней болезни отмечается понижение уровня глюкозы (ниже 3 ммоль/л), при летальных исходах содержание глюкозы было в виде следов. У 60% больных содержание глюкозы ниже 2, 2 ммоль/л, а отношение уровня глюкозы к таковому в крови у 70% составляет менее 0, 31. Увеличение содержания глюкозы — почти всегда прогностически благоприятный признак.
При туберкулезном менингите бактериоскопическое исследование СМЖ часто дает отрицательный результат. Микобактерии чаще обнаруживают в свежих случаях заболевания (у 80% больных туберкулезном менингитом). Нередко отмечается отсутствие микобактерий в люмбальном пунктате при обнаружении их в цистернальной СМЖ. В случае отрицательного или сомнительного бактериоскопического исследования туберкулез диагностируют методом посева или биологической пробой. При туберкулезном менингите СМЖ прозрачна, бесцветна или слегка опалесцирует. Плеоцитоз колеблется от 50 до 3000 в 1 мкл, в зависимости от стадии заболевания, составляя к 5-7 дню болезни 100-300 в 1 мкл. При отсутствии этиотропного лечения число клеток нарастает от начал до конца заболевания. Может быть внезапное падение цитоза при повторной люмбальной пункции, проведенной через 24 часа после первой. Клетки преимущественно лимфоциты, однако нередко в начале болезни встречается смешанный лимфоцитарно-нейтрофильный плеоцитоз, что считается типичным для миллиарного туберкулеза с обсеменением мозговых оболочек. Характерным для туберкулезного менингита является пестрота клеточного состава, когда наряду с преобладанием лимфоцитов встречаются нейтрофилы, моноциты, макрофаги и гигантские лимфоциты. Позднее — плеоцитоз приобретает лимфоплазмоцитарный или фагоцитарный характер. Большое количество моноцитов и макрофагов свидетельствует о неблагоприятном течении заболевания.
Общий белок при туберкулезном менингите всегда повышен до 2-3 г/л, причем ранее исследователи отмечали, что белок увеличивается до появления плеоцитоза и исчезает после значительного его уменьшения, т. е. в первые дни заболевания имеет место белковоклеточная диссоциация. Для современных атипичных форм туберкулезного менингита характерно отсутствие типичной белковоклеточной диссоциации.
При туберкулезном менингите рано отмечается снижение концентрации глюкозы до 0, 83-1, 67 ммоль/л и ниже. У части больных выявляется снижение содержания хлоридов. При вирусном менингите около 2/3 случаев возбудителями являются вирус эпидемического паротита и группа энтеровирусов.
При серозных менингитах вирусной этиологии СМЖ прозрачна или слегка опалесцирует. Плеоцитоз небольшой (редко до 1000) с преобладанием лимфоцитов. У части больных в начале заболевания могут преобладать нейтрофилы, что характерно для более тяжелого течения и менее благоприятного прогноза. Общий белок в пределах 0, 6-1, 6 г/л или нормальный. У части больных выявляется снижение концентрации белка, обусловленное гиперпродукцией ликвора.
ЗАКРЫТАЯ ЧЕРЕПНО-МОЗГОВАЯ ТРАВМА
Проницаемость мозговых сосудов в остром периоде черепно-мозговой травмы в несколько раз превышает проницаемость периферических сосудов и находится в прямой зависимости от степени тяжести травмы. Для определения тяжести поражения в остром периоде можно использовать ряд ликворологических и гематологических тестов. Сюда относятся: степень выраженности и длительность наличия гиперпротеинорахии как теста, характеризующего глубину дисгемических расстройств в мозге и проницаемости гематоликворного барьера; наличие и выраженность эритроархии как теста, достоверно характеризующего продолжающееся внутримозговое кровотечение; наличие в течение 9-12 дней после травмы выраженного нейтрофильного плеоцитоза, что служит указанием на ареактивность тканей, ограничивающих ликворные пространства и угнетение санирующих свойств клеток паутинной оболочки или присоединения инфекции.
— Сотрясение головного мозга: СМЖ обычно бесцветна, прозрачна, не содержит эритроцитов или их количество незначительно. В 1-2 день после травмы цитоз нормальный, на 3-4 день появляется умеренно выраженный плеоцитоз (до 100 в 1 мкл), который снижается до нормальных цифр на 5-7 день. В ликворограмме лимфоциты с наличием незначительного количества нейтрофилов и моноцитов, макрофаги, как правило, отсутствуют. Уровень белка в 1-2 день после травмы нормальный, на 3-4 день он повышается до 0, 36-0, 8 г/л и к 5-7 дню возвращается к норме.
— Ушиб головного мозга: количество эритроцитов колеблется от 100 до 35000 а при массивном субарахноидальном кровоизлиянии достигает 1-3 млн. В зависимости от этого цвет СМЖ может быть от сероватого до красного. Из-за раздражения мозговых оболочек развивается реактивный плеоцитоз. При ушибах легкой и средней степени тяжести плеоцитоз на 1-2 день в среднем равен 160 в 1 мкл, а при тяжелой степени достигает несколько тысяч. На 5-10 сутки плеоцитоз достоверно снижается, но не достигает нормы и в последующие 11-20 сутки. В ликворогамме лимфоциты, часто макрофаги с гемосидерином. Если характер плеоцитоза меняется на нейтрофильный (70-100% нейтрофилов) — развился гнойный менингит как осложнение. Содержание белка при легкой и средней тяжести в среднем 1 г/л и не приходит к норме к 11-20 суткам. При тяжелых повреждениях головного мозга уровень белка может достигать 3-10 г/л (часто заканчивается летальным исходом).
При черепно-мозговой травме энергетический обмен мозга переключается на путь анаэробного гликолиза, что ведет к накоплению в нем молочной кислоты, и, в конечном итоге, к ацидозу мозга.
Исследование параметров, отражающих состояние энергетического обмена мозга, позволяет судить о тяжести течения патологического процесса. Снижение артериовенозной разницы по рО2 и рСО2, увеличение потребления мозгом глюкозы, нарастание веноартериальной разницы по молочной кислоте и увеличение ее в ликворе. Наблюдаемые изменения являются результатом нарушения деятельности ряда ферментных систем и не могут быть компенсированы кровоснабжением. Необходимо стимулировать нервную деятельность больных.
ГЕМОРРАГИЧЕСКИЙ ИНСУЛЬТ
Цвет ликвора зависит от примеси крови. У 80-95% больных на протяжении первых 24-36 ч СМЖ содержит явную примесь крови, а в более поздний срок она либо кровянистая, либо ксантохромная. Однако у 20-25% пациентов при небольших очагах, расположенных в глубинных отделах полушарий, или в случае блокады ликворопроводящих путей вследствие быстро развивающегося отека мозга эритроциты в СМЖ не определяются. Кроме того, эритроциты могут отсутствовать при проведении люмбальной пункции в самые первые часы после начала кровоизлияния, пока кровь достигает спинального уровня. Такие ситуации являются поводом к диагностическим ошибкам — постановке диагноза «ишемический инсульт». Наибольшее количество крови обнаруживается при прорывах крови в желудочковую систему. Выведение крови из ликворных путей начинается с первых же суток заболевания и продолжается в течение 14-20 дней при черепно-мозговых травмах и инсультах, а при аневризмах сосудов головного мозга до 1-1, 5 месяцев и не зависит от массивности кровоизлияния, а от этиологии процесса.
Вторым важным признаком изменения СМЖ при геморрагическом инсульте является ксантохромия, выявляемая у 70-75% больных. Она появляется на 2-е сутки и исчезает через 2 недели после инсульта. При очень большом количестве эритроцитов ксантохромия может появиться уже через 2-7 часов.
Увеличение концентрации белка наблюдается у 93, 9% больных и количество его колеблется от 0, 34 до 10 г/л и выше. Гипрепротеинорахия и повышенное содержание билирубина могут сохраняться длительное время и, наряду с ликвородинамическими нарушениями, могут быть причиной менингеальных симптомов, в частности головных болей, даже спустя 0, 5 — 1 год после субарахноидального кровоизлияния.
Плеоцитоз выявляют почти у 2/3 пациентов, он носит нарастающий в течение 4-6 дней характер, количество клеток колеблется от 13 до 3000 в 1 мкл. Плеоцитоз связан не только с прорывом крови в ликворные пути, но и с реакцией оболочек мозга на излившуюся кровь. Представляется важным определять в таких случаях истинный цитоз ликвора. Иногда при кровоизлияниях в мозг цитоз остается нормальным, что связано с ограниченными гематомами без прорыва в ликворное пространство, либо с ареактивностью оболочек мозга.
При субарахноидальных кровоизлияниях примесь крови может быть настолько велика, что ликвор визуально почти не отличим от чистой крови. В 1-й день количество эритроцитов, как правило, не превышает 200-500 х 109/л, в дальнейшем их количество увеличивается до 700-2000х109/л. В самые первые часы после развития небольших по объему субарахноидальных кровоизлияний при люмбальной пункции может быть получен прозрачный ликвор, однако к концу 1-х суток в нем появляется примесь крови. Причины отсутствия примеси крови в СМЖ могут быть те же, что при геморрагическом инсульте. Плеоцитоз, в основном нейтрофильный, свыше 400-800х109/л, к пятым суткам сменяется лимфоцитарным. Уже через несколько часов после кровоизлияния могут появиться макрофаги, которые можно считать маркерами субарахноидального кровоизлияния. Повышение общего белка обычно соответствует степени кровоизлияния и может достигать 7-11 г/л и выше.
ИШЕМИЧЕСКИЙ ИНСУЛЬТ
СМЖ бесцветна, прозрачна, у 66% цитоз остается в пределах нормы, у остальных повышается до 15-50х109/л, в этих случаях вы- являются характерные инфаркты мозга, близко расположенные к ликворным путям. Плеоцитоз, преимущественно лимфоидно-нейтрофильный, обусловлен реактивными изменениями вокруг обширных ишемических очагов. У половины больных содержание белка определяется в пределах 0, 34-0, 82 г/л, реже до 1 г/л. Повышение концентрации белка обусловлено некрозом мозговой ткани, повышением проницаемости гематоэнцефалического барьера. Содержание белка может увеличиваться к концу первой недели после инсульта и держатся свыше 1, 5 мес. Довольно характерным для ишемического инсульта является белково-клеточная (увеличение содержания белка при нормальном цитозе) или клеточно-белковая диссоциация.
АБСЦЕСС ГОЛОВНОГО МОЗГА
Для начальной фазы формирования абсцесса характерны нейтрофильный плеоцитоз и небольшое повышения белка. По мере развития капсулы, плеоцитоз уменьшается и нейтрофильный его характер сменяется лимфоидным, причем, чем больше развитие капсулы, тем менее выражен плеоцитоз. На этом фоне внезапное появление резко выраженного нейтрофильного плеоцитоза свидетельствует о прорыве абсцесса. Если же абсцесс располагался вблизи желудочковой системы или поверхности мозга цитоз составит от 100 до 400 в 3 мкл. Незначительный плеоцитоз или нормальный цитоз может быть тогда, когда абсцесс был отграничен от окружающей мозговой ткани плотной фиброзной или гиалинизированной капсулой. Зона воспалительной инфильтрации вокруг абсцесса в этом случае отсутствует или слабо выражена.
ОПУХОЛИ ЦНС
Наряду с белково-клеточной диссоциацией, считающейся характерной для опухолей, может иметь место плеоцитоз при нормальном содержанни белка в ликворе. При глиомах больших полушарий, независимо от их гистологии и локализации, повышение белка в ликворе наблюдается в 70, 3% случаев, причем при незрелых формах — в 88%. Нормальный или даже гидроцефальный состав желудочковой и спинальной жидкости может иметь место как при глубинных, так и при врастающих в желудочки глиомах. Это, в основном, наблюдается при зрелых диффузнорастущих опухолях (астроцитомы, олигодендроглиомы), без явных очагов некроза и кистообразования и без грубого смещения желудочковой системы. В то же время те же опухоли, но с грубым смещением желудочков, обычно сопровождаются повышением количества белка в ликворе. Гиперпротеинорахия (от 1 гл и выше) наблюдается при опухолях, расположенных на основании мозга. При опухолях гипофиза содержание белка колеблется от 0, 33 до 2, 0 гл. Степень сдвига протеинограммы находится в прямой зависимости от гистологической природы опухоли: чем злокачественнее опухоль, тем грубее изменения в белковой формуле ликвора. Появляются бета-липопротеиды, не обнаруживаемые в норме, снижается содержание альфа-липопротеидв.
У больных с опухолями мозга, независимо от их гистологической природы и локализации, довольно часто имеет место полиморфный плеоцитоз. Клеточная реакция обусловлена особенностями биологических процессов, протекающих в опухоли на определенных этапах ее развития (некрозы, геморрагии), обусловливающих реакцию. Окружающих опухоль тканей мозга и оболочек. Клетки опухоли больших полушарий мозга в жидкости из желудочков могут быть обнаружены в 34, 4%, а в спинальном ликворе — от 5, 8 до 15 % всех наблюдений. Основным фактором, обусловливающим попадание клеток опухоли в ликвор, является характер строения ткани опухоли (бедность связующей стромы), отсутствие капсулы, а также расположение новообразования вблизи ликворных пространств.
ХРОНИЧЕСКИЕВОСПАЛИТЕЛЬНЫЕ ЗАБОЛЕВАНИЯ (арахноидиты, арахноэнцефалиты, перивентрикулярные энцефалиты)
Содержание белка в спинномозговой жидкости у большинства больных остается в пределах нормы или незначительно повышено (до 0, 5 г/л). Увеличение белка до 1 г/л наблюдается крайне редко и чаще при менингоэнцефалитах, нежели при арахноидитах.
Источник: «МЕТОДЫ ЛАБОРАТОРНОГО ИССЛЕДОВАНИЯ ЦЕРЕБРОСПИНАЛЬНОЙ ЖИДКОСТИ», УЧЕБНОЕ ПОСОБИЕ, Москва 2008г. МОНИКИ. Авторы: к. м. н. Н. В. Инюткина, д. м. н. , проф. С. Н. Шатохина, к. м. н. М. Ф. Фейзулла, м. н. с. В. С. Кузнецова
Статья добавлена 19 мая 2016 г.
Источник
Гнойный менингит (Бактериальный менингит)
Гнойный менингит — воспалительный процесс, возникающий в мягкой оболочке головного мозга при проникновении в нее гноеродных микроорганизмов (пневмококков, менингококков, стрептококков и пр.). Гнойный менингит характеризуется высокой температурой тела, интенсивной головной болью, тошнотой, рвотой, нарушениями со стороны черепно-мозговых нервов, ранним появлением менингеальных симптомов, гиперестезией, расстройством сознания, психомоторным возбуждением. Диагностировать гнойный менингит можно на основании типичной клинической картины и данных анализа цереброспинальной жидкости. Гнойный менингит является показанием к обязательному проведению антибиотикотерапии. Применяются противоотечные препараты, глюкокортикостероиды, транквилизаторы, противосудорожные средства и пр. симптоматическая терапия.
Общие сведения
Гнойный менингит — это воспаление мозговых оболочек (менингит), имеющее бактериальную этиологию. Гнойный менингит встречается с частотой 3,3 случаев на 100 тыс. населения. Заболеванию подвержены все возрастные категории, но наиболее часто гнойный менингит развивается у детей до 5 лет. Отмечено, что гнойный менингит часто возникает на фоне ослабленного состояния иммунной системы. Повышение заболеваемости наблюдается в зимне-весенний период. С начала 90-х годов прошлого века произошло существенное снижение заболеваемости гнойным менингитом, уменьшение числа летальных исходов и случаев развития тяжелых осложнений.
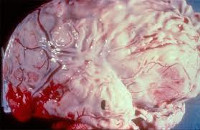
Гнойный менингит
Причины возникновения гнойного менингита
К развитию гнойного менингита может приводить не только менингококковая инфекция, но также пневмококки, гемофильная палочка и другие бактерии. Почти половина случаев гнойного менингита приходится на долю гемофильной палочки. В 20% причиной гнойного менингита является менингококк, в 13% случаев — пневмококк. У новорожденных гнойный менингит зачастую возникает в результате стрептококковой инфекции, сальмонеллеза или инфицирования кишечной палочкой.
В зависимости от механизма проникновения возбудителя в оболочки головного мозга в неврологии выделяют первичный и вторичный гнойный менингит. Первичный гнойный менингит развивается при гематогенном распространении возбудителя из полости носа или глотки, куда он попадает из внешней среды. Заражение происходит от больных лиц и носителей воздушно-капельным и контактным путем. Прямое инфицирование мозговых оболочек возможно при переломе черепа и открытой черепно-мозговой травме, открытых повреждениях сосцевидного отростка и придаточных пазух носа, недостаточно тщательном соблюдении правил асептики в ходе нейрохирургических вмешательств.
Вторичный гнойный менингит возникает на фоне имеющегося в организме первичного септического очага, инфекция из которого проникает в оболочки головного мозга. Контактное распространение гноеродных микроорганизмов может наблюдаться при абсцессе головного мозга, остеомиелите костей черепа, септическом синустромбозе. Гематогенное и лимфогенное распространение возбудителя возможно из инфекционного очага любой локализации, но наиболее часто происходит при длительно протекающих инфекциях лор-органов (остром среднем отите, хроническом гнойном среднем отите, синуситах).
Проникновению возбудителей гнойного менингита через гематоэнцефалический барьер способствует ослабленное состояние иммунной системы организма, которое может быть вызвано частыми ОРВИ, гиповитаминозом, перенесенным стрессом, физическими перегрузками, резкой сменой климата.
Классификация гнойного менингита
В зависимости от тяжести клинических проявлений гнойный менингит классифицируется на легкую, среднетяжелую и тяжелую формы. Тяжелые формы заболевания наблюдаются в основном на фоне резкого снижения иммунитета и у пациентов с удаленной селезенкой.
По особенностям течения выделяют молниеносный, абортивный, острый и рецидивирующий гнойный менингит. Наиболее часто встречается острый гнойный менингит с типичными общемозговыми и оболочечными симптомами. Молниеносное течение гнойного менингита с первых часов заболевания характеризуется быстрым нарастанием отека головного мозга, приводящего к нарушению сознания и витальных функций. Абортивный вариант отличается стертой клинической картиной, в которой на первый план выходят симптомы интоксикации. Рецидивирующий гнойный менингит может наблюдаться при недостаточном или запоздалом лечении острой формы заболевания, а также при наличии в организме хронического очага гнойной инфекции.
Симптомы гнойного менингита
Инкубационный период первичного гнойного менингита в среднем длится от 2 до 5 суток. Типично острое начало с резкого повышения температуры тела до 39-40°С, сильного озноба, интенсивной и нарастающей головной боли, тошноты и многократной рвоты. Могут наблюдаться психомоторное возбуждение, бред, нарушения сознания. В 40% случаев гнойный менингит протекает с судорожным синдромом. Специфичные для менингита оболочечные симптомы (симптом Кернига, Брудзинского, Гийена, ригидность затылочных мышц) выражены с первых часов заболевания и усиливаются на 2-3-й день. Типичны выраженная гиперестезия и снижение брюшных рефлексов на фоне общего повышения глубоких рефлексов. Возможно появление диффузной сыпи геморрагического характера.
Очаговая симптоматика, сопровождающая гнойный менингит, чаще всего заключается в нарушении функций различных черепно-мозговых нервов. Наиболее часто наблюдается поражение глазодвигательных нервов, приводящее к двоению, развитию косоглазия, опущению верхнего века и появлению разницы в размере зрачков (анизокории). Реже отмечается неврит лицевого нерва, поражение тройничного нерва, расстройство функции зрительного нерва (выпадение полей зрения, снижение остроты зрения) и преддверно-улиткового нерва (прогрессирующая тугоухость). Более тяжелая очаговая симптоматика свидетельствует о распространении воспалительных изменений на вещество головного мозга или о развитии сосудистых нарушений по типу ишемического инсульта, обусловленных васкулитом, рефлекторным спазмом или тромбозом сосудов головного мозга.
При переходе воспалительного процесса на вещество мозга говорят о развитии менингоэнцефалита. При этом гнойный менингит протекает с присоединением характерной для энцефалита очаговой симптоматики в виде парезов и параличей, нарушений речи, изменений чувствительности, появления патологических рефлексов, повышения мышечного тонуса. Возможны гиперкинезы, галлюцинаторный синдром, нарушения сна, вестибулярная атаксия, расстройства поведенческих реакций и памяти. Распространение гнойного процесса на желудочки мозга с развитием вентрикулита проявляется спастическими приступами по типу горметонии, сгибательными контрактурами рук и разгибательными ног.
Осложнения гнойного менингита
Ранним и грозным осложнением, которым может сопровождаться гнойный менингит, является отек головного мозга, приводящий к сдавлению мозгового ствола с расположенными в нем жизненно важными центрами. Острый отек головного мозга, как правило, возникает на 2-3-й день заболевания, при молниеносной форме — в первые часы. Клинически он проявляется двигательным беспокойством, нарушением сознания, расстройством дыхания и нарушениями со стороны сердечно-сосудистой системы (тахикардия и артериальная гипертензия, в терминальной стадии сменяющиеся брадикардией и артериальной гипотонией).
Среди прочих осложнений гнойного менингита могут наблюдаться: септический шок, надпочечниковая недостаточность, субдуральная эмпиема, пневмония, инфекционный эндокардит, пиелонефрит, цистит, септический панофтальмит и др.
Диагностика гнойного менингита
Типичные клинические признаки, наличие менингеальных симптомов и очаговой неврологической симптоматики в виде поражения черепно-мозговых нервов, как правило, позволяют неврологу предположить у пациента гнойный менингит. Более затруднительна диагностика в случаях, когда гнойный менингит имеет абортивное течение или возникает вторично на фоне симптомов существующего септического очага другой локализации. Чтобы подтвердить гнойный менингит необходимо произвести люмбальную пункцию, в ходе которой выявляется повышенное давление ликвора, его помутнение или опалесцирующая окраска. Последующее исследование цереброспинальной жидкости определяет увеличенное содержание белка и клеточных элементов (в основном за счет нейтрофилов). Выявление возбудителя производится в ходе микроскопии мазков цереброспинальной жидкости и при ее посеве на питательные среды.
С диагностической целью производят также анализ крови и отделяемого элементов кожной сыпи. При предположении о вторичном характере гнойного менингита проводятся дополнительные обследования, направленные на поиск первичного инфекционного очага: консультация отоларинголога, пульмонолога, терапевта; рентгенография околоносовых пазух, отоскопия, рентгенография легких.
Дифференцировать гнойный менингит необходимо от вирусного менингита, субарахноидального кровоизлияния, явлений менингизма при других инфекционных заболеваниях (сыпном тифе, лептоспирозе, тяжелых формах гриппа и др.).
Лечение гнойного менингита
Все имеющие гнойный менингит пациенты подлежат лечению в условиях стационара. Таким больным должна быть неотложно проведена люмбальная пункция и бактериоскопическое исследование ликвора. Сразу же после установления этиологии менингита пациенту назначается антибиотикотерапия. В большинстве случаев она представляет собой сочетание ампициллина с препаратами цефалоспоринового ряда (цефтриаксоном, цефотаксимом, цефтазидимом). При гнойном менингите неустановленной этиологии стартовая терапия заключается во внутримышечном введении аминогликозидов (канамицина, гентамицина) или их комбинации с ампициллином. Тяжело протекающий гнойный менингит может потребовать внутривенного или интратекального введения антибиотиков.
С целью уменьшения гидроцефалии и отека мозга при гнойном менингите назначают дегидратационную терапию (фуросемид, маннитол). Патогенетическое лечение гнойного менингита также включает применение глюкокортикостероидных препаратов (дексаметазона, преднизолона), дозы которых зависят от тяжести заболевания. Наряду с этим производится необходимая симптоматическая терапия. При нарушениях сна назначаются транквилизаторы; для купирования психомоторного возбуждения и судорог — литические смеси (хлорпромазин, дифенгидрамин, тримеперидина), диазепам, вальпроевая кислота; при гиповолемии и развитии инфекционно-токсического шока проводится инфузионная терапия.
В восстановительном периоде после перенесенной острой фазы гнойного менингита рекомендован прием ноотропных и нейропротекторных препаратов, витаминотерапия и общеукрепляющее лечение. Лечение пациентов, имеющих вторичный гнойный менингит, должно включать ликвидацию первичного септического очага, в том числе и путем хирургического вмешательства (санирующая операция при среднем отите, фронтотомия, этмоидотомия, сфенотомия, удаление внутримозгового абсцесса и т. п.).
Прогноз гнойного менингита
По некоторым данным в 14% случаев гнойный менингит приводит к летальному исходу. Однако при своевременно начатом и корректно проведенном лечении гнойный менингит имеет в основном благоприятный прогноз. После перенесенного менингита может наблюдаться астения, ликворно-динамические нарушения, нейросенсорная тугоухость, отдельные слабо выраженные очаговые симптомы. Тяжелые последствия гнойного менингита (гидроцефалия, амавроз, глухота, деменция, эпилепсия) в наше время являются редкостью.
Профилактика гнойного менингита
На сегодняшний день наиболее эффективным способом, позволяющим предупредить гнойный менингит, является вакцинация. Прививки проводится против основных возбудителей гнойного менингита: гемофильной палочки, менинго- и пневмококков. В России эти вакцины не считаются обязательными и вводятся по показаниям или по желанию пациентов.
Вакцинация против гемофильной инфекции проводится в основном детям в возрасте от 3 месяцев до 5 лет и людям, страдающим иммунодефицитными состояниями в результате ВИЧ-инфекции, проведения иммуносупрессивной терапии онкозаболеваний, удаления тимуса или селезенки и т. п. Вакцинация против менингококковой инфекции рекомендована детям после 18 месяцев и взрослым. Детям до 18 месяцев вакцинация проводится по эпидемическим показаниям (например, если менингококковый гнойный менингит диагностирован у одного из членов семьи). В регионах, опасных по менингококковому гнойному менингиту, вакцинация должна проводиться пациентам с иммунодефицитом и людям, имеющим анатомические дефекты черепа. Вакцинация против пневмококковой инфекции показана часто болеющим детям, пациентам с частыми пневмониями и отитами, в случаях пониженного иммунитета.
Источник